сотрет не помогает что делать
Опыт применения Сотрета у больных со среднетяжелыми и тяжелыми формами акне
Опубликовано в журнале:
Врач, №7, 2013
С. Остапенко
Медико-санитарная часть №5, Самара Сотрет (изотретиноин) – эффективное медикаментозное средство для системной терапии акне, действующее на все основные звенья патогенеза заболевания: образование кожного сала, комедогенез, колонизацию P. acnes. Прием препарата рекомендуется при среднетяжелых и тяжелых формах акне, высокой степени рубцевания, отсутствии эффекта традиционных методов лечения.
Ключевые слова: акне, системные ретиноиды, Сотрет.
Experience with Sotret in patients with moderate and severe acne
S. Ostapenko
Medical Sanitary Unit Five, Samara Sotret (isotretinoin) is an effective medication for systemic therapy of acne, which acts on the basic components of the pathogenesis of the disease: sebum production, comedogenesis, and P. acnes colonization. The drug is recommended in cases of moderate-to-severe acne, high scarring, and ineffective traditional treatments.
Key words: acne, systemic retinoids, Sotret.
Акне (вульгарные угри) – хроническое кожное заболевание, которое является самой распространенной дерматологической патологией в подростковом периоде. В 30% случаев угревая сыпь сохраняется и в зрелом возрасте. Более чем в 1/3 случаев это заболевание требует длительного лечения.
Наиболее часто при акне поражаются лицо и верхняя часть шеи, но в процесс могут быть вовлечены также грудь, спина и плечи. На коже появляются элементы сыпи – папулы, пустулы, кисты и др. В лечении акне используют местные бактерицидные средства (при легких формах – препараты, содержащие бензоилпероксид, менее эффективен триклозан), антибиотики (наружно применяются доксициклин, эритромицин, клиндамицин, спирамицин или антибиотики тетрациклинового ряда). У женщин эффективна гормональная терапия акне – применяют комбинированные препараты эстрогена и прогестогена. Наиболее эффективен ципротерон в сочетании с эстрогеном; можно использовать спиронолактон (особенно у больных с синдромом поликистоза яичника, а также локальные инъекции кортизона). В настоящее время разрабатываются новые концепции и перспективы в лечении акне, предусматривающие возможность использования генетических методов лечения. Ученые ищут возможные гены, ответственные за данную патологию; планируется также использование фагов, элиминирующих бактерии.
Ретиноиды – производные (изомеры) витамина А (третиноин, изотретиноин, адапален, тазаротен) влияют на жизненный цикл клеток кожи и таким образом нормализируют кератинизацию и десквамацию эпителиальных клеток. Для местного применения используют гели, содержащие ретиноиды: Эффезел (адапален и бензоила пероксид, оказывающий противомикробное действие и не вызывающий резистентности), Клензит (адапален), Изотрексин (включающий изотретиноин и антибиотик эритромицин). Показано, что эритромицин в сочетании с изотретиноином эффективен против эритромицинрезистентных штаммов Propionibacterium acnes, однако препараты с адапаленом (по данным Global Alliance to Improve Outcomes in Acne) являются препаратами 1-го выбора при лечении акне.
Для терапии тяжелых и резистентных форм акне ретиноиды применяют внутрь. Синтетическое производное витамина А – изотретиноин (13-cis ретиновая кислота, Сотрет) считается самым эффективным средством для системного лечения акне. Оптимальной ежедневной дозой считается 0,5 мг на 1 кг массы тела; при приеме лекарства в такой дозировке улучшение наблюдается уже через 2–4 нед. Реакция на терапию примерно у 50% пациентов сопровождается кратковременным ухудшением состояния кожи, связанным с высвобождением филаментов и воспалительным преобразованием комедонов. Повышение дозы до 1 мг/кг показано при тяжелой себорее, выраженном конглобатном акне или при локализации акне на туловище. Более низкие суточные дозы (0,2 мг/кг) также эффективны, однако необходима более длительная терапия, иначе количество рецидивов существенно увеличивается.
Изотретиноин является единственным терапевтическим средством лечения акне, которое влияет на 4 главных звена патогенеза заболевания: себорею, нарушения ороговения, воспаление и размножение бактерий P. acnes. Он интенсивно снижает секрецию сальных желез, одновременно уменьшая их, причем не обладает гормональным эффектом. Препарат устраняет инфраинфундибулярный ретенционный гиперкератоз и оказывает противовоспалительное действие. Кроме того, он подавляет бактериальную кожную флору в рамках себостатического эффекта, не обладая антибактериальной активностью. Изотретиноин также характеризуется иммуномодулирующими свойствами.
При акне происходят качественные и количественные изменения продукции кожного сала сальными железами и нарушения кератинизации в сально-волосяных протоках. Эти процессы контролируются нейрогуморальными механизмами. Среди гормональных нарушений наиболее важен уровень продукции андрогенов в организме. В результате возросшего влияния андрогенов на сально-волосяные фолликулы в андрогензависимых участках кожного покрова (лицо, спина, грудь, плечи) отмечаются избыточная продукция кожного сала в сальных железах, а также повышенная адгезия корнеоцитов, выстилающих сально-волосяные протоки, что затрудняет их десквамацию в просвет протока. Эти нарушения влекут за собой замедление или прекращение перемещения кожного сала и ороговевших клеточных масс по протоку. В результате происходит его закупорка, что клинически проявляется формированием открытых и (или) закрытых комедонов. В таких условиях создается благоприятная среда для роста и размножения бактериальной флоры (P. acnes, Staphylococcus epidermidis), что, в свою очередь, способствует развитию реактивного и иммунного воспаления в окружающей дерме. Клинически это проявляется образованием воспалительных элементов акне разной степени тяжести (папулы, пустулы, узлы, кисты, конглобатные, абсцедирующие, флегмонозные угри).
Нами изучена эффективность изотретиноина (Сотрета) как препарата для системной терапии среднетяжелых и тяжелых форм акне. Под наблюдением находились 18 пациентов с акне. Диагностическое обследование включало:
Дополнительно проводили: общий анализ крови; биохимический анализ крови (содержание билирубина, холестерина, β-липопротеидов, липидов, триглицеридов аланин- и аспартатаминотрансферазы, щелочной фосфатазы, креатинина, мочевины, глюкозы); у женщин – тест на беременность.
Больные были в возрасте от 19 до 26 лет: 8 пациентов мужского пола (2 больных – от 19 до 20 лет; 1 – 20 лет, 2 – 22 лет, 2 – 23 года и 1 – 25 лет) и 10 – женского (3 – в возрасте 19 лет, 2 – 20 лет, 2 – 21 года, 1 – 23 лет и 2 – 26 лет).
Длительность акне от 2 до 3 лет отмечалась у 5 пациентов; в пределах 4–6 лет – у 8; в 5 случаях угри существовали около 10 лет. На сезонное обострение акне (ухудшение состояния кожи в зимнее время) указали 12 больных.
Генетическая предрасположенность к заболеванию отмечена у 11 пациентов: у 4 обследованных акне страдала мать, у 3 – отец, у 2 – сестра и у 2 – брат. Обострение угревой сыпи на фоне нервно-психических перегрузок отметили 4 пациента, после переохлаждения – 2, в результате погрешностей в диете – 5.
Лекарственная аллергия в анамнезе отмечена у 2 обследованных: соответственно на пенициллин и сульфадиметоксин. Сопутствующие кожные проявления в виде себореи зарегистрированы у 5 больных (у 2 – выраженная себорея волосистой части головы), ладонно-подошвенного гипергидроза – у 3, атрофических полос – у 4, отека Квинке – у 1. Сопутствующая соматическая патология: хронический гастрит (у 4), хронический дуоденит (у 1), миопия средней степени (у 1), киста яичника и диффузный зоб (у 1), поликистоз (у 2 больных).
Клиническая картина заболевания включала невоспалительные (открытые и закрытые комедоны) и воспалительные элементы в виде папул, пустул, конглобатных, абсцедирующих и узловато-кистозных акне. Узловато-кистозная форма была зарегистрирована у всех пациентов, папуло-пустулезная – у 9, конглобатная – у 8 и абсцедирующая – у 5 пациентов. Высыпания у больных локализовались на лице, шее, спине; на груди угревая сыпь была у 9, на верхних конечностях в области плеч – у 7 пациентов. Среднее количество патологических элементов составляло: на коже лица – 25,1 на площади 5Ч5 см, на коже спины – 39,2 на площади 20Ч20 см. Распространенное поражение наблюдалось у 7 больных. Среднетяжелое течение акне зафиксировано у 10 пациентов, тяжелое – у 5, очень тяжелое – у 3. Осложнения в виде экскориаций были у 2, атрофических рубцов – у 10, индуративных рубцов – у 7 обследованных. У 6 пациентов отмечены келоидные рубцы, в том числе на лице. Дисхромия была представлена в виде как гиперпигментации (у 10), так и гипопигментации (у 8). Среднее количество атрофических рубцов на коже спины составляло 44, индуративных – 30. Все угревые высыпания отнесены к конституциональным юношеским угрям, а осложненные экскориациями акне у 2 пациентов – к экскориированным.
Предшествующая терапия акне включала системное лечение до 1 мес доксициклином (у 5), рифампицином (у 1), витаминами группы В (у 3); крем Ретин А местно применяли 3 пациента, растворы салициловой кислоты – 4, гель бензоилпероксид – 6, солнцезащитные кремы – 3. Таким образом, 6 больных никогда не использовали системных препаратов для лечения акне. У 2 пациентов отмечен раздражающий эффект Ретина А и у 4 – салициловой кислоты (жжение и зуд).
Основными критериями для выбора Сотрета в качестве препарата для системной терапии были:
Сотрет назначали с учетом массы тела пациента из расчета 0,5 мг/кг в сутки, что составляло 20–40 мг/сут. Длительность курса терапии – от 5 до 8 мес (в зависимости от выраженности клинического эффекта). Больным, которые применяли препарат более 2 мес, снижали дозу на 0,1 мг/кг в сутки ежемесячно. До начала лечения и ежемесячно в процессе терапии проводили клинико-лабораторный мониторинг биохимических показателей сыворотки крови для исключения лабораторных признаков заболеваний печени, почек, гиперлипидемии, сахарного диабета.
В зависимости от клинических проявлений акне в качестве местных препаратов 6 пациентов использовали крем Скинорен, 12 – гамма эфаклар, 16 – солнцезащитный крем с фактором защиты 50.
Клинический контроль проводили ежемесячно с учетом уменьшения количества патологических элементов, а также снижения степени тяжести акне и выраженности рубцовых изменений.
У всех пациентов наблюдались побочные эффекты в виде сухости кожи, слизистых оболочек глаз, губ. Однако эти явления легко устранялись с помощью увлажняющих кремов. У 2 пациентов в 1-й месяц приема Сотрета появились носовые кровотечения, но после снижения дозы препарата они прекратились. Клиническое улучшение было достигнуто у всех пациентов уже через 1 мес после начала приема Сотрета с регрессом патологических элементов на 30–35%. После 2 мес лечения наблюдался значительный эффект с регрессом патологических элементов на 55–60%. У 4 пациентов с тяжелым течением акне улучшение на 70–75% наступило через 3 мес терапии. У 9 пациентов (у 3 – очень тяжелое течение и у 6 – тяжелое) прием препарата был продлен до 8 мес. Клинический эффект в виде улучшения в этой группе составил 80%. Кроме уменьшения количества элементов, снижались частота и выраженность рубцовых изменений, а также степень тяжести акне (рис. 1, 2).
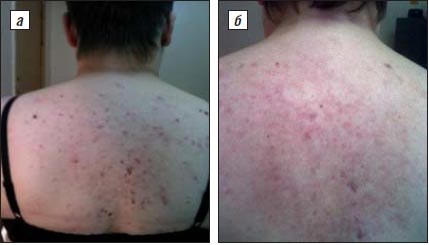
Рис. 1. Элементы сыпи при акне у больной А., 24 лет (узловатые акне тяжелой степени, конглобатные акне, IV степень тяжести, по классификации из Европейского руководства по лечению акне, 2012 г.):
а – до лечения; б – после лечения
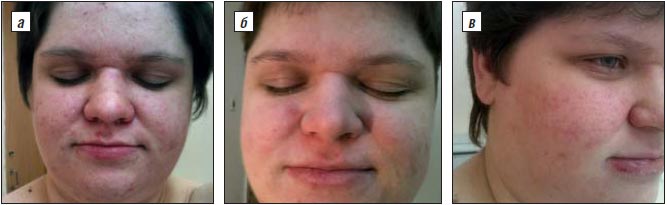
Рис. 2. Проявления акне у больной В., 26 лет (тяжелые папулопустулезные акне, III степень тяжести):
а – до лечения; б – в ходе терапии; в – после лечения
Полученные результаты показали, что изотретиноин (Сотрет) оказывает выраженное себостатическое действие и уменьшает количество P. acnes. Подавление секреции кожного сала (на 85%) происходит за счет сокращения размеров сальной железы (на 50–90%), снижения выраженности воспалительной реакции в этой области. Плотность заселения бактериями P. acnes сально-волосяного аппарата уменьшается на несколько порядков. Изотретиноин снижает сцепление кератиноцитов в сальных фолликулах, препятствуя таким образом формированию микрокомедонов, инициирующих воспалительный процесс.
Таким образом, Сотрет (изотретиноин) является эффективным медикаментозным средством для системной терапии среднетяжелых и тяжелых форм акне. Препарат действует на все основные звенья патогенеза акне – образование кожного сала, комедогенез, колонизацию P. acnes.
Прием Сотрета рекомендуется при среднетяжелых и тяжелых формах акне, высокой степени рубцевания, отсутствии значительного клинического эффекта традиционных методов лечения угревой сыпи.
Рекомендуемая литература
Эффективность vs неэффективность системных ретиноидов при акне
Акне (вульгарные угри) считается одним из наиболее распространенных заболеваний кожи [1]. По разным данным, частота его встречаемости составляет 60–85%. Чаще патологией страдают подростки и лица молодого возраста. Акне занимает первое место среди заболеваний кожи в данной популяции.
Несмотря на обилие лекарственных средств, лечение акне остается сложной задачей.
Недостаточная эффективность лечения, ассоциированные с данной нозологией аффективные расстройства, такие как дисморфофобия и депрессия, существенно снижающие качество жизни больных и способствующие их социальной дезадаптации, обусловливают медико-социальную значимость проблемы.
Воспаление поддерживается липидными медиаторами: лейкотриенами, простагландинами и 15-гидроксиэтоксисатетраеновыми кислотами [2].
Синтез провоспалительных цитокинов осуществляется через NF-κβ или через Toll-подобные рецепторы (Toll-Like Receptors – TLRs). С помощью TLRs происходит высвобождение антимикробных пептидов (бета-дефенсинов) и металлопротеиназ, которые способствуют развитию воспаления и образованию рубцов при акне [3].
Кроме того, в многочисленных исследованиях установлено, что развитие акне происходит на фоне нескольких взаимосвязанных патогенетических процессов. Наиболее значимыми являются нарушение кератинизации, фолликулярный гиперкератоз, избыточная продукция жирового секрета, что сопровождается дисбалансом липидов и размножением микроорганизмов [4].
Усиление секреции кожного сала происходит за счет увеличения синтеза андрогенов или повышения чувствительности рецепторов к ним. Ранее установлено, что андрогены, такие как тестостерон, дегидроэпиандростерон сульфат и дигидротестостерон, регулируют гены, ответственные за рост сальных желез и выработку кожного сала. Фермент альфа-редуктаза катализирует превращение тестостерона в 5-альфа-дегидротестостерон, экспрессирующийся преимущественно в коже. У пациентов с акне выявлена более высокая активность 5-альфа-редуктазы 1-го типа [5].
Гиперандрогения приводит к изменению не только количественного, но и качественного состава себума. Концентрация альфа-линоленовой кислоты – регулятора дифференцировки кератиноцитов фолликула снижается. В результате нарушения последней развивается фолликулярный кератоз, приводящий к закупорке сальной железы.
В пубертатном периоде гипофиз секретирует гормон роста, который стимулирует выработку инсулиноподобных факторов роста. Себоциты содержат рецепторы к инсулиноподобным факторам роста, взаимодействие с которыми приводит к росту сальной железы. Эстрогены напрямую ингибируют секрецию тестостерона и участвуют в регуляции генов роста сальной железы. Нестабильный гормональный фон и низкий уровень эстрогенов также способствуют развитию акне.
Лечение акне зависит от степени его тяжести. Так, при легкой степени ограничиваются наружными средствами, при средней – назначают антибиотики.
Наиболее эффективными в терапии акне средней и тяжелой степени являются системные ретиноиды – изотретиноин. Изотретиноин показан пациентам с узловато-кистозными угрями и часто рецидивирующими воспалительными высыпаниями, у которых антибиотики оказались неэффективными, а также больным с тенденцией к разрешению акне в виде рубцов.
В последние годы спектр показаний для назначения изотретиноина расширяется, в том числе в отношении лечения единичных, но рецидивирующих высыпаний на лице. Ряду больных они доставляют много страданий. Прежде всего это относится к публичным лицам – артистам, танцорам, журналистам и т.д., которые хотят быстрого и стойкого эффекта.
Являясь комедонолитиком, системный изотретиноин воздействует на патологическую фолликулярную кератинизацию и функцию сальных желез. Несмотря на то что препарат не обладает прямым антибактериальным эффектом, он способен влиять на хемотаксис и фагоцитоз и таким образом уменьшать численность Cutibacterium [6]. Уже через две недели от начала лечения изотретиноином уменьшается продукция кожного сала. Как следствие, рост микроорганизмов и провоспалительных медиаторов резко сокращается.
На сегодняшний день изотретиноин является единственным препаратом, который эффективен в отношении большинства звеньев патогенеза акне. Это обусловлено молекулярными механизмами действия. Взаимодействуя с ядерными рецепторами, изотретиноин уменьшает дифференцировку клеток сальных желез, что способствует выраженному уменьшению размеров и активности себоцитов.
Изотретиноин назначается на шесть месяцев и более в дозе от 0,1 до 1,0 мг/кг в зависимости от тяжести заболевания. Обязательным условием является прием препарата во время еды.
К сожалению, из-за побочных эффектов, в первую очередь тератогенного действия, ряд врачей, прежде всего вследствие недостатка клинического опыта, ограничивают назначение изотретиноина.
Наиболее частыми нежелательными явлениями на фоне терапии изотретиноином считаются хейлит и сухость кожи. Иногда могут отмечаться ухудшение зрения в ночное время, конъюнктивит, повышенная фоточувствительность, транзиторная потеря волос, артралгия и миалгия, головная боль, транзиторное повышение печеночных трансаминаз, триглицеридов и холестерина. Однако частота развития перечисленных явлений крайне низка.
Ввиду тератогенного действия на центральную нервную систему и сердечно-сосудистую систему плода изотретиноин нельзя принимать во время беременности.
Бытует мнение, что после курса системных ретиноидов высока вероятность рождения ребенка с уродствами и планировать беременность следует только через два года по окончании лечения. Однако период полураспада изотретиноина в отличие от других ретиноидов (этретината и ацитретина) составляет 19 часов. Поэтому женщинам, получающим его, необходимо использовать средства контрацепции только в период терапии и еще в течение месяца по ее завершении. Чтобы минимизировать риск развития данного нежелательного явления, все пациентки детородного возраста перед началом лечения должны получить консультацию по поводу методов контрацепции.
Для лечения среднетяжелых и тяжелых форм акне уже несколько лет с успехом применяется Акнекутан, в производстве которого используется запатентованная технология Lidose® (Бельгия).
Как известно, изотретиноин относится к плохо растворимым соединениям и всасывается в пищеварительном тракте не полностью. Технология Lidose® предполагает добавление двух компонентов в состав каждой капсулы препарата Акнекутан (Гелюцира и Спана). Благодаря этому увеличивается растворенная фракция изотретиноина в капсуле и, как следствие, его абсорбция. Биодоступность увеличивается на 20% по сравнению с обычной формой изотретиноина. Это позволяет уменьшить количество изотретиноина в каждой капсуле, так как количество работающего вещества полностью соответствует таковому в оригинальном препарате (12 мг из 16 мг Акнекутана или 12 мг из 20 мг Роаккутана), а количество неактивного уменьшается на 50% (4 мг в Акнекутане и 8 мг в Роаккутане). В результате риск развития побочных эффектов снижается.
Необходимо отметить, что биодоступность Акнекутана в меньшей степени зависит от приема пищи, чем биодоступность обычной формы изотретиноина. Так, при приеме без пищи Акнекутан абсорбируется на 70%, препараты обычной формы изотретиноина – только на 38%.
Таким образом, применение изотретиноина в составе Акнекутана позволяет на 20% снизить количество принимаемого пациентом изотретиноина без ущерба для терапевтической эффективности, а также быть уверенным в том, что даже при неполном соблюдении пациентом правил по приему препарата с пищей курсовая доза изотретиноина будет набрана.
Рекомендуемая суточная доза Акнекутана составляет 0,4–0,8 мг/кг, курсовая – 100–120 мг/кг.
Под нашим наблюдением находилось 190 пациентов (105 (55,3%) женщин и 85 (44,7%) мужчин) в возрасте от 14 до 27 лет. Степень тяжести заболевания определяли с помощью дерматологического индекса акне (ДИА) путем подсчета воспалительных элементов – папул, пустул и узлов. У 114 (60%) больных диагностирована средняя степень тяжести, у 76 (40%) – тяжелая. Пациенты ранее применяли разные методы лечения многократными курсами: системные антибиотики, метронидазол, антиандрогены, наружные средства, плазмолифтинг, чистки, пилинги, мезотерапию, физиотерапевтические процедуры и др. Однако эффект был временный.
Акнекутан назначали после обследования, которое включало клинический и биохимический анализ крови, у женщин при наличии болезненных и обильных менархе – исследование гормонального профиля.
Способ применения Акнекутана – из расчета 0,4–0,8 мг/кг/сут во время приема пищи. Суточная доза зависела не только от массы тела, но и от выраженности клинических проявлений акне.
Для нивелирования проявлений ксероза и хейлита пациенты применяли крем для лица Перфэктоин и увлажняющие губные помады.
При достижении выраженного улучшения суточная доза Акнекутана постепенно снижалась.
Длительность лечения определялась сроками достижения кумулятивной дозы препарата – 100–120 мг/кг. В среднем она составила 32,4 ± 4,6 недели.
Лечение продолжали до достижения клинической ремиссии. Поэтому редукция показателей ДИА у всех пациентов составила 100% (рис. 1 и 2).
Нежелательные явления носили дозозависимый характер, наблюдались в первые три-четыре месяца и были представлены хейлитом (190 (100%) больных), ретиноевым дерматитом (180 (94,7%)), конъюнктивитом (17 (8,9%)), носовыми кровотечениями (7 (6,7%)), транзиторным повышением трансаминаз (75 (39,4%)), гиперлипидемией (38 (20%)), миалгиями и артралгиями (5 (2,6%)), головной болью (5 (2,6%)).
Побочные явления легко переносились пациентами и не были серьезными.
Нежелательные явления со стороны кожи и органов зрения легко купировались увлажняющими средствами, губными стиками, средствами искусственной слезы.
Изменения показателей клинического и биохимического анализа крови были незначительными и не превышали 20–30% от исходных значений.
При транзиторном повышении трансаминаз назначался гепатопротектор и снижалась суточная доза препарата.
Через один – три года после лечения рецидивы отмечены у девяти пациентов, из них восемь женщин и один мужчина. Эти пациенты были более тщательно обследованы гинекологом и эндокринологом. У шести выявлено повышение уровня тестостерона и дегидроэпиандростерона, у двух – поликистоз яичников по результатам ультразвукового исследования органов малого таза. В двух случаях отмечалось увеличение лютеинизирующего гормона и изменение соотношения «лютеинизирующий гормон/фолликулостимулирующий гормон» > 2. У всех пациенток в анамнезе нарушение менархе.
У двух пациентов (одна женщина и один мужчина) с повышенной массой тела диагностировано нарушение толерантности к глюкозе.
Полученные нами результаты свидетельствуют о высокой эффективности Акнекутана.
Необходимо отметить, что женщинам с рецидивирующими, устойчивыми к проводимой терапии вульгарными угрями и гормональными нарушениями, обусловленными прежде всего гиперандрогенией, рекомендуется лечение половыми гормонами. Прием пероральных гормонов уменьшает секрецию кожного сала, ингибирует эффекты андрогенов в сальных железах.
При угревой болезни используют три группы гормонов: эстрогены, которые подавляют овариальные андрогены, глюкокортикоиды, которые ингибируют надпочечниковые андрогены, и пероральные антиандрогены, которые действуют на периферическом уровне. Эстрогены в небольших дозах (35–50 мкг), применяемые в качестве пероральных противозачаточных средств, способны значительно снизить секрецию сала. Лечение антиандрогенами проводится после консультации с гинекологом-эндокринологом, при этом может потребоваться оценка гормонального профиля крови (уровня лютеинизирующего гормона, фолликулостимулирующего гормона, эстрадиола, прогестерона, тестостерона, пролактина и дегидроэпиандростерона), ультразвуковое исследование органов малого таза и надпочечников, рентген/томография черепа/мозга.
При средней и тяжелой степени акне лечение гормональными препаратами может проводиться в комплексе с системными ретиноидами или антибиотиками.
Риск развития рецидивов после полноценного курса системных ретиноидов может быть обусловлен синдромом поликистозных (мультифолликулярных) яичников, аденомой гипофиза, опухолью надпочечников или врожденной гиперплазией коры надпочечников, заболеванием щитовидной железы, нарушением толерантности к глюкозе и др. Поэтому необходима консультация гинеколога и эндокринолога.
Другой важной причиной рецидивов является недостаточная суммарная доза изотретиноина или несоблюдение режима приема препарата. Вероятность рецидива при применении низких доз значительно возрастает, что требует более продолжительного курса лечения, чем при использовании стандартных схем [7]. А.L. Zaenglein и соавт. установили, что рецидивы при кумулятивной дозе более 150 мг/кг возникают реже, чем при дозе менее 120 мг/кг [8]. Наименьшая частота рецидивов отмечается при кумулятивной дозе 220 мг/кг [8].
В нашем наблюдении все пациенты получали адекватные дозы в зависимости от степени тяжести кожного процесса и массы тела.
Акнекутан является высокоэффективным и безопасным препаратом для лечения акне средней и тяжелой степени. Побочные эффекты незначительны, легко купируются и не требуют отмены препарата.
Как показал наш опыт, рецидивы при применении изотретиноина возникают при наличии сопутствующих эндокринных заболеваний и гормональных нарушений, поэтому лечение акне в таких случаях необходимо проводить совместно с другими специалистами – гинекологами и эндокринологами. Рецидивы могут быть обусловлены назначением неадекватной суточной и кумулятивной дозы препарата, а также нарушением режима его приема.