ингибиторы кальциневрина что это
Локальная противовоспалительная терапия при атопическом дерматите: современный подход
В XXI в. произошли существенные изменения в изучении атопического дерматита (АД): новейшие методы молекулярной генетики и биологии, междисциплинарный подход, активная научно-исследовательская работа способствовали прогрессу медицины в области патофизиолог
В XXI в. произошли существенные изменения в изучении атопического дерматита (АД): новейшие методы молекулярной генетики и биологии, междисциплинарный подход, активная научно-исследовательская работа способствовали прогрессу медицины в области патофизиологии и терапии этого заболевания.
Наиболее важные достижения, а также соответствующие рекомендации по лечению и профилактике АД были сформулированы экспертами США и Европейского Союза (ЕС) в согласительном документе «Диагностика и лечение атопического дерматита у детей и взрослых» в 2006 г. [1]. В нем определение заболевания звучит коротко: «АД — хроническое воспалительное заболевание кожи, сопровождающееся зудом». Международная группа ученых рекомендует врачам при планировании лечения больных с АД использовать ступенчатый подход (рис.).
Как видно из представленной схемы, на всех стадиях течения АД больным показано основное лечение, которое включает соответствующий уход за кожей (очищение и гидратацию кожи с помощью увлажняющих/смягчающих средств и исключение/снижение влияния провоцирующих факторов), на фоне которого в дальнейшем назначают противовоспалительные препараты.
Уход за кожей основан на применении особых лечебных средств, достаточно широко представленных на современных фармацевтических рынках России. Местная противовоспалительная терапия включает всего лишь две группы лекарств — топические глюкокортикостероиды (ТГКС) и топические ингибиторы кальциневрина (ТИК). При осложнениях АД бактериальной/грибковой/вирусной инфекциями лечение следует продолжить наружными комбинированными или системными препаратами.
Системную терапию (антибиотики, пероральные кортикостероиды, циклоспорин А, азатиоприн, антигистаминные препараты) назначают больным с тяжелой формой АД, имеющим упорно рецидивирующее течение и/или другие сопутствующие заболевания. Взрослым и детям в возрасте старше 12 лет, страдающим тяжелым течением АД, возможно использование фототерапии. В последнее время рассматривается также целесообразность применения аллерген-специфической иммунотерапии в лечении АД.
Наружная (топическая) терапия является патогенетически обоснованной и абсолютно необходимой для каждого пациента с АД. Такая принципиальная важность топической терапии при АД объясняется несколькими факторами. Во-первых, АД — это хронический воспалительный процесс, который протекает в дерме, поэтому главное место в лечении заболевания должна занимать наружная терапия. Во-вторых, при АД крайне важно достичь восстановления и поддержания целостности кожного барьера, нарушение которой является кардинальным признаком АД, влекущей за собой усиление трансэпидермальной потери воды, а также повышение чувствительности кожи к различным ирритантам и аллергенам [3, 4]. Другим важным подходом является воздействие на сухость (ксероз) кожи при АД. Иными словами, наружная терапия — это именно тот вид лечения, который может изменить течение и исход АД.
Рассмотрим некоторые особенности наружной терапии АД, основанной на поэтапном подходе (рис.). Совершенно очевидно, что прежде следует оценить тяжесть течения заболевания.
Оценка степени тяжести АД
АД, как правило, начинается в раннем детском возрасте. Согласно последней классификации, различают не-атопическую и атопическую формы АД (в англоязычной литературе АД обозначают термином «экзема») (2001). По данным зарубежных исследователей, у 30–50% детей с типичной клинической картиной АД не удается подтвердить наличие атопических механизмов; у 15–45% детей описана преходящая (транзиторная) форма АД с низкими сывороточными уровнями IgE, не сопровождающаяся явной сенсибилизацией [2]. Позднее некоторые случаи так называемой eczema infantum спонтанно разрешаются без развития типичного АД. У другой части детей, напротив, заболевание характеризуется формированием сенсибилизации. Недавно Novembre E. с соавторами, исследовав 111 детей в возрасте 2–11 лет, установили, что по данным кожных прик-тестов лишь через 9 лет более чем у половины из них отрицательные кожные пробы стали положительными [3].
К сожалению, не существует потенциальных и объективных маркеров, которые отражали бы степень тяжести и прогрессирования заболевания и которые могли бы быть использованы для оценки эффективности терапии.
В клинической практике для оценки степени тяжести течения АД чаще всего врачи используют такие критерии, как выраженность эритемы, инфильтрации, папулы (индексы IGA — Investigator’s Global Assessment, EASI — Eczema Area Severity Index), еще раньше с этой целью был предложен индекс SCORAD (Scoring Atopic Dermatitis), рекомендованный Европейской академией аллергологии и клинической иммунологии в 1992 г. (данная система учитывает распространенность кожного процесса, интенсивность клинических проявлений и субъективные симптомы).
Вместе с тем, диагноз АД — прежде всего клинический. Основные подходы к наружной терапии при обеих формах АД одинаковы и ставят своей целью увлажнение/смягчение кожи и облегчение зуда. Лечение сухости кожи у больных АД проводят постоянно, тогда как выбор противовоспалительных средств зависит от степени тяжести течения заболевания.
Увлажняющие/смягчающие средства
Тот факт, что сухость (ксероз) и дефекты барьерной функции кожи влияют на течение АД, вполне очевиден. В результате многих исследований установлено, что существует взаимосвязь между зудом, сухостью и воспалением кожи, однако, что первично в этих процессах, точно не ясно. В последнее время дефекты барьерной функции кожи рассматривают как один из важных фенотипических признаков АД, который приводит не только к ксерозу, но и к снижению уровня антимикробных пептидов в коже и повышению трансэпидермальной потери воды. Но одни ученые рассматривают нарушение эпидермального барьера кожи как первичное звено в развитии АД, что способствует облегчению проникновения аллергенов и ирритантов в кожу, впоследствии инициирующих воспалительный ответ и гиперреактивность кожи. Другие, напротив, полагают, что нарушение барьерной функции кожи является вторичным процессом вследствие воспаления, которое развивается в ответ на проникновение аллергенов и ирритантов в кожу [4].
Нарушение барьерной функции кожи имеет место при обоих типах АД — атопическом и неатопическом (при последнем, возможно, оно выражено в большей степени). Доказано также, что при АД кожа сухая даже вне обострения заболевания [1–3]. В связи с этим обосновано применение увлажняющих/смягчающих средств и в те периоды заболевания, когда его симптомы отсутствуют.
На что влияет сухость кожи? Установлено, что при наличии ксероза восприимчивость кожи к экспозиции окружающих аллергенных и неаллергенных раздражителей, ирритантов, а также бактерий и вирусов существенно повышается. Следует учитывать также тесную взаимосвязь цикла «ксероз–зуд». Кроме того, при сухости кожи отмечается усиление системной абсорбции ТГКС, следовательно, и их побочных действий [5].
Из этих данных следует, что эффективное воздействие на сухость, зуд кожи, а также дефекты ее барьерной функции будет способствовать повышению результатов терапии АД. Однако повлиять на такие причины возникновения ксероза, как изменения в роговом слое, нарушения кератинизации, состава баланса внутриклеточных липидов, метаболизма трансэпидермальной воды, изменения рН кожи и т. п. — весьма сложная задача. Кроме того, ксероз и дефекты барьерной функции кожи характеризуются различными биохимическими, физико-химическими и морфологическими изменениями.
Разработан целый ряд специальных лечебных средств ухода за сухой и атопической кожей. В России в настоящее время доступны очищающие и увлажняющие/смягчающие средства различных лечебно-косметических линий: «Топикрем», «Авен», «Мустела Стелатопия», «Урьяж Cu-Zn», «Биодерма», «Дардия», «Виши» и т. п. При их использовании следует учитывать: полноту серии; возраст, с которого можно использовать наружное средство; способность средства создавать защитную пленку на коже, подавлять рост микроорганизмов; восстанавливать липидный слой в коже; противовоспалительный эффект и т. д. Эффективность увлажняющих/смягчающих средств зависит от дозы (их следует применять регулярно и в достаточном количестве), рН кожи, а также от комплаентности больных.
Локобейз Рипеа ® также содержит наночастицы твердого парафина, которые повышают его эффективность, удлиняют время действия и улучшают косметические свойства крема.
Как показывают клинические исследования, за счет восстановления и поддержания нарушенной барьерной функции кожи у пациентов с АД Локобейз Рипеа ® ускоряет разрешение симптомов обострения, повышает эффективность ТГКС и уменьшает потребность в их применении.
Локобейз Рипеа ® не содержит красители, отдушки и консерванты, что минимизирует риск развития аллергических реакций.
Постоянное использование специально разработанных для базового ухода за атопической кожей препаратов, способных эффективно восстанавливать нарушенный кожный барьер, помогает существенно снизить количество обострений и улучшить качество жизни больных с АД.
Следует отметить, что увлажняющие смягчающие средства не обладают противовоспалительным действием и в меньшей степени облегчают симптомы, определяющие тяжесть течения АД. Со своей стороны, противовоспалительные препараты не предназначены для лечения сухости кожи.
Топические противовоспалительные препараты
ТГКС — хорошо изученная группа лекарственных средств. Несмотря на появление нового класса противовоспалительных средств — ТИК, они остаются препаратами первой линии в лечении обострений заболевания.
Как известно, при бронхиальной астме алгоритм применения ингаляционных кортикостероидов разработан и предусматривает регулярное их использование в качестве поддерживающей терапии больным всех степеней тяжести заболевания. При АД подход к назначению ТГКС иной и связан прежде всего с высоким потенциальным риском развития местных нежелательных реакций. При назначении ТГКС следует учитывать тяжесть заболевания, место локализации и возраст больного.
В педиатрической практике широко используют синтетическое производное гидрокортизона — гидрокортизона-17-бутират (Локоид). Эстерификация гидрокортизона боковым звеном масляной кислоты по С17 позволила улучшить абсорбцию препарата через кожу и усилить его метаболизм. В результате гидрокортизона-17-бутират приобрел уникальное соотношение эффективность/безопасность: препарат относится к сильным стероидам (как бетаметазон 17-валерат или триамцинолон), но его местная и системная безопасности сравнимы с таким слабым стероидом, как гидрокортизон.
Препарат может применяться длительно (до 4 недель), разрешен к применению у детей начиная с 6-месячного возраста.
Отсутствие значимого угнетения гипоталамо-гипофизарно-надпочечниковой системы (ГГНС) при использовании гидрокортизона 17-бутирата у здоровых добровольцев и пациентов с АД подтверждено в ряде клинических исследований [7, 8].
Тормозящее влияние экзогенных кортикостероидов на гипофиз-адреналовую функцию вполне ожидаемо. Вместе с тем, как было недавно показано в оригинальном исследовании Haeck I. с соавторами, низкое содержание кортизола у больных с тяжелым течением АД в большей степени может быть связано со степенью тяжести самого заболевания, чем с применением ТГКС [9]. Авторы сравнивали базальный уровень кортизола в крови у 25 больных с тяжелой формой АД (1-я группа), которым требовалась госпитализация, и 28 амбулаторных больных со средней и тяжелой степенью тяжести АД (группа 2): у 80% пациентов 1-й группы уровень кортизола был достоверно ниже уровня больных 2-й группы (p
Д. Ш. Мачарадзе, доктор медицинских наук, профессор
РУДН, Москва
Основные подходы к наружной терапии атопического дерматита у детей
Опубликовано в журнале:
«ПРАКТИКА ПЕДИАТРА»; февраль; 2016; стр.54-59
Ключевые слова: атопический дерматит, наружная терапия, базовая терапия, топические глюкокортикостероиды, топические ингибиторы кальциневрина
Key words: atopic dermatitis, topical treatment, basic treatment, topical corticosteroids, topical calcineurin inhibitors
При назначении терапии следует включать:
Всем больным АтД вне зависимости от тяжести, распространенности, остроты кожного процесса, наличия или отсутствия осложнений назначаются средства базового ухода за кожей. Базовая терапия должна включать рациональный уход за кожей, направленный на восстановление нарушенной функции кожного барьера путем использования смягчающих и увлажняющих средств, средств для очищения кожи, а также выявление и устранение контакта со специфическими и неспецифическими триггерами [5].
Купание ребенка с АтД является необходимой процедурой, позволяющей очистить кожу от нанесенных ранее слоев препаратов, слущивающихся чешуек эпидермиса, корок. Очищение кожи позволяет достигнуть непосредственного контакта лекарственного средства с кожей. Исключением является наличие очагов выраженного мокнутия, вторичного инфицирования кожи. В этот период целесообразно воздержаться от принятия ванной, общего душа в течение нескольких дней, для того, чтобы избежать диссеминации инфекции. Далее купание можно проводить ежедневно, соблюдая комфортную для малыша температуру воды. Вода для купания должна быть 35-36 градусов и желательно дехлорированной (отстаивание воды в течение 1-2 часов). Один-два раза в неделю используются не щелочные моющие средства (так называемые синдеты), без использования жестких мочалок. Высушивание кожи проводится промокающими движениями, без травмирующего растирания кожи. После очищения кожи необходимо обработать расчесы, трещины раствором антисептика (фукорцин, зеленка, мирамистин или др.). Это позволяет свести к минимуму риск вторичного инфицирования и возникновения инфекционно-зависимых обострений дерматита, избежать попадания компонентов наружных средств на участки с нарушенной целостностью кожных покровов, ведущее к возникновению неприятных субъективных ощущений в виде жжения и зуда.
Сразу после купания необходимо использование увлажняющих, релипидирующих средств по уходу за кожей. Это позволяет удержать влагу в эпидермисе, исключить пересыхание кожи [6, 7]. Следует избегать нанесения средств косметического ухода за кожей на очаги острого и подострого воспаления. Конкретный препарат и его лекарственная форма подбираются индивидуально на основании предпочтений пациента, индивидуальных особенностей кожи, сезона, климатических условий, а также времени суток.
Общие рекомендации по применению увлажняющих и смягчающих средств согласно федеральным клиническим рекомендациям по лечению атопического дерматита [2]:
Средства с противовоспалительной активностью выбираются в соответствии со стадией воспалительного процесса (табл.) [7,11].
Таблица.
Применение лекарственных форм при различных стадиях атопического дерматита
| Характер воспалительного процесса | Лекарственная форма |
Острое воспаление с мокнутием (фото 1, 2)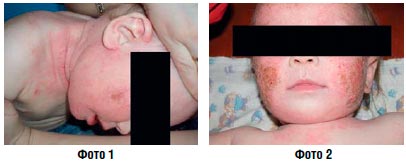 | Примочка Аэрозоль Лосьон Раствор |
Острое воспаление без мокнутия (фото 3)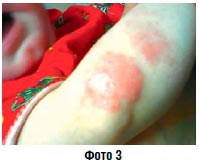 | Водные болтушки Крем Липокрем Паста Аэрозоль |
Подострое воспаление (фото 4, 5)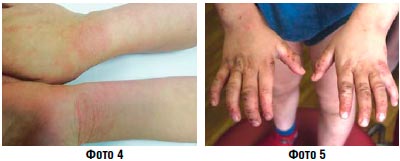 | Крем Липокрем Паста |
Хроническое воспаление (фото 6)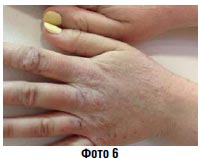 | Мазь Паста Компресс |
Количество топического препарата для наружного применения измеряется согласно правила «длины кончика пальца» (FTU, FingerTipUnit), при этом одна 1 FTU соответствует столбику мази диаметром 5 мм и длиной, равной дистальной фаланге указательного пальца, что соответствует массе около 0,5 г. Этой дозы топического средства достаточно для нанесения на кожу двух ладоней взрослого человека, что составляет около 2% всей площади поверхности тела. Наружные противовоспалительные лекарственные средства необходимо наносить на увлажненную кожу, непосредственно на очаги поражения кожи. Их применение прекращают при разрешении процесса и переходят на базовую терапию. В последнее время рекомендуют метод проактивного лечения: длительное использование малых доз топических противовоспалительных препаратов на пораженные участки кожи в сочетании с применением эмолиентов на весь кожный покров и регулярное посещение дерматолога для оценки состояния кожного процесса [2,12]. Эффективность наружной терапии зависит от трех основных принципов: достаточная сила препарата, достаточная доза и правильное нанесение. При атопическом дерматите с противовоспалительной целью используются топические глюкокортикостероиды, топические ингибиторы кальциневрина, активированный пиритоин цинка. Также возможно использование экстемпоральных мазей, паст, примочек, имеющих в своем составе салициловую кислоту, вазелин, вазелиновое масло, метилурацил, ланолин, нафталан, ихтиол, дерматол, цинк, крахмал, висмут, тальк, борную кислоту, йод, масло оливковое, они обладают комплексным противовоспалительным, кератолитическим, кератопластическим, дезинфицирующим, высушивающим действием.
На сегодняшний день основой местной терапии при обострениях АтД являются топические глюкокортикостероиды (ТГКС). Выбор ТГКС определяется тяжестью течения и обострения. Согласно Европейской классификации (Miller J., Munro D., 1980), выделяют четыре класса данных препаратов в зависимости от их активности. Основные глюкокортикостероидные препараты, рекомендуемые для лечения АтД у детей: гидрокортизон, флутиказона пропионат, мометазона фуроат, гидрокортизона бутират, метилпреднизолона ацепонат. Наружные глюкокортикостероидные препараты наносят на пораженные участки кожи от 1 до 3 раз в сутки, в зависимости от выбранного препарата и тяжести воспалительного процесса. Не рекомендуется разведение официнальных топических препаратов индифферентными мазями, так как такое разведение изменяет концентрацию действующего вещества, но не снижает частоту появления побочных эффектов. Необходимо избегать использования ТГКС высокой активности на кожу лица, область гениталий и интертригинозные участки. Для этих областей обычно рекомендуются ТГКС с минимальным атрофогенным эффектом (мометазона фуроат, метилпреднизолона ацепонат, гидрокортизона-17-бутират). Во избежание резкого обострения заболевания дозу ТГКС следует снижать постепенно. Это возможно путем перехода к ТГКС средствам меньшей степени активности с сохранением ежедневного использования или путем продолжения использования сильного ТГКС, но со снижением частоты аппликаций (интермиттирующий режим) [2, 13]. В ряде клинических исследований было показано, что использование топических ТГКС совместно со смягчающими/увлажняющими средствами позволяет уменьшить курсовую дозу ТГКС [14].
При наличии или подозрении на инфекционное осложнение показано назначение ТГКС, комбинированных с антибиотиками и противогрибковыми средствами (фото 2, 5). Следует учитывать. Что многие комбинированные препараты содержат высокоактивный бетаметазона дипропионат, применение которого у детей нежелательно.
Группа топических ингибиторов кальциневрина (ТИК) включает такролимус и пимекролимус. Фармакологическое действие ТИК обусловлено ингибированием кальциневрина и дальнейшего выделения Т-лимфоцитами и тучными клетками воспалительных цитокинов и медиаторов.
Общие рекомендации по применению ТИК [13]:
Вакцинацию необходимо провести до начала применения мази или спустя 14 дней после последнего использования мази такролимус. В случае применения живой аттенуированной вакцины этот период должен быть увеличен до 28 дней.
Пимекролимус 1%-й крем показан при атопическом дерматите легкого и среднетяжелого течения и может применяться у детей старше 3 месяцев. Однако в ряде стран Европы, США и Канаде пимекролимус разрешен к применению у детей старше 3 лет. Препарат обладает выраженным действием на большинство штаммов Malazessia, что может быть полезно в случаях сенсибилизации к этому грибу [3]. В 2013 году рядом авторов предложен новый алгоритм терапии атопического дерматита легкой и средней тяжести с применением 1%-го крема пимекролимус [13]. При длительно существующем АтД легкой степени тяжести препарат используется дважды в день при появлении первых признаков обострения. Острый АтД легкой и средней тяжести: на протяжении 3-4 дней использование ТКС, с дальнейшим назначением пимекролимуса дважды в день на все пораженные участки до исчезновения симптомов. Предложено проведение поддерживающей терапии длительностью до 3 месяцев 1 раз в день или реже, по усмотрению лечащего врача, на ранее пораженных участках кожи для предотвращения обострений заболевания.
Активированный пиритион цинка (аэрозоль 0,2%, крем 0,2% и шампунь 1%) является нестероидным препаратом, обладающим широким спектром фармакологических эффектов. Может применяться у детей от 1 года, допускается использование на всех участках тела без ограничений по площади. Препарат снижает колонизацию кожи Malassezia furfur, другими грибами, а также S. aureus, участвующими в патогенезе атопического дерматита. Его применение сопровождается уменьшением выраженности кожного зуда, уменьшением степени тяжести и активности кожного процесса, снижением потребности в использовании топических и антигистаминных препаратов. Крем наносят 2 раза в сутки, возможно применение под окклюзионную повязку. Аэрозоль используют в случаях выраженного мокнутия, распыляют с расстояния 15 см 2-3 раза в сутки [2].
Таким образом, современный интегральный подход к терапии АтД включает ступенчатое использование ТГКС, ТИК или других противовоспалительных средств, постоянное использование базовой терапии эмолиентами, бережное очищение кожи, своевременное назначение наружных антисептиков, антибактериальных, противогрибковых препаратов.
Ингибиторы кальциневрина что это
ФГОУ Институт повышения квалификации Федерального медико-биологического агентства РФ, Москва
ФГБУН «Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова» РАН, Москва, Россия, 117997
ООО «Клиники Чайка», 123317, Москва, Российская Федерация
Институт биоорганической химии им. М.М. Шемякина и Ю.А. Овчинникова РАН, Москва, 117997, Российская Федерация
Поддерживающая терапия при атопическом дерматите у взрослых и детей
Журнал: Клиническая дерматология и венерология. 2017;16(4): 14-20
Матушевская Е. В., Коцарева О. Д., Матушевская Ю. И., Свирщевская Е. В. Поддерживающая терапия при атопическом дерматите у взрослых и детей. Клиническая дерматология и венерология. 2017;16(4):14-20.
Matushevskaia E V, Kotsareva O D, Matushevskaia Iu I, Svirshchevskaia E V. Supportive therapy for atopic dermatitis in children and adults. Klinicheskaya Dermatologiya i Venerologiya. 2017;16(4):14-20.
https://doi.org/10.17116/klinderma201716414-20
ФГОУ Институт повышения квалификации Федерального медико-биологического агентства РФ, Москва
В обзоре приведены данные зарубежных и отечественных клинических исследований по изучению эффективности и безопасности топических ингибиторов кальциневрина (ТИК) в лечении атопического дерматита. Представлены основные механизмы действия ТИК и их влияние на барьерные функции кожи. Показаны преимущества одного из препаратов группы ТИК — такролимуса по эффективности, безопасности и возможности включения в поддерживающую терапию по сравнению с другими наружными противовоспалительными лекарственными средствами. Гидрофильная лекарственная форма и фармакоэкономический показатель, повышающие комплаентность лечению, позволяют рассматривать новый препарат как оптимальное топическое средство для лечения среднетяжелых и тяжелых форм атопического дерматита.
ФГОУ Институт повышения квалификации Федерального медико-биологического агентства РФ, Москва
ФГБУН «Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова» РАН, Москва, Россия, 117997
ООО «Клиники Чайка», 123317, Москва, Российская Федерация
Институт биоорганической химии им. М.М. Шемякина и Ю.А. Овчинникова РАН, Москва, 117997, Российская Федерация
В последнее время дерматологи выделяют ряд отличающихся по патогенезу и клиническим проявлениям заболеваний кожи, при которых объединяющим признаком служит принципиальное участие клеток иммунной системы в патогенезе. Атопический дерматит (АтД) — один из воспалительных дерматозов, для лечения которого более 60 лет применяют топические глюкокортикостероиды (ТГКС), оказывающие противовоспалительное, противоаллергическое, антиэкссудативное и противозудное действие. В настоящее время ТГКС по-прежнему остаются препаратами «первой линии» терапии АтД. Но в связи с тем, что АтД характеризуется хроническим рецидивирующим течением, а при длительном применении ТГКС могут вызывать ряд побочных действий, актуальным было создание новых эффективных, но более безопасных средств для местной длительной поддерживающей терапии АтД.
Результаты многочисленных клинических исследований, в ходе которых доказана высокая эффективность и безопасный профиль действия, позволяют рекомендовать для терапии таких заболеваний топические ингибиторы кальциневрина (ТИК).
Основная область применения ТИК в дерматологии — это наружное лечение АтД.
АтД является хроническим рецидивирующим воспалительным заболеванием кожи, сопровождающимся зудом. Наиболее часто встречается у детей. АтД часто ассоциирован с повышением сывороточного IgE и наличием в клиническом или семейном анамнезе гиперчувствительности I типа, аллергического ринита и астмы. В патогенезе АтД выявлена роль генетических факторов и влияния окружающей среды.
Механизмы действия препаратов
Препараты групп ТГКС и ТИК различаются по механизмам действия. Несомненно, что стероидные средства более мощные, чем ингибиторы кальциневрина. Основным противовоспалительным действием ТИК считается специфичное связывание с цитозольным рецептором макрофилином-12 Т-лимфоцитов и подавление действия кальцийзависимой фосфатазы кальциневрина в Т-лимфоцитах. ТГКС не только подавляют активацию Т-лимфоцитов, но и оказывают прямое действие на все другие типы клеток (тканевые макрофаги, кератиноциты, фибробласты), что снижает выброс аларминов и приток новых клеток в место воспаления. Поскольку в воспалении определяющим является суммарное количество активированных клеток, то их одновременное подавление на стадии обострения является предпочтительным. Однако, с учетом побочных эффектов такого тотального действия ТГКС, использование ТИК совместно с ТГКС на участках, склонных к атрофии (лицо, аногенитальная область, складки кожи), значительно улучшает профиль безопасности топической терапии.
В настоящий момент имеются ограниченные данные, показывающие, что ингибиторы кальциневрина не только подавляют активацию Т-лимфоцитов, но и оказывают влияние на кератиноциты. Кальций является триггером переключения пролиферации и дифференцировки кератиноцитов, в котором принимает непосредственное участие кальций/кальмодулинзависимая фосфатаза. Показано, что обработка кератиноцитов мыши циклоспорином, А подавляла экспрессию дифференцировочных маркеров [9]. Соответственно, основное действие ТИК при терапии АтД может быть связано больше с репарацией кожного барьера, чем с действием на Т-лимфоциты.
Результаты клинических исследований в значительной мере подтверждают данное предположение. Так, сравнение противовоспалительного эффекта ТИК и ТГКС на иммунные клетки проведено J. Jensen и соавт. [10]. Больных лечили бетаметазона дипропионатом или пимекролимусом, после лечения проводили биопсию в поврежденном и здоровом участках, выделяли РНК и проводили анализ экспрессии различных генов. Терапия ТГКС приводила к значительному снижению мРНК генов, кодирующих воспалительные цитокины, хемокины, сериновые протеазы, маркеры активации дендритных клеток, Т-клеток, ферментов, участвующих в синтезе липидов, богатых пролином белков, участвующих в связывании церамида. В отличие от ТГКС, пимекролимус почти не снижал экспрессию этих генов. С другой стороны, ТГКС и пимекролимус восстанавливали экспрессию филаггрина и лорикрина, участвующих в формировании верхнего слоя эпидермиса.
Основной курс терапии, основанный на использовании увлажняющих кремов, ТГКС или ТИК, приводит к репарации кожного барьера, что в свою очередь повышает резистентность к патогенам, снижает обсемененность кожи стафилококком, защищает от нормальной флоры кожи. В ряде исследований [11—13] показано, что снижение экспрессии факторов, манифестирующих повреждение кожного барьера в процессе воспалительной реакции, в ответ на терапию ТГКС и ТИК приводит к разрыву обратной связи между барьером и иммунной системой, что ведет к постепенной репарации кожи и восстановлению ее естественной бактерицидности.
Комбинированное применение топических глюкокортикостероидов и ингибиторов кальциневрина
Клинические рекомендации рассматривают возможные варианты комбинированного применения ТГКС и ТИК как последовательно, так и сочетанно для наружной терапии АтД [14].
Имеется ряд сравнительных испытаний по эффективности комбинации ТИК и ТГКС, в которых препараты использовались последовательно или параллельно. В исследовании T. Nakahara и соавт. [15] применение в течение 4 нед топического бетаметазона пропионата, а затем такролимуса давало лучший результат в виде регресса лихенизаций и хронических папулезных элементов при АтД, чем ТГКС и смягчающая терапия. Одновременное использование 0,1% мази такролимуса с мазью дексаметазона давали лучший эффект по сравнению с монотерапией такролимусом или при сочетании 0,1% крема клокортолона и 0,1% мази такролимуса [16, 17]. С другой стороны, J. Spergel и соавт. [18] провели 2-недельное исследование сравнительной эффективности терапии 0,05% кремом флутиказона пропионата в сочетании с пимекролимусом и только ТГКС при обострениях АтД. Авторы не выявили преимуществ дополнительного введения пимекролимуса в схему лечения, что может быть связано с использованием короткого курса терапии и менее эффективного, чем такролимус, препарата.
Влияние на барьерные функции кожи
Анализ влияния ТГКС и ТИК на барьерные и иммунные функции кожи важен для понимания возможных побочных эффектов такой терапии. Часто такой анализ проводится на коже здоровых добровольцев с использованием метода «двух рук» (right-left), когда на предплечье или локтевую зону одной руки наносится изучаемый препарат, а на вторую — препарат сравнения или плацебо. Так, нанесение на кожу одной руки добровольцев 0,1% крема бетаметазона валерата в течение 4 нед снижало барьерные функции кожи, уровень нормальных метаболитов кератиноцитов — пирролидон-5-карбоновой и трансуроканиновой кислот [19]. На другую руку наносили 0,1% мазь такролимуса. Такролимус не вызывал снижения метаболизма и несколько усиливал гидратацию кожи. Оба препарата снижали рН кожи и усиливали трипсиноподобную активность ферментов эпидермиса [19].
В исследовании A. Jiráková и соавт. [20] новым методом отражательной конфокальной микроскопии на 45 больных АтД показано, что в результате применения топического такролимуса 2 раза в день в течение 3 мес структура кожи сохранялась на уровне нормы. Эффект пимекролимуса на барьерные функции кожи больных АтД сравнивали также с эффектом триамцинолона ацетонида в исследовании J. Jensen и соавт. [21]. Рандомизированное двойное слепое исследование, проведенное методом «двух рук», включило 15 больных АтД с похожей локализацией зон поражения в локтевой зоне. Авторы оценивали на 1-й, 8-й и 22-й дни терапии индекс тяжести АтД EASI, гидратацию кожи, трансэпидермальную потерю воды, а также морфологическое состояние эпидермиса (структура ламеллярных отростков и липидных слоев, что было сделано методом «punch» биопсии кожи). Триамцинолона ацетонид эффективнее снижал ЕASI, чем пимекролимус. Пимекролимус повышал гидратацию кожи. Методом трансмиссионной электронной микроскопии показано, что в зоне поражения кожи при АтД наблюдается значительное снижение числа ламеллярных тел. Использование ТИК восстанавливало структуру ламеллярных тел. Аналогичные данные по эффекту препаратов группы ТИК на структуру кожи получены группой S. Dähnhardt-Pfeiffer [22]. В открытом исследовании участвовали 20 больных АтД (SCORAD 10—63), использовавших дважды в день в течение 10 дней 0,1% мазь такролимуса или мометазона фуората. Клинический результат оценивался по индексу SCORAD, уровню трансэпидермальной потери воды и толщине липидного слоя. Клинические симптомы разрешались в обеих группах сравнимым образом. По сравнению с ТГКС такролимус эффективнее улучшал гидратацию кожи и липидный слой [22]. Аналогичные данные по протективному эффекту препаратов групп ТИК получены и другими авторами [23].
Препараты группы ТИК за рубежом используются не только в виде мазей и кремов, но также в виде жидкости для ополаскивания полости рта или при ректальном применении, что является одним из вариантов топических препаратов. Эффект такролимуса оценивали в рандомизированном полуслепом открытом исследовании на группе больных с язвенным красным плоским лишаем [24]. Сравнение проводилось с раствором дексаметазона. Оба препарата были равно эффективны начиная с 4-й недели лечения. При сублингвальном использовании препараты ТИК практически не попадают в кровь [25]. При ректальном использовании ТИК регистрировался в крови [25].
Противозудное действие препаратов группы топических ингибиторов кальциневрина
ТИК обладают противозудной активностью на уровне ТГКС. Исследование было проведено на 30 больных узловатой почесухой, которые получали терапию 1% кремом пимекролимуса на одной руке и 0,1% кремом гидрокортизона на второй. Улучшение наблюдали к 10-му дню терапии, при этом эффективность противозудного действия препаратов была сравнимой [26]. По сравнению с плацебо 0,03% мазь такролимуса эффективно снимала зуд ануса у больных АтД, предъявляющих данные жалобы [27]. Противозудное действие препаратов группы ТИК показано и другими исследователями [28].
Варианты терапии топическими ингибиторами кальциневрина
В отдельных отечественных клинических рекомендациях ТИК позиционируются при лечении витилиго, розацеа, себорейного дерматита, локализованной склеродермии [29]. В то же время результаты исследования D. Funaro и соавт. [30] показали большую эффективность 0,05% клобетазола пропионата по сравнению с 0,1% такролимусом для лечения склероатрофического лишая наружных половых органов. В исследовании G. Müller и соавт. [31] такролимус показал эффективность в монотерапии кератоконъюнктивита. В исследовании приняли участие 24 больных тяжелой формой сезонного кератоконъюнктивита, получавших монотерапию такролимусом (0,03%) или комбинацию такролимуса с глазными каплями олопатадина. Результаты лечения показали равную эффективность монотерапии и комбинированной терапии на основе такролимуса [31].
Такролимус показал умеренную эффективность для терапии кожной формы красной волчанки. В исследовании A. Kuhn и соавт. [33] на 30 больных показано, что ограниченная терапия (два пораженных участка) 0,1% мазью такролимуса дважды в день в течение 12 нед снижала отек, эритему, улучшала состояние кожи по сравнению с группой плацебо. Однако эффект наблюдался транзиторный и исчезал на 3-м месяце лечения. Лучше всего на терапию такролимусом отвечали больные с тумидной формой дискоидной красной волчанки.
Такролимус эффективен при витилиго [34]. Поддерживающая терапия (2 раза в неделю) позволила снизить долю повторной депигментации кожи с 40% в контрольной группе до 10% в группе такролимуса.
Эффективность терапии атопического дерматита препаратами топических ингибиторов кальциневрина
В Европе и Америке 1% крем пимекролимуса рекомендован для лечения АтД легкой и средней тяжести у детей старше 2 лет и взрослых [14], в России пимекролимус можно применять у детей в возрасте старше 3 мес [29]. Мазь 0,03% такролимуса разрешена для терапии АтД средней и тяжелой формы у детей от 2 до 17 лет как в Европе, так и в России; 0,1% мазь такролимуса — для терапии больных старше 18 лет [14, 29]. Такролимус применяется для лечения больных со среднетяжелым и тяжелым течением АтД, так как эффективность такролимуса аналогична эффективности сильных ТГКС. Авторы метаанализа (2015 г.) результатов 25 рандомизированных контролируемых клинических исследований, включивших 4186 и 6897 больных, сравнили эффективность ТИК и ТГКС [35, 36]. Результаты работы показали, что ТИК объективно более эффективны, чем плацебо. Такролимус (0,1%) был так же эффективен, как сильные ТГКС, при применении в течение 3 нед и более эффективен, чем при комбинированной терапии 0,1% гидрокортизона бутиратом (на тело) и 1% гидрокортизона ацетатом (на лицо) при терапии в течение 12 нед. В ходе прямого сравнения эффективности 0,03% такролимуса и 0,1% такролимуса однозначно показано преимущество 0,1% такролимуса после 12 нед применения. В то же время пимекролимус был менее эффективен, чем 0,1% бетаметазона валерат при 3-недельном применении. ТИК значительно чаще вызывали ощущение жжения в месте нанесения, чем ТГКС. Частота ассоциированных кожных инфекций была сравнима при использовании любого из ТИК. Еще одно двойное слепое исследование эффективности применения такролимуса в качестве препарата «второй линии» терапии проведено N. Doss и соавт. [37]. Мазь 0,03% такролимуса (n=240) или 0,005% мазь флутиказона (n=239) использовали для терапии детей с АтД в возрасте от 2 до 15 лет, ранее получавших стандартную терапию, но не достигнувших ремиссии. Лечение проводили до разрешения симптомов, но не более 3 нед 2 раза в день. Задачами терапии было разрешение симптомов по EASI, снижение зуда, нормализация сна, улучшение общего состояния, снижение частоты новых эпизодов, безопасность. Результаты наблюдения показали сравнимую эффективность и безопасность препаратов. В группе такролимуса отмечено меньше новых эпизодов на коже (5,5%) по сравнению с группой ТГКС (11,3%). Побочные эффекты были также сравнимы, за исключением чувства жжения в области нанесения такролимуса. Авторы сделали заключение о равной эффективности и безопасности препаратов. Аналогичные данные получены T. Bieber и соавт. [38] в сравнительном исследовании эффективности и безопасности 0,1% мази метилпреднизолона ацепоната (МПА) и 0,03% мази такролимуса у детей с тяжелой и очень тяжелой формой АтД. Эффективность терапии оценивали в терминах «чисто» или «почти чисто», по индексу EASI, уровню снижения зуда, улучшения сна, а также стоимости терапии. В исследовании приняли участие 257 больных АтД. Препараты были равно эффективны по первому критерию; МПА быстрее вызывал эффект по EASI, зуду и улучшению сна. Такролимус вызывал жжение в месте нанесения у части больных. Стоимость лечения МПА была значительно ниже.
Препараты группы ТИК имеют более безопасный по сравнению с ТГКС профиль действия на кожу и эффективны в терапии детского АтД. В контролируемом рандомизированном исследовании M. Rahman и соавт. [39], проведенном на 60 больных АтД в возрасте от 2 до 10 лет, на основе оценки индекса тяжести заболевания (EASI) показана большая эффективность терапии мазью такролимуса (p
