иммунодепрессивное состояние что это такое
Иммунодепрессивное состояние что это такое
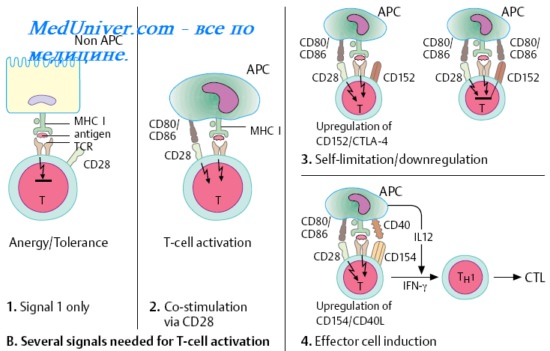
Не следует путать иммунную толерантность и неспецифическое подавление иммунной реактивности, отличающиеся механизмом развития и направленностью. Если толерантность достигается введением толерогена, то иммунодепрессивное состояние носит неспецифическое действие, вовлекая все фазы иммунного ответа и основные популяции иммунокомпетентных клеток. Иммунодепрессивные состояния обычно приводят к нежелательным последствиям; в частности они являются основной причиной развития инфекций, вызываемых условно-патогенной и оппортунистической микрофлорой, а также создают предпосылки для развития болезней злокачественного роста.
Искусственное создание иммунодепрессивного состояния проводят в целях предотвращения отторжения трансплантата и для лечения аутоиммунных заболеваний. Состояние иммунодепрессии могут вызывать различные физические, химические и наследственные факторы.
Врождённые иммунодефициты — как правило редкие генетические заболевания, характеризующиеся изолированным Т- или В-клеточным дефицитом или комбинированным (Т- и В-) расстройством.
Гиперкортицизм (синдром Кушинга) возникает в результате значительного повышения содержания глюкокортикоидоз в крове.
Двусторонняя гиперплазия коры надпочечников (болезнь Иценко-Кушинга) — наиболее частая причина развития синдрома. Эктопический синтез адренокортикотропного гормона опухолями (например, овсяно-клеточная карцинома лёгкого, карцинома поджелудочной железы) вызывает гиперплазию надпочечников и синдром Кушинга.
Ятрогенный синдром Кушинга обычно развивается у больных, длительное время получающих глюкокортикоиды по поводу бронхиальной астмы, артрита и других заболеваний. Ионизирующая радиация повреждает пролиферирующие иммунокомпетентные клетки.
Антилимфоцитарная сыворотка. Иммунодепрессивный эффект основан на феномене антителозависимого цитолиза иммунокомпетентных клеток <феномен впервые установил И.И. Мечников в 1899 г.).
Инфекционные заболевания. Многие вирусные инфекции (например, грипп, корь и др.) вызывают развитие транзиторных иммунодепрессивных состояний, длящихся недели и месяцы. Иммунодепрессивные свойства вирусов создают предпосылки для развития бактериальных суперинфекций, столь характерных для многих ОРВИ. Особую группу составляют так называемые лимфотропные вирусы семейства Retroviridae, вызывающие Т-клеточные иммунодефициты, в дальнейшем приводящие к тотальной иммунодепрессии.
— Вернуться в оглавление раздела «Микробиология.»
Иммунодепрессант: понятие, виды, особенности
Иммуномодулирующие препараты и иммунодепрессанты имеют еще и другое название – иммуносупрессоры. Они используются для замедления работы и размножения клеток иммунной системы. Их нужно принимать тогда, когда нужно остановить иммунные реакции, например, при пересадке органов, аутоиммунных патологиях, костно-мышечной системы и прочих серьезных заболеваниях.
Особенности иммунодепрессантов
Применять иммуносупрессивные средства нужно тогда, когда другие методы лечения испробованы и не достигнуты желаемые результаты, а шансы на положительный исход намного выше рисков от их использования. Из перечня лекарств-иммунодепрессантов практически все имеют иммуносупрессивную активность, оказывают широкое действие. Их применение понижает антибактериальный и противоопухолевый иммунитет, повышает риск появления инфекционных заражений, онкопатологии.
Поскольку заболевания и осложнения состояния здоровья во многих случаях имеют неблагоприятный исход, то противопоказания для лечения иммуносупрессорами несущественны.
Ученые работают над тем, чтобы придать лекарству узкую сферу действия, то есть, чтобы оно действовало на одну конкретную проблему, не затрагивая другие клетки.
С учетом действия препарата на иммунитет человека, их относят к нескольким группам:
Полностью подавляющие иммунную систему;
Для облегчения проявлений аутоиммунных заболеваний;
Противовоспалительное действие – необходимы при нарушении работы мозга.
Есть и другая классификация препаратов:
Также есть несколько поколений этих средств:
Принцип действия
Иммуноспрессоры имеют определенный механизм работы:
«Азатиоприн» и «Метотрексат» препятствуют разделению клеток, приостанавливают образование белковых элементов. Результат происходит медленно и с момента использования будет заметен только через пол года. Эти препараты имеют противоопухолевое действие. Также если принимать его в небольшом количестве, то будет достигнут противовоспалительный результат. Первый препарат содержит меньшее количество токсичных веществ.
«Циклоспорин». Достигается селективное и обратимое воздействие на клеточный иммунный ответ. Повышается продолжительность функционирования аллогенных трансплантатов разных органов.
Глюкокортикоиды. Отличаются сильным иммунодепрессивным эффектом. Останавливают работу макрофагов, лимфоцитов, не позволяя им попадать в кровь. Если принимать в большом количестве, то будет приостановлена работа иммуноглобулина. Отличаются выраженным и быстрым противовоспалительным действием.
Препараты золота, собираясь в зараженных суставных тканях, уменьшают фагоцитарную работу макрофагов, снижают содержание иммуноглобулина в плазме, что приводит к уменьшению его разрушительного воздействия на суставы. Результат будет заметен спустя 6 месяцев.
Даклизумаб. Это очень сильный препарат, от которого достигается более мощный цитостатический эффект.
Клинико-фармакологические принципы
Чтобы достигнуть желаемого результата от применения лекарственных препаратов, нужно учитывать некоторые клинико-фармакологические принципы:
Большие дозы – маленькие дозы;
Маленькое противовоспалительное действие – большое противовоспалительное действие;
Быстрое лечение – продолжительное лечение;
Разное время достижения результата – эффект будет заметен через конкретный промежуток времени (день, неделя, месяц, полгода);
Подавление производства ДНК – подавление разделения РНК.
Особенности применения
При приеме этих лекарственных препаратов нужно учитывать меры предосторожности. Во-первых, их нужно с осторожностью принимать при беременности, грудном вскармливании, проблемах работы почек и печени, инфекционных заражениях, нарушенной функции костного мозга. Их прописывают при следующих заболеваниях и хирургических вмешательствах:
пересадка органов и тканей;
миокард в хронической форме.
Средства с избирательным воздействием не мешают появлению защитных клеток при инфекционных заболеваниях и практически никак не сказываются на противоопухолевом иммунитете.
Разница между иммунодепрессантов и иммуностимуляторов
Иммунитет человека иногда нуждается в коррекции. В таком случае стоит прибегать к помощи особых лекарственных препаратов – иммунодепрессантов и иммуностимуляторов. Стоит понимать разницу между ними:
при продолжительном хроническом заболевании защитная функция организма нарушается и отмечаются аутоиммунные сбои, то есть происходит самоатака клеток. В этом случае необходима коррекция иммуносупрессорами. Их прописывают при разных аллергиях, чрезмерной работе лимфоцитных клеток, после пересадки тканей и органов;
при заражении вредными микроорганизмами запускается производство особых клеток. Если же их количества недостаточно, то человек заболевает. Для повышения выработки защитных клеток стоит использовать иммуностимуляторы. Как правило их нужно принимать при таких серьезных проблемах, как: хронические медленно протекающие заболевания с регулярными рецидивами, которые спровоцированы микробной и вирусной инфекцией.
Как видно, оба этих средства направлены на улучшение иммунитета индивида.
Можно сделать вывод, что эти препараты обладают широким действием и используются при различных заболеваниях и показаны при пересадке тканей и органов. К тому же у них нет побочных реакций, которые могли бы нанести вред здоровью и жизни человека. Вы также можете приобрести препараты для улучшения кровообращения через наш каталог.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Иммунодепрессивные состояния
Полезное
Смотреть что такое «Иммунодепрессивные состояния» в других словарях:
Иммунопатология — I Иммунопатология (иммуно[логия] (Иммунология) + Патология раздел иммунологии, изучающий поражение иммунной системы при различных заболеваниях. Отсутствие одной из нескольких субпопуляций клеток иммунной системы проявляется как врожденное… … Медицинская энциклопедия
Иммунотерапия — I Иммунотерапия (иммун[итет] (Иммунитет) + греч. therapeia лечение) лечение заболеваний с помощью средств целенаправленной активации иммунитета или его подавления. Различают специфические и неспецифические методы И. Специфические методы… … Медицинская энциклопедия
Гингивит — Острый и хронический гингивит Тяжелая форма гингивита д … Википедия
Гидраденит — (устар. Сучье вымя[1], лат. hidradenitis) гнойное воспаление апокриновых потовых желез.[2] Содержание 1 Распространенность 2 … Википедия
Миелит — МКБ 10 G04.04. G05.05. МКБ 9 323323 … Википедия
Иммунокорри́гирующие сре́дства — (иммун[итет] (Иммунитет) + corrigere исправлять, улучшать; синоним: иммуномодулирующие средства, иммуномодуляторы, иммунотропные средства) лекарственные средства, модулирующие (стимулирующие или угнетающие) иммунные реакции организма. Среди И. с … Медицинская энциклопедия
ХИРУРГИЯ — отрасль медицины, задачей которой является лечение заболеваний, деформаций и травм посредством оперативных вмешательств. Хирургические способы лечения применялись еще в доисторические времена, причем имеются свидетельства, что уже тогда хирургия… … Энциклопедия Кольера
ПЕРЕСАДКА ОРГАНОВ — изъятие жизнеспособного органа у одной особи (донора) с перенесением его другой (реципиенту). Если донор и реципиент принадлежат к одному и тому же виду, говорят об аллотрансплантации; если к разным о ксенотрансплантации. В тех случаях, когда… … Энциклопедия Кольера
ТРАНСПЛАНТАЦИЯ — изъятие жизнеспособного органа у одной особи (донора) с перенесением его другой (реципиенту). Если донор и реципиент принадлежат к одному и тому же виду, говорят об аллотрансплантации; если к разным о ксенотрансплантации. В тех случаях, когда… … Энциклопедия Кольера
Клозапин — (Clozapine) Химическое соединение … Википедия
Что такое вторичный иммунодефицит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бычковой Е.Ю., остеопата со стажем в 22 года.
Определение болезни. Причины заболевания
Вторичный иммунодефицит формируется у людей старше 6 лет с исходно нормальным иммунитетом. До этого возраста происходит созревание иммунной системы, особенно полноценных механизмов противоинфекционной защиты, поэтому частое развитие инфекционных заболеваний у детей младше 6 лет не является признаком патологии.
Появление вторичного иммунодефицита обычно связано с воздействием окружающей среды или каких-либо других факторов, но у многих из пациентов можно выявить генетическую предрасположенность к нарушению иммунитета.
Иммунологически здоровый организм способен контролировать и предотвращать развитие инфекций и опухолевых процессов, то есть осуществлять иммунологический контроль внутренней среды.
Когда можно заподозрить вторичный иммунодефицит
Причины развития вторичных иммунодефицитных состояний:
Иммунодефицитные состояния у детей
Развитию иммунодефицита у детей, как и у взрослых, способствуют:
Дисбактериоз у матери является причиной дисбактериоза у ребёнка с последующим замедлением и неполноценным созреванием иммунной системы. Каждый курс антибиотикотерапии может усугубить это состояние.
Проявления иммунодефицита зависят от степени его выраженности, они сопровождаются частыми ОРВИ с инфекционными осложнениями, эпизодами лихорадки, болезненностью, увеличением лимфоузлов, болью в животе, рвотой и нарушением стула.
Симптомы вторичного иммунодефицита
Как проявляется вторичный иммунодефицит
Клинические проявления вторичного иммунодефицита разнообразны. Очень часто на первый план выходят симптомы основного заболевания, которое привело к развитию иммунодефицита. Но основные проявления проблем с иммунитетом, которые указывают на необходимость иммунологического обследования, всё же присутствуют. К ним относятся:
Все хронические инфекции и воспаления протекают на фоне ослабленной иммунной защиты. Поэтому любая хронизация инфекции будет указывать на несостоятельность иммунитета, который не может справиться с болезнью в ходе острого воспалительного процесса.
Патогенез вторичного иммунодефицита
В течение жизни организм подвергается воздействию различных повреждающих факторов, вызывающих вторичный иммунодефицит. Они приводят к угнетению реакций клеточного иммунитета, снижению лейкоцитов и интерферонов — белков иммунной системы, которые вырабатываются лейкоцитами и иммунными клетками и блокируют распространение вируса. Вследствие этого появляются хронические инфекционно-воспалительные процессы, часто рецидивирующие.
Опухоли, возникающие в организме с ослабленной иммунной защитой, истощают иммунитет по мере своего роста, а проводимое лечение (операция, лучевая и химиотерапия) усугубляют возникший иммунодефицит. В этом случае страдает клеточное звено иммунитета:
Классификация и стадии развития вторичного иммунодефицита
По причине возникновения выделяют:
По форме вторичный иммунодефицит может быть:
По продолжительности выделяют два типа вторичного иммунодефицита:
По локализации основного дефекта различают:
Установить локализацию повреждения иммунной системы, основываясь только на симптомах, без лабораторного исследования иммунного статуса, практически невозможно: сходная клиническая картина может наблюдаться при разных типах вторичного дефицита. Например, склонность к вирусным инфекциям может встречаться как при Т-клеточном дефиците, так и при дефиците системы интерферонов.
Осложнения вторичного иммунодефицита
Вторичный иммунодефицит, развивающийся на фоне инфекции и/или воспаления, становится причиной тяжёлых жизнеугрожающих состояний. Без своевременной коррекции иммунитета патологический круг замыкается: течение основной болезни ухудшается.
Наиболее частыми осложнениями вторичного иммунодефицита являются тяжёлые инфекционные заболевания: пневмония, сепсис, абсцесс и флегмона. Их основные проявления: высокая температура и признаки воспаления. При пневмонии наблюдается одышка, кашель и боль в грудной клетке. Сепсис является жизнеугрожающим состоянием, он развивается при попадании в кровь инфекции, сопровождается системной воспалительной реакцией и полиорганной недостаточностью. При абсцессах и флегмоне в организме присутствует очаг гнойного воспаления с выраженной болью, отёком и гиперемией (покраснением).
Диагностика вторичного иммунодефицита
Диагноз «вторичный иммунодефицит» ставится на основании истории болезни, физикального обследования и оценки статуса иммунной системы.
Чтобы назначить эффективных мер по коррекции иммунитета, важно выявить факторы, которые поспособствовали развитию иммунодефицита. Поэтому на консультацию к врачу-иммунологу стоит принести все имеющиеся обследования, а врач будет очень подробно расспрашивать о перенесённых заболеваниях, проведённом лечении, операциях и образе жизни пациента.
Как распознать вторичный иммунодефицит
При подозрении на вторичный иммунодефицит врач назначает анализ крови и иммунограмму — иммунологические тесты, которые оценивают компоненты иммунной системы с точки зрения количества и качества.
Схема обследования различных звеньев иммунной системы (иммунограмма):
На вторичный иммунодефицит могут указывать как пониженные, так и повышенные показатели иммунограммы.
При подозрении на дисбаланс ключевых нутриентов (витаминов, микроэлементов и т. д.) врач-иммунолог может назначить исследования:
В своём заключении врач-иммунолог может указать «вторичный иммунодефицит» как основной или сопутствующий диагноз. Всё зависит от клинической картины.
Лечение вторичного иммунодефицита
Лечение пациента с вторичным иммунодефицитом проводится совместно с врачом, который курирует пациента по поводу основного заболевания. Задача врача-иммунолога заключается в подборе иммунокорригирующей терапии.
«Коррекция иммунитета» в данном случае подразумевает восстановление ослабленной иммунной защиты, исправление дисбаланса её компонентов и иммунных реакций, ослабление патологических иммунных процессов и подавление аутоиммунных реакций.
Лечение вторичного иммунодефицита начинают с определения и устранения его причины. Например, при нарушении иммунитета, вызванном инфекционно-воспалительным процессом, устраняются очаги хронического воспаления.
Если вторичный иммунодефицит возник в результате витаминно-минеральной недостаточности, то назначаются комплексы, содержащие дефицитные компоненты. Например, при истощении лимфоузлов и старении вилочковой железы назначают витамины В6. При обострении или начале аутоиммунных и лимфопролиферативных заболеваний показаны витамины Е.
Важными минералами для иммунной системы являются цинк, йод, литий, медь, кобальт, хром, молибден, селен, марганец и железо. Эти микроэлементы помогают активировать ферменты, которые участвуют в иммунных реакциях. К примеру, цинк предотвращает гибель клеток иммунной системы.
Заместительное лечение вторичного иммунодефицита
Заместительная терапия помогает предотвратить инфекции. Для этого применяют:
Иммунотропное лечение вторичного иммунодефицита
При остром инфекционном воспалении иммуностимуляторы позволяют:
При хроническом инфекционном воспалении иммуномодуляторы:
На степень эффективности иммунокоррекции влияет кратность приёма и стадия заболевания. Срок действия иммуномодуляторов зависит от характера препарата, показателей иммунного статуса и вида заболевания, вызвавшего вторичный иммунодефицит.
Устранение дефицита одного звена иммунитета может привести к компенсации другого звена, так как иммунная система работает по принципу взаимосвязанных модулей.
Может быть назначен как один иммуномодулятор, так и несколько, то есть их комбинация. При комбинированной иммунокоррекцией последовательно или одновременно принимают несколько модуляторов, обладающих разными механизмами действия. Таких иммуномодулирующих препаратов сейчас довольно много.
Показаниями для комбинированной иммунотерапии являются:
ВАЖНО: Самостоятельно назначать себе иммунокорректоры нельзя, так как их бесконтрольное применение может спровоцировать развитие вторичного иммунодефицита.
Прогноз. Профилактика
При вторичном иммунодефиците работа иммунной системы нарушена слабее, чем при первичном. В большинстве случаев выявляется несколько факторов, подавляющих иммунный ответ.
Прогноз определяется тяжестью основного заболевания. Например, если иммунодефицит возник из-за нехватки витаминов или нарушения режима труда и отдыха, он намного легче компенсируется, чем иммунодефицит, спровоцированный опухолевым процессом, сахарным диабетом или ВИЧ-инфекцией.
У детского организма отдельные звенья иммунной системы ещё незрелы: Т-лимфоциты только начинают «знакомиться» с различными инфекциями, поэтому ребёнок часто болеет ОРВИ. Со временем нарабатываются «клетки памяти». По мере взросления формируется широкий «репертуар» Т-лимфоцитов, способных распознавать и быстро запустить иммунный ответ, в связи с чем заболеваемость снижается.
С возрастом иммунная система стареет: в ответ на новые антигены участвует меньше Т-клеток, ухудшается кооперация между клетками иммунной системы, фагоциты хуже поглощают вирусы и мёртвые клетки. Поэтому многие инфекционно-воспалительные заболевания у пожилых людей протекают значительно тяжелее и чаще дают осложнения.
Первичная профилактика вторичного иммунодефицита заключается в ведении здорового образа жизни, сбалансированном питании, отказе от курения. Всё это позволяет предупредить развитие различных заболеваний.
Вторичная профилактика направлена на своевременное лечение инфекционных и общесоматических заболеваний.
Людям с вторичным иммунодефицитом нужны «особые условия», которые не позволят усугубить нарушение иммунитета. Пациентам следует:
Вакцинотерапия
Вакцинация проводится в соответствии с национальным календарем прививок. Перед введением вакцины нужно скомпенсировать иммунодефицит: пропить курс витаминов, минералов и иммуномодуляторов по назначению врача. Это позволит сформировать иммунный ответ на прививку и снизить риск осложнений.
Иммунодепрессивное состояние что это такое
Как уже известно к настоящему времени, COVID-19-ассоциированные заболеваемость и смертность объясняются патологическими изменениями иммунного ответа пациента. Выдвигаются две противоречивые гипотезы: поражение, опосредованное гипервоспалительным «цитокиновым штормом», и нарушение иммунологического защитного механизма хозяина, приводящее к неконтролируемому распространению вируса и поражению органов. Ключевой причиной неспособности объяснить такое противоречие является отсутствие диагностических инструментов для оценки иммунной функции при заражении COVID-19.
Один из наиболее примечательных фактов о текущей эпидемии SARS-CoV-2 (COVID-19) заключается в том, что, несмотря на активно проводимые по всему миру исследования, патофизиологические процессы, играющие решающую роль в заболеваемости и смертности среди пациентов, по-прежнему остаются неизвестными. Господствующая в настоящее время парадигма патологического процесса подразумевает, что слишком сильный иммунный ответ, медиаторами которого выступают чрезмерно продуцируемые провоспалительные цитокины, вызывает обширное поражение легких и состояние склонности к тромбозам. Соответственно, предполагается, что летальный исход наступает в первую очередь по причине воспалительного заболевания легких, нарушения микро- и макроциркуляции и наступающих в конечном итоге дыхательной недостаточности или васкулярной коагулопатии. Это понятие опосредованного «цитокиновым штормом» летального исхода среди пациентов с COVID-19 популяризовано как в неспециализированных печатных изданиях, так и во многих ведущих научных публикациях.
На основании вышеизложенной теории проводятся испытания ряда антицитокиновых и противовоспалительных терапий для лечения COVID-19, включая антитела к интерлейкину-6, антагонисты рецептора интерлейкина-1 и ингибиторы сигнального пути JAK-STAT, но в ходе более ранних клинических исследований существенную эффективность таких подходов доказать не удалось.
В то же время, как это ни парадоксально, вторая, диаметрально противоположная теория COVID-19-индуцированной заболеваемости и смертности заключается в коллапсе системы иммунитета пациента. Такой коллапс иммунитета проявляется в неспособности его сдерживать неконтролируемые репликацию и распространение вируса наряду с прямой цитотоксичностью продуктов иммунного ответа пациента. В качестве обоснования этой прямо противоположной теории приводится наблюдаемая у пациентов прогрессивная и глубокая лимфопения, уровни которой порой достигают таких же значений, как при СПИДе. Результаты многих недавно выполненных исследований свидетельствуют о том, что, в отличие от «цитокинового шторма», который часто считается эпизодическим, лимфопения сохраняется у критически больных пациентов с COVID-19 и коррелирует с повышенной тяжестью вторичных заболеваний и летальным исходом.
Персонализированный подход к оказанию медицинской помощи требует более полного понимания, какой из этих типов реакции системы иммунитета преобладает, поскольку подходящие вмешательства будут различаться кардинальным образом в зависимости от постановки диагноза — наличия у пациента гиперреактивности или же глубокой иммуносупрессии. Например, в настоящее время выполняется клиническое исследование антител против интерлейкина-6, антагонистов рецептора IL-1 и ингибиторов JAK-STAT в качестве терапевтических средств для лечения пациентов с COVID-19 и существует вероятность, что они могут еще больше нарушить способность организма пациента побороть вирус. С другой стороны, методы терапии с использованием иммуностимуляторов, например, ингибиторов иммунных контрольных точек интерлейкина-7, интерферона-γ или GM-CSF, могут усугубить нарушенный и устойчивый воспалительный ответ и привести к усилению степени поражения органов.
Суммируя вышесказанное, становится ясным, что при ведении критически больных пациентов с COVID-19 необходимо ответить на два конкретных и являющихся ключевыми вопроса:
1) каков их первичный иммунный эндотип, т.е. является ли он гиперреактивным или иммуносупрессивным;
2) каким образом это состояние изменяется с течением времени в связи с прогрессированием заболевания или нормализацией состояния.
Более полное понимание иммунного статуса пациента с COVID-19 поможет провести правильную иммунотерапию. Задачей последующих исследований в этой области будет определение, развивается ли при COVID-19 усиленный провоспалительный «цитокиновый шторм» или же состояние, развивающееся при указанной патологии, представляет собой иммуносупрессивный тип иммунного ответа, а также изучение, как изменяется функция иммунной системы по мере прогрессирования заболевания.