ифт костного мозга что это
Ифт костного мозга что это
Диагноз хронического лимфолейкоза (ХЛЛ) может быть установлен при абсолютном количестве лимфоцитов в крови более 5•10 9 /л, наличии в костно-мозговом пунктате не менее 30 % лимфоцитов и иммунологическом подтверждении клонового В-клеточного характера лимфоцитоза.
В подавляющем большинстве случаев предположение о наличии у больного хроническим лимфолейкозом (ХЛЛ) возникает в связи с изменениями картины крови: обнаружение абсолютного и относительного лимфоцитоза. Международное рабочее совещание в 1989 г. установило среди критериев для постановки диагноза хронического лимфолейкоза наличие абсолютного лимфоцитоза в крови не менее 10 • 109/л, однако позже это положение было пересмотрено. В настоящее время для предположения о заболевании ХЛЛ считается достаточным наличие абсолютного лимфоцитоза 5•10 9 /л.
Иногда на протяжении 2—3 лет при числе лейкоцитов, лишь незначительно превышающем норму или даже соответствующем нормальному показателю, наблюдается постепенно нарастающий лимфоцитоз — 50—60—70 %. Эти изменения лейкоцитарной формулы еще не являются оснаванием для постановки диагноза хронического лимфолейкоза без дополнительных исследований: пункции костного мозга и иммунологического исследования крови и костно-мозгового пунктата. Тем не менее такой пациент должен быть под пристальным наблюдением врача: обязательны осмотр и анализы крови каждые 3—4 мес, поскольку, как правило, такие изменения крови являются проявлением начала хронического лимфолейкоза.
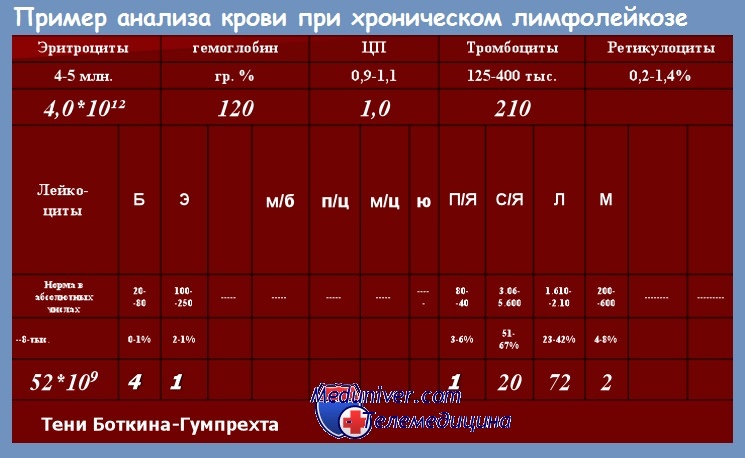
В крови среди ядерных элементов обнаруживается преобладание зрелых лимфоцитов — клеток малого размера, округлых, с плотным ядром и узким ободком светлой или слегка базофильной цитоплазмы. В мазках крови обычно определяется то или иное количество клеток Гумпрехта—Боткина — полуразрушенных размытых ядер лимфоцитов. Их появление связано с повышенной ломкостью мембраны лимфоцитов при хроническом лимфолейкозе.
Количество клеток Гумпрехта — Боткина, как правило, больше у больных с высоким лейкоцитозом. Клетки, или, как их нередко называют, тени Гумпрехта — Боткина, образуются при приготовлении мазка, их наличие и количество не имеют прогностического значения.
Количество лейкоцитов при хроническом лимфолейкозе может быть различным, в большинстве случаев при установлении диагноза хронического лимфолейкоза оно составляет 20—50•10 9 /л, но нередко при первом обращении к врачу уже имеется гиперлейкоцитоз (100—500 • 10 9 /л), свидетельствующий о длительном недиагностированном периоде заболевания. Мы наблюдали больного, у которого при первом обращении к врачу по поводу длительно существующих увеличенных лимфатических узлов количество лейкоцитов оказалось 1200•10 9 /л.
При подсчете лейкоцитарной формулы содержание лимфоцитов обычно составляет 50—70 %, при высоком лейкоцитозе иногда достигает 95—99 %. Наряду со зрелыми лимфоцитами в крови обычно в очень небольшом количестве (как правило, не более 1—3 %) удается обнаружить пролимфоциты — более крупные клетки с отчетливой нуклеолой в ядре. Постепенное увеличение содержания пролимфоцитов в течение болезни, так же как их постоянное присутствие в количестве 10 % и более, является плохим прогностическим признаком.
Е. Matutes и соавт. на большом клиническом материале показали, что выживаемость больных хроническим лимфолейкозом прямо коррелирует с числом циркулирующих пролимфоцитов и значительно снижается уже при числе пролимфоцитов более 5 %.
На основании изучения морфологической картины крови почти 550 больных ХЛЛ Е. Matutes и соавт. выделили примерно 15 % больных с необычной морфологией клеток. Они предложили считать таких больных страдающими атипичным ХЛЛ, отметив два его подтипа: один с повышенным более 10 % количеством пролимфоцитов и второй — с лимфоплазмоцитоидной дифференцировкой лимфоцитов и/или наличием лимфоцитов с расщепленным (cleaved) ядром. Во втором случае одновременно имеются обычные лимфоциты, характерные для хронического лимфолейкоза, и переходные формы — более крупные лимфоциты с выраженной базофилией цитоплазмы или с намечающейся расщелиной ядра.
Течение болезни в этом случае обычно не отличается от характерного для типичного хронического лимфолейкоза, однако нередко при обоих указанных вариантах имеется трисомия хромосомы 12. При обоих подтипах: повышенном количестве пролимфоцитов и лимфоплазмоцитоидной морфологии лимфоцитов — течение болезни у больных с трисомией хромосомы 12 более агрессивное.
Костно-мозговой пунктат при хроническом лимфолейкозе обычно гиперклеточный, инфильтрация лимфоцитами чаще всего имеет диффузный характер, хотя иногда встречаются случаи нодулярной инфильтрации. В большинстве случаев процентное содержание лимфоцитов значительно превышает необходимые для установления диагноза 30 %, нередко достигая 90—95 %.
Лимфоциты в костном мозге морфологически не отличаются от лимфоцитов крови, но обычно имеется 3—5 % пролимфоцитов даже в тех случаях, когда они не обнаруживаются в крови.
При морфологическом исследовании лимфатического узла обнаруживают стирание нормального рисунка и мономорфную инфильтрацию лимфоцитами, морфологически сходными с лимфоцитами крови и костного мозга, иногда имеющими несколько большие размеры. В небольшом количестве встречаются пролимфоциты и клетки, названные параиммунобластами: клетки среднего размера с дисперсным хроматином и круглыми или овальными ядрышками. В селезенке преобладает инфильтрация белой пульпы, хотя красная пульпа обычно тоже оказывается в той или иной степени инфильтрированной малыми лимфоцитами.
Несмотря на характерную картину, результаты морфологического исследования не могут считаться достаточными для установления диагноза хронического лимфолейкоза (ХЛЛ), поскольку аналогичная морфологическая картина крови и костного мозга нередко наблюдается при фолликулярной и мантийно-клеточной лимфомах с поражением костного мозга. Согласно современным критериям, диагноз хронического лимфолейкоза может считаться установленным только после иммунологического исследования, подтверждающего диагноз. Патологические лимфоциты при хроническом лимфолейкозе имеют абсолютно характерный иммунофенотип.
Они экспрессируют антигены CD19, CD5, CD23, отмечается слабая экспрессия на поверхности клеток иммуноглобулинов (экспрессируются IgM, нередко одновременно с IgD) с одной L-цепью, определяется слабая экспрессия антигенов CD20 и CD22, у ряда больных экспрессируется молекула FMC-7. Антиген CD79b, или Igb, являющийся частью В-клеточного рецептора, либо не экспрессируется, либо экспрессируется очень слабо в подавляющем большинстве случаев.
Характерный иммунофенотип опухолевых клеток позволяет отличить В-ХЛЛ от других лимфопролиферативных заболеваний.
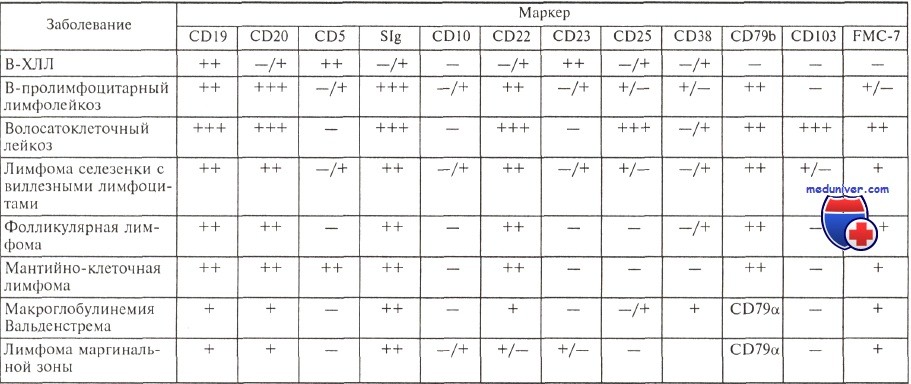
Е. Matutes и соавт. предложили числовую систему, помогающую при дифференциальной диагностике В-ХЛЛ и других лимфопролиферативных заболеваний. По этой системе каждый иммунологический признак, характерный для В-ХЛЛ, расценивается как 1 балл, его противоположное значение — как 0.
Иммунофенотип опухолевых клеток при различных лимфопролиферативных заболеваниях
Иногда возникают трудности в дифференциальной диагностике хронического лимфолейкоза и так называемого монокло-нового В-лимфоцитоза неопределенного значения (MLUS — monoclonal lymphocytosis of undetermined significance), названного так по аналогии с моноклоновыми гаммапатиями неопределенного значения (MGUS). Термин был впервые введен еще в конце 80-х годов прошлого века для отличия непрогрессирующего моноклонового лимфоцитоза без признаков ХЛЛ от индолентного ХЛЛ с признаками заболевания. В настоящее время чаще употребляется термин CLUS (clonal lymphocytosis of undetermined significance).
При CLUS обычно на протяжении многих лет сохраняются умеренный и стабильный лейкоцитоз и лимфоцитоз (меньше необходимых для диагноза ХЛЛ 5•10 9 /л), нормальные показатели эритро- и тромбоцитопоэза, отсутствует увеличение лимфатических узлов и селезенки.
В наблюдениях С. Wang и соавт. клиническая картина и лабораторные показатели при CLUS оставались неизменными на протяжении 3—10 лет. Клоновая природа лимфоцитоза была подтверждена рестрикцией L-цепи экспрессируемых на поверхности лимфоцитов иммуноглобулинов. Никаких хромосомных аберраций на протяжении всего времени наблюдения выявлено не было. У всех пациентов исследование иммунофенотипа на протяжении всего времени наблюдения обнаруживало экспрессию лимфоцитами антигенов CD19, CD20 и слабую экспрессию поверхностных иммуноглобулинов, однако неизменно выявляло отсутствие экспрессии CD5 и CD23. Таким образом, данные наблюдения не отвечают всем признакам В-ХЛЛ. Однако в большинстве случаев иммунофенотип при CLUS не отличается от типичного иммунофенотипа В-ХЛЛ. A. Rowstron на основании анализа нескольких сотен наблюдений раннего стабильного хронического лимфолейкоза и сравнения их с CLUS указывает, что частота прогрессирования в этих случаях одинакова и не превышает 10 %.
Известно, что истинный хронический лимфолейкоз, имеющий все необходимые для установления диагноза черты, также может годами не проявлять признаков прогрессирования. В подобных случаях имеется характерный для данного заболевания иммунофенотип, а при длительном наблюдении (в одном нашем наблюдении спустя 22 года со времени постановки диагноза) во многих случаях появляются черты прогрессирующего хронического лимфолейкоза. В других наблюдениях клиническая картина сохраняется неизменной на протяжении всей жизни больного.
Мы наблюдали больную в течение 29 лет, которая не получала никакого лечения, поскольку все это время у нее была стабильная гематологическая и клиническая картина: отсутствие увеличенных лимфатических узлов и селезенки, количество лейкоцитов 15—20•10 9 /л, лимфоцитов 65—70 %. Это наблюдение похоже на наблюдения Т. Han и соавт., описавших 10 больных с лейкоцитозом более 10 • 109/л и моноклоновым В-клеточным лимфоцитозом, у которых в течение 6—24 лет не было признаков прогрессирования и которые не нуждались в терапии.
Возможно, эти наблюдения являются отражением возрастного изменения В-клеточного репертуара. Почти 10 лет назад было обнаружено, что у мышей с возрастом постепенно суживается разнообразие клонов В-клеток (В-клеточный репертуар) и одновременно происходит увеличение размеров (амплификация) отдельных клонов. N. Chiorazzi и М. Ferrarini указывают, что у здоровых людей старше 50 лет наличие таких клонов В-лимфоцитов является обычным. Возможно, отдельные клоны, возникшие под влиянием длительной стимуляции определенным антигеном, могут приобретать значительные размеры и определяться при рутинном иммунологическом исследовании.
Обнаруженная недавно в половине исследованных методом FISH случаев CLUS делеция 13ql4, являющаяся самой частой генетической аберрацией при ХЛЛ, подтверждает мнение о том, что CLUS следует расценивать как раннюю стадию хронического лимфолейкоза доброкачественного течения. В то же время P. Ghia и соавт., обследовав 500 здоровых людей старше 65 лет, обнаружили у части из них клоны клеток с иммунофенотипом, характерным для различных лимфопролиферативных заболеваний, иногда у одного и того же больного. Авторы полагают, что это, скорее всего, является не ранней стадией болезни, а отражением постепенно суживающегося с возрастом В-клеточного репертуара.
В 1982 г. описан постоянный поликлоновый В-лимфоцитоз у курящих женщин средних лет. У некоторых из них были частые респираторные заболевания. Это редкий феномен, и со времени первой публикации появилось не более 90 подобных описаний. Исследования с помощью ПЦР показали, что во всех изученных случаях имеется реаранжировка BCL-2/IgH, которая, однако, не всегда сопровождалась повышенной экспрессией BCL-2.
У некоторых курящих женщин с поликлоновым В-лимфоцитозом обнаружены незначительное увеличение размеров селезенки и поликлоновая гамма-патия, которые, как и лимфоцитоз, иногда исчезали после прекращения курения.
Несколько случаев поликлонового В-лимфоцитоза описаны у некурящих. С помощью ПЦР у некоторых пациентов в крови был обнаружен вирус Эпштейна—Барр. Неясно, играет ли этот вирус роль в развитии синдрома поликлонового В-лимфоцитоза.
Очевидно, в настоящее время подобные случаи не являются трудными для дифференциальной диагностики с хроническим лимфолейкозом (ХЛЛ), поскольку поликлоновый характер лимфоцитоза обнаруживается при иммунофенотипировании. Трудности для трактовки представляет описанный недавно случай поликлонового В-клеточного лимфоцитоза с комплексными хромосомными аберрациями — трисомией хромосом 3, 15 и 18, инверсией хромосомы 18, t(13;14) в отдельных клетках у длительно курящей женщины. Гематологическая картина остается стабильной на протяжении нескольких лет наблюдения, но отмечаются часто повторяющиеся инфекции верхних дыхательных путей. Необходимо длительное наблюдение для выяснения вопроса о том, не являются ли имеющиеся хромосомные аберрации отражением начала лимфопролиферативного заболевания.
При некоторых хронических инфекциях (туберкулез, сифилис), иногда при неинфекционных заболеваниях (тиреотоксикоз, болезнь Аддисона) наблюдается постоянный Т-клеточный лимфоцитоз, чаще всего при нормальном количестве лейкоцитов. Его также нетрудно дифференцировать от хронического лимфолейкоза (ХЛЛ) на основании данных иммунологического исследования.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Ифт костного мозга что это
Прогресс в развитии современной гематологии в определенной степени связаны с увеличением аналитических возможностей лабораторной диагностики. Метод иммунофенотипирования (ИФТ) широко применяется для диагностики заболеваний, оценки эффективности терапии и выявления минимальной остаточной болезни, количественного определения гемопоэтических стволовых клеток периферической и пуповинной крови, костного мозга, при мониторировании реакции трансплантата против хозяина. В связи с накоплением значительного объема информации по строению и функции маркерных молекул лейкоцитов разработана и постоянно пополняется специализированная номенклатура CD, включающая 350 маркеров CD [3].
При дифференциальной диагностике парапротеинемий часто встречаются сходные клинико-лабораторные данные, наблюдающиеся при многих патологических процессах и зачастую бывает сложно своевременно поставить диагноз. В программу обследования необходимо включать довольно разнообразные тесты и изучать их в динамике течения опухолевого процесса.
Целесообразно поводить обследование больных с использованием всех доступных методов, включая иммунофенотипирование плазматических клеток костного мозга.
По данным R-Garcia-Sanz (1999), проанализировавшим 26 больных с первичным ПКЛ, для больных (в отличие от ММ) были характерны III стадия заболевания, экстрамедуллярные очаги, высокий уровень ЛДГ. Обнаружена также высокая пролиферативная активность опухолевых клеток в периферической крови и костном мозге. При ИФТ опухолевые клетки больных как ММ, так и ПКЛ экспрессировали СD38+ СD 138+ СD 2+ СD 3+ СD16+ СD10+ СD13+ СD15+. Отличие ПКЛ от ММ было только в экспрессии антигенов СD 56+, СD9+, HLA-DR, СD117+ СD20+. Характерной особенностью лейкемических плазматических клеток периферической крови и костного мозга при ПКЛ является частая утрата маркера СD 56+ [6].
Клинико-лабораторные особенности пациентов с ПКЛ в Тюменском гематологическом центре с 2008 г.
Иммунофенотипирование в диагностике острых лейкозов
Санкт-Петербургский Медицинский Университет им. акад. И.П.Павлова, Санкт-Петербург, Российская Федерация
Резюме
На сегодняшний день иммунофенотипирование онкогематологических заболеваний представляет собой одно из наиболее востребованных клинических приложений проточной цитометрии. Рассмотрены основные критерии выявления лейкозных бластов, верификации их линейной принадлежности и определения аберрантности фенотипа с использованием преимуществ многоцветного анализа.
Резюме
На сегодняшний день иммунофенотипирование онкогематологических заболеваний представляет собой одно из наиболее востребованных клинических приложений проточной цитометрии. Рассмотрены основные критерии выявления лейкозных бластов, верификации их линейной принадлежности и определения аберрантности фенотипа с использованием преимуществ многоцветного анализа.
Лабораторная диагностика ОЛ начинается с выявления в периферической крови, костном мозге, и, реже, спинномозговой жидкости бластных клеток, которые идентифицируются методом световой микроскопии. Подробное морфологическое и цитохимическое описание разных типов бластов в настоящее время обязательно присутствует в каждом руководстве по онкогематологии, но фактически требует от патолога значительного опыта и далеко не всегда дает однозначную оценку бластов. Детально разработанная в конце 70-х годов (1976-1980) гематологами и патологами Франции, США и Великобритании ФАБ-классификация (France-America-Britain) разделила острые лейкозы на лимфобластные и нелимфобластные (миелобластные). При оценке бластов миелоидного происхождения морфологические критерии ФАБ-классификации достаточно информативны, однако, для верификации бластов лимфоидного происхождения их применение признано нецелесообразным (ВОЗ, 2000). В настоящее время основой для диагностики гемобластозов (заболеваний, связанных с пролиферацией гемопоэтических клеток предшественников и клеток крови на разных стадиях дифференцировки) служит классификация ВОЗ 2000г.
Годы активного внедрения ФАБ-классификации в клиническую онокогематологию одновременно стали временем объединения фундаментальных открытий в биологии и биотехнологии, временем накопления знаний о путях дифференцировки клеток костного мозга, о роли Т- и В-лимфоцитов в развитии онкогематологических заболеваний, об особенностях лейкозных клеток. Поистине революционное значение для диагностической иммунологии и гематологии оказала разработка методов получения моноклональных антител, что было подтверждено в 1984 присуждением Нобелевской премии Kohler и Milstein вместе с Jerne за вклад в развитие теоретической иммунологии и биотехнологии. Создание гибридом вобрало в себя основные положения теории антителообразования: клональный принцип строения лимфоидной ткани, моноспецифичность антител, функционирование генов иммуноглобулинов только в лимфоидных клетках и их производных. Применение моноклональных антител в диагностике позволило охарактеризовать структуру и функцию линейно-ассоциированных и дифференцировочных антигенов, а затем и антигенов, экспрессия которых обусловлена активацией и пролиферативной активностью клеток. В 80-е годы прошлого века острый лейкоз рассматривался как блок дифференцировки клетки на определенной стадии ее развития, поэтому и варианты лимфобластных лейкозов получали свое название соответственно той стадии дифференцировки, антигены которой выявлялись на бластах в первую очередь. Дифференцировочный статус гемопоэтических новообразований определялся как «замороженная» стадия онтогенеза, т.е. аксиомой было сохранение опухолью направления и стадии дифференцировки клетки-предшественницы. Догмой онкогематологии было представление о том, что опухоли гемопоэтической системы представляют собой наиболее яркий пример сохранения дифференцировочного/антигенного статуса нормальных клеток при их опухолевой трансформации. И это рассматривалось как исключение из правила классической онкологии, согласно которому нарушение гистотипа с более или менее выраженной утратой тканевой специфичности является характерным признаком эпителиальной опухоли.
В настоящее время сохранение дифференцировочного статуса при всех формах гемобластозов расценивается как свидетельство существования различных форм взаимодействия трансформации и дифференцировки. Стало очевидно, что клональность происхождения не означает неизменности характеристик лейкозных бластов в течение болезни: антигенный дрейф, или изменение антигенной экспрессии в течение заболевания или в ответ на адекватную терапию является одним из отражений опухолевой прогрессии. Сохранение гемобластозами дифференцировочного статуса клетки-предшественницы в основном связано с тем, что опухолевая трансформация гемопоэтических клеток включает (запускает) механизмы нормальной дифференцировки и опирается на них. Эти механизмы участвуют как в самом процессе трансформации (ошибки физиологических рекомбинаций), так и в поддержании опухолевого фенотипа (активация протоонкогенов, блокировка созревания и т. д.). Одной из характеристик лейкозной клетки является ее способность избегать уничтожения либо за счет увеличения пролиферативного потенциала, либо за счет изменения продолжительности жизни. Клетка теряет способность воспринимать физиологические сигналы о необходимости прекращения функции, о необходимости к переходу в другое состояние для обеспечения поддержания нормального гомеостаза организма. Говоря иными словами, клетка учится избегать старения, увядания, т.е. всего того, что приводит ее к смерти. Необычно высокая экспрессия белков гиперсемейства генов, контролирующих клеточную гибель, вызывает изменение срока жизни клетки, популяции и влияет на эффективность отдельных видов химиотерапии. Баланс активности проапоптотических и антиапоптотических генов является в какой-то мере определяющим в формировании клинической картины лейкоза и особенностей его прогрессии. Тесное взаимодействие трансформации и дифференцировки является, по-видимому, уникальной особенностью гемобластозов и создает возможность их «дифференцировочной» терапии. Широкое, быстро превращающееся в рутинное использование моноклональных гуманизированных антител для терапии онкогематологических заболеваний подтверждает это положение. Моноклональные антитела, специфичные к антигенам опухолевых клеток-мишеней, становятся препаратами выбора для отдельных форм лимфопролиферативных заболеваний (Rituximab, Genistein, Campath и другие).
Иммунодиагностика гемобластозов основана на сопоставлении морфофункциональных характеристик лейкозных бластов и нормальных/нетрансформированных клеток гемопоэза. Известно, что нормальный процесс дифференцировки клеток в костном мозге и/или тимусе происходит с определенной, достаточно постоянной скоростью, определяемой потребностью организма в кроветворных и иммунокомпетентных клетках. По мере функционального созревания лимфоидных и миелоидных клеток происходит перестройка генов, кодирующих специфические рецепторы клеток, а значит, происходит изменение набора рецепторов для различных факторов роста, дифференцировки и межклеточного взаимодействия. По набору мембранных и цитоплазматических антигенов можно установить линейную принадлежность, стадию зрелости и функциональное состояние клетки. С начала 80-х годов ХХ века, когда развитие моноклональных антител пошло по экспоненте, стало возможным нарастающее по сложности иммунофенотипирование. Затем, качество реагентов и оборудования улучшилось, как следствие, методики стали проще и воспроизводимее. были разработаны программы внешнего контроля качества типирования ОЛ. К настоящему времени ИФТ превратилось в быстрый и полезный способ получения подробной характеристики опухолевых клеток, необходимой для диагностики ОЛ. Сходство между лейкозными и нормальными клетками позволяет установить линейность и стадию созревания патологических клеток, что необходимо для иммунофенотипического диагноза, классификации и прогностической оценки различных типов онкогематологических заболеваний. Фенотипические аберрации, характеризующие лейкозные клетки, позволяют выявлять случаи с максимальной вероятностью специфических генетических поломок, для подтверждения которых необходима молекулярная диагностика.
Для количественного определения популяционного состава лейкоцитов используется способность их рецепторов взаимодействовать со специфическими антителами с образованием стабильных комплексов на поверхностной мембране клетки. Фактически, как это часто бывает в жизни, мы определяем вещи (в данном контексте клетки) по признакам, не имеющим ничего общего с их функциями. Так и молекулы на мембране или внутри клеток, делая доступным и простым их распознавание по признаку антигенности, могут выполнять функции, отличные от иммунных.
На основании классической реакции антиген-антитело разработано довольно много способов количественного учета клеток, часть из которых имеет сугубо историческое значение, другие применяются в основном для научных исследований. Для практических целей максимально адаптированы и дают наиболее воспроизводимые результаты иммуноцитохимия (световая и люминесцентная микроскопия) и проточная цитометрия (рис.1). Однако не только в клинически сложных случаях, но и в повседневной практике микроскопирование все чаще уступает место проточной цитометрии, ставшей основным методом ИФТ в диагностике гемобластозов.
Выявление лейкозных бластов
Выявление лейкозных бластов в периферической крови и/или костном мозге методом проточной цитометрии основано на отличии их фенотипа от фенотипа неизмененных клеток. Нормальные клетки, сохраняющиеся в некотором количестве даже при выраженной опухолевой экспансии, могут использоваться как внутренний стандарт антигенной экспрессии. Именно уровень антигенной экспрессии и физические характеристики определяют местоположение каждой популяции клеток в многомерном пространстве проточной цитометрии.
При работе с бластными популяциями обогащение образца, т.е. отбор определенных, интересующих клеток можно проводить двумя путями:
o сохраняет возможность анализа образца в целом, всех составляющих его популяций;
o дает возможность выбрать любую нужную популяцию и определить ее иммунофенотипический профиль при дальнейшем, более прицельном анализе, не теряя дополнительное время на выделение суспензии мононуклеаров.
При диагностике гематологических заболеваний предпочтительно использовать селективное гейтирование, в частности, по панлейкоцитарному маркеру CD45. Гейтирование по гистограмме SSC/CD45 является удобным средством идентификации патологических клеток, так как обычно бласты занимают (на гистограмме SSC/CD45) такое положение, где располагается очень мало здоровых клеток. Особенно ярко это видно на образцах периферической крови (рис.2). При гейтировании по CD45 следует соблюдать определенную осторожность, так как
? ядросодержащие эритроидные клетки костного мозга, равно как и некоторые лейкозные клетки могут быть отрицательны по этому антигену;
? при Т-клеточных опухолевых процессах интенсивность СD45 очень высока, но для дифференциальной диагностики этот факт имеет ограниченную ценность;
При цитопении неясной этиологии и при отсутствии клеток волосатоклеточного лейкоза (ВКЛ) с классической морфологией использование гистограммы SSC/CD45 может помочь выявить популяцию опухолевых клеток: трансформированные клетки располагаются в обычном месте расположения моноцитов, но средний уровень флюоресценции этих клеток по CD45 выше, чем у нормальных лимфоцитов и даже моноцитов.
Для получения подробной характеристики бластов при лимфобластных лейкозах более специфичным является гейтирование по CD19 или CD7 (соответственно SSC/CD19 и SSC/CD7). Линейно-ассоциированные лимфоидные бласты В- или Т-клеточного происхождения, экспрессирующие соответственно CD19 или CD7, обладают, как и лимфоциты, низким уровнем гранулярности и располагаются в строго определенном пространстве гистограммы. В гистограммах здорового костного мозга это пространство обычно пустует, там не располагаются нетрансформированные клетки (Рис.3). Использование определенного маркера для селективного гейтирования патологической популяции предполагает, что моноклональные антитела к этому маркеру должны быть включены во все пробирки, подготовленные к анализу на проточном цитометре Желательно, чтобы гейтирующий маркер был конъюгирован с флуорохромом для учета по третьему, или, если есть техническая возможность, по четвертому каналу флуоресценции, так как это дает максимальный простор для выбора других маркеров и определения их сочетанной экспрессии внутри патологической популяции.
Однако, даже теоретически, не может быть определен вариант гейтирования, подходящий для всех вариантов злокачественной трансформации гемопоэтических клеток. Поэтому так важно иметь широкий выбор диагностических моноклональных антител для определения фенотипа злокачественных клеток в разных клинических ситуациях. Информация о вариантах гейтирования, применяемых в онкологических центрах всего мира, постоянно публикуется в Интернете в открытом доступе. Необходимо, чтобы накопление опыта селективного гейтирования стало доступно отечественным врачам на родном языке в режиме реального времени (on-line).
При определенных усилиях процессы пробоподготовки (доаналитический этап) и получения данных (собственно аналитический этап) могут быть автоматизированы, что оправдано технически и экономически в крупных гематологических центрах, проводящих в день определение иммунофенотипа патологических клеток у большого количества пациентов (более 20-40 человек). Анализ же полученной информации, установление варианта лейкозной трансформации и соотнесение ее с данными других лабораторных технологий является задачей врача и требует накопления определенного опыта.
Определение количества лейкозных клеток
В большинстве случаев количество бластов указывается в миелограмме, сопровождающей костный мозг, направленный на ИФТ. Однако, на практике, материал стернальной пункции одновременно направляется морфологу для получения детальной миелограммы и иммунологу на иммунофенотипирование для определения варианта лейкоза, т.е. клеточность образца неизвестна. Первым следствием этого является необходимость вносить специфические антитела в некотором избытке, а не из расчета на количество клеток. Затем, для определения уровня бластоза при проточной цитометрии необходимо средствами программного обеспечения отделить собственно клетки от дебриса и от дуплетов клеток (слипшихся клеток), которые могут в разном количестве присутствовать в анализируемом образце. Дуплеты особенно часто наблюдаются при В-лимфопролиферативных заболеваниях и обладают более высокими значениями по светорассеянию и флуоресценции по сравнению с одиночными клетками. Если между временем получения костного мозга (периферической крови) и началом пробоподготовки проходит более двух-четырех часов или были грубо нарушены условия транспортировки, то из анализа должны быть исключены мертвые клетки в связи с их способностью к неспецифическому связыванию антител. В некоторых случаях, при вынужденном длительном хранении образца, в частности, при транспортировке из географически удаленных регионов, селективное гейтирование должно проводится по жизнеспособным клеткам, что может позволить анализировать только функционально сохранные клетки. Для оценки жизнеспососбности клеток анализируемого образца оптимально использование 7AAD (7-аминоактиномицин D), который может быть применен одновременно с антителами, мечеными ФИТЦ и фикоэритрином.
При определении количества лейкозных клеток в костном мозге, надо помнить о возможном разведении образца периферической кровью, что может серьезно влиять на конечный результат определения количества патологических клеток в образце. Характеристика лейкозных клеток
При выявлении в образце неопластических клеток и определении их количества должны быть решены две основные задачи ИФТ гемобластозов:
1) идентификация патологических клеток и
2) иммунофенотипическая характеристика бластов, в том числе
? определение линейной принадлежности бластов и уровня их дифференцировки;
? Определение степени гетерогенности клеток патологической популяции за счет выявления различных патологических клонов или наличия клеток на разных стадиях дифференцировки;
? получение подробной фенотипической характеристики каждой выявленной субпопуляции патологических клеток.
И если первая задача может быть выполнена в течение одного-двух часов, то формулировка диагноза требует иногда гораздо большего времени, особенно при низком уровне бластоза в образце.
Определение линейной принадлежности лейкозных бластов является обязательной частью обследования пациентов с подозрением на гемобластоз. Для этого может быть достаточной оценка экспрессии маркеров скриннинговой панели:
i) линейную принадлежность клеток определяют:
(a) миелоидные маркеры:
МПО, CD13, CD33;
(b) Лимфоидные маркеры:
1. Маркеры Т-лимфоцитов
i. CD2, CD7, cyCD3 и sCD3;
2. Маркеры В-лимфоцитов
i. CD10, CD19, cyCD22 и sCD22.
ii) незрелость клетки характеризуют TdT, CD34, HLA-DR.
Определение линейной коммитированности опухолевых клеток тем проще, чем больше дифферецировочных маркеров выявляется на их мембране. Трудности в определении линейной принадлежности бластов чаще всего связаны с отсутствием экспрессии линейных маркеров на поверхностной мембране клеток и с существованием перекрестной экспрессии линейных антигенов. Поверхностные линейно-ассоциированные маркеры не выявляются при опухолевой трансформации самых ранних клеток-предшествеников гемопоэза или, в отдельных случаях, утрачиваются при опухолевой прогрессии после химиотерапии. При отсутствии экспрессии линейных маркеров на поверхностной мембране клеток необходимо проводить выявление маркеров линейной принадлежности (миелопероксидаза, CD3, CD79a, CD22) в цитоплазме, что требует введения дополнительных шагов в протокол пробоподготовки. Для того, чтобы избежать необходимости последовательного проведения дополнительных окрашиваний, логичнее с самого начала включить в диагностическую панель несколько пробирок для выявления внутриклеточных антигенов. Это требует минимального увеличения времени пробоподготовки за счет фиксации и пермеабилизации, но компенсируется получением абсолютно достоверной информации о линейной принадлежности бластов.
Наиболее специфичным маркером Т-ряда является поверхностный и/или цитоплазматический CD3 и Т-клеточный рецептор (TCR). Предшественники Т-клеток ОЛЛ обычно положительны по CD7 и отрицательны по CD19. Для установления варианта Т-ОЛЛ необходимо оценить экспрессию CD1a, CD2, cyCD3, CD4, CD5, CD8, CD16, CD56, варианта TCR (Табл.2).
Одновременное отсутствие или аномальная реактивность с маркерами CD7 и CD19 при наличии позитивной реакции с миелоидными маркерами является доказательством нелимфоидного происхождения лейкоза даже при отсутствии МРО. Для миелоидных клеток наиболее высокоспецифичными маркерами являются миелопероксидаза и лизоцим. До настоящего времени иммунологическая классификация миелолейкозов до сих пор очень несовершенна (Табл.3). Исключением являются мегакариоцитарные маркеры CD61, CD41, CD42 и эритроидный антиген гликофорин А, с помощью которых можно верифицировать мегакариобластный лейкоз (ОМЛ, вариант М6) и острый эритромиелоз (ОМЛ, вариант М7), но именно эти формы максимально узнаваемы клинически и морфологически и редко требуют проведения ИФТ с диагностической целью.
При обнаружении на бластных клетках одновременной яркой экспрессии антигенов различных гемопоэтических линий, т.е. при подозрении на бифенотипический лейкоз (БФЛ) дополнительным шагом интерпретации данных ИФТ является балльная оценка экспрессии маркеров (табл.4). Она проводится, согласно рекомендациям Европейской группы по исследованию лейкозов (EGIL), если не менее 10-20% лейкозных бластов одновременно экспрессируют миелоидные и лимфоидные маркеры. Каждый маркер оценивается определенным баллом. Диагноз БФЛ ставится при оценке больше 2 для миелоидной и 1 для лимфоидной линии. Предполагая БФЛ надо обращать внимание на внутриклеточную экспрессию не одного, а как минимум двух маркеров миелоряда, чтобы избежать ошибочной гипердиагностики. Кроме того, нужно помнить, что этот вариант острых лейкозов на самом деле является достаточно редким, для него не разработано специфических схем полихимиотерапии (ПХТ). Больные получают ПХТ согласно группе риска, определяемой по совокупности данных клиники, морфологии, цитохимии, цитогенетики и ИФТ.
Использование многоцветного (мультипараметрического) анализа показало, что практически у всех пациентов с острыми лейкозами фенотип патологических клеток является аберрантным, т.е. не полностью соответствующим какому-то определенному уровню дифференцировки нормальной клетки крови. Эта аномальная экспрессия отражает генетические изменения, лежащие в основе опухолевого перерождения лейкозной клетки. Таким образом, именно аберрации антигенной экспрессии позволяют отделять/дискриминировать здоровые клетки от патологических при анализе биологического материала пациентов с подозрением на онкогематологическое заболевание. К основным типам аберрантности фенотипа при острых лейкозах относятся
? эктопическая, (например, тимус-ассоциированная при Т-ОЛЛ, т.е. выявление в костном мозге или периферической крови бластов с фенотипом тимических лимфоцитов);
? полное отсутствие или низкий уровень экспрессии антигена, характерного для данной стадии дифференцировки, например, в некоторых случаях острого миелолейкоза с признаками созревания уровень экспрессии линейного маркера несопоставим с уровнем его экспрессии на неизмененных клетках миелоряда (Рис.4);
? асинхронная, т.е. одновременная экспрессия антигенов, относящихся к разным стадиям дифференцировки (в норме никогда не определяется одновременная экспрессия ранних и поздних антигенов) (Рис.5 А);
? избыточная экспрессия антигена (например, очень высокий уровень экспрессии CD10 при B II варианте острого лимфобластного лимфобласте);
? фенотипический профиль, практически не встречающийся в норме (клетки с яркой экспрессией CD7 определяются в костном мозге в норме с частотой Список литературы
4. Bene MC, Bernier M, Castoldi G. et al. Impact of Immunophenotyping on management of acute leukemias//Hematologica 1999 (84): 1024-1034.
5. Basso G, Buldini B., L.de Zen, Orfao A. New methodological approaches for immunophenotyping acute leukemias// Hematologica 2001 (86): 675-692.
6. Hoelzer D., Gokbuget N., Ottman O. et al. Acute Lymphoblastic leukemia//Hematology 2002(1):162-192.