стандарт fda что это
Сертификат GMP: подтверждение качества лекарственных средств
Сертификат GMP — это соблюдение изготовителем лекарственных препаратов требований надлежащей производственной практики. В России они сформулированы в национальном стандарте ГОСТ Р 52249-2009, который идентичен правилам, действующим в Европейском Союзе.
К каким производствам применима эта процедура?
В настоящее время в странах, которые контролируют соответствие стандарту GMP на своих территориях, его правила применяются для проверки качества следующих категорий продукции:
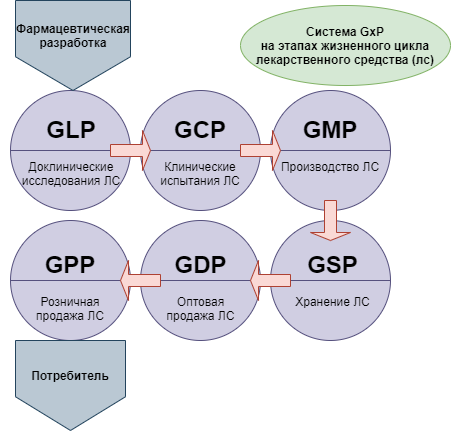
При этом для понимания ситуации следует принимать во внимание, что новая версия сертификации GMP — это не единственная система требований, которые в международной практике применяются в целях стандартизации медицинского обслуживания населения. Кроме них, производителям, работающим в такой сфере как фармация, необходимо соответствовать требованиям комплекса правил, объединенных под общим наименованием GxP:
Нормативная база
В Российской Федерации получение сертификата GMP осуществляется на основании действующей нормативной базы, включающей следующие основные правовые акты:
При этом необходимо принимать во внимание, что в настоящий момент наша страна вместе с другими государствами, входящими в состав Евразийского экономического союза, находится на этапе становления общего рынка, объединяющего фармацевтическое и косметическое производство в границах Союза. Это предполагает в том числе введение в действие единых требований к качеству и безопасности таких продуктов. В соответствии с принятым в мире порядком они реализуются в форме внедрения стандартов надлежащей производственной практики. Применение таких стандартов регулируется следующими нормативными документами:
Обратите внимание!
Для полноценного применения разработанного административного регламента необходимо решение Правительства о порядке реализации некоторых процедур, связанных с проведением фармацевтических инспекций. Приказ № 2945 вступит в силу только после принятия соответствующего постановления: пока этого не произошло.
Преимущества обладания сертификатом
Несмотря на необходимость проведения достаточно сложной и дорогостоящей процедуры, производители знают, что сертификация по стандартам GMP является весьма важной для представителей фармацевтической отрасли. В частности, оно обеспечивает продукции и производству следующие серьезные преимущества:
КОММЕНТАРИЙ ЭКСПЕРТА АТТЭК
Каков срок действия сертификата?
Срок действия российских сертификатов составляет 3 года. При этом срок действия иностранного сертификата GMP составляет от 1 до 3 лет. По истечении этого периода сертификацию потребуется проходить заново. Кроме того, это означает, что на протяжении всего этого срока компании необходимо обеспечить соответствие своего производства и продукции требованиям комплекса правил GMP.
Кто в России занимается сертификацией по стандартам GMP?
Сейчас сертификация контролируется департаментом развития медицинской и фармацевтической промышленности Министерства промышленности и торговли РФ. Он является организацией, ответственной за обеспечение надлежащего контроля за качеством, безопасностью и эффективностью лекарственных средств. Осуществлением требуемых сертификационных процедур занимается Государственный институт лекарственных средств и надлежащих практик (ФГБУ «ГИЛС и НП»).
Стандарт GMP в международной практике
Процесс сертификации на соответствие лекарственного препарата стандартам GMP в международной практике имеет комплексный характер, а ее основной целью является подтверждение безопасности и действенности продукции. В этой связи для достижения поставленной цели специалисты аккредитованных сертификационных организаций не ограничиваются оценкой ряда выборочных образцов лекарственных препаратов, как это часто предусматривается другими стандартами. В процедуру установления требуемого уровня качества лекарств любой международный центр сертификации лекарственных средств включает оценку предприятия, занимающегося его выпуском. В результате эксперты, занимающиеся проведением сертификации, анализируют конкретный препарат и процесс его выпуска в следующих областях:
Правила GMP в России
Порядок и сроки проведения всех операций в рамках этой процедуры, список лиц и организаций, ответственных за их осуществление, размер платы за проведение экспертной оценки и другие аспекты выполнения сертификации определены постановлением Правительства № 1314.
Процедура получения сертификата в России
Первым шагом для производителя, который желает пройти сертификацию, является подача соответствующего заявления в Минпромторг. В течение 10 рабочих дней специалисты ведомства проводят проверку корректности представленных в заявлении сведений и определяют возможность проведения сертификации.
В случае необходимости они вправе запросить у заявителя дополнительные документы, которые он обязан предоставить в течение 20 рабочих дней. В случае, если в отношении данного препарата принято положительное решение о проведении процедуры сертификации, необходимые данные направляются в ФГБУ «ГИЛС и НП», который в течение 20 рабочих дней с момента их получения обязан определить дату проведения сертификационных мероприятий и внести ее в график. Такая дата должна наступить не позднее 160 рабочих дней со дня, когда специалисты Минпромторга приняли положительное решение о сертификации, а сама экспертиза и расшифровка ее результатов должны занимать не более 10 рабочих дней.
На подготовку итогового отчета по результатам ее проведения исполнителю отводится 30 рабочих дней, а на его направление заявителю — 3 рабочих дня. Копия такого отчета также направляется в Минпромторг. На основании отчета формируется окончательное заключение, которое в случае положительного характера сопровождается выдачей сертификата производителю лекарственного препарата.
Документы для сертификации
Чтобы получить сертификат GMP в России, производитель обращается в уполномоченный орган с заявлением, к которому прилагает пакет документов, включающий:
Важнейшие документы предоставляются заявителем в копиях, поскольку при утере их восстановить невозможно или очень сложно. Правила регламентируют, что если заявление подает иностранный производитель, и некоторые документы в составе пакета представлены на другом языке, они должны быть переведены на русский язык и заверены в установленном порядке.
Сроки сертификации
Общая продолжительность процедуры сертификации складывается из следующих сроков.
Этап сертификационной процедуры
Максимальная допустимая продолжительность
Проверка полноты пакета документации, представленной с заявлением о сертификации, и правильности ее оформления, назначение инспекции
Направление информации о назначении инспектирования в уполномоченное учреждение, которое проводит проверку
Инспектирование и анализ лекарственного средства
Принятие решения о выдаче заключения по результатам инспекционного отчета
160-дневный период инспектирования включает внесение производителя в график инспекций, ожидание процедуры и проведение самой инспекции. Она должна занимать не более 10 рабочих дней.
Такой порядок действует, если в документации, поданной производителем, не обнаружат ошибок и недочетов, из-за которых ее могут направить на доработку. В этом случае вся процедура займет немногим более 180 рабочих дней, то есть свыше 8 месяцев.
Стоимость получения сертификата
Обязательной для всех производителей лекарственных средств, претендующих на получение сертификата, подтверждающего соответствие их продукции стандартам GMP, является оплата государственной пошлины за рассмотрение соответствующего заявления в Министерстве промышленности и торговли. Ее размер составляет 7500 рублей. Оплатить данную сумму необходимо еще до подачи заявления в ведомство, а ее размер никак не зависит от результатов рассмотрения документа.
Однако данная пошлина — это далеко не единственный и не самый крупный платеж, который потребуется осуществить производителю лекарств. Другой значительной статьей расходов станет плата за проведение экспертной оценки производства и продукции заявителя. Такая процедура выполняется специалистами ФГБУ «ГИЛС и НП»: для каждого из них предварительно проводится аттестация эксперта по GMP в России.
При этом размер платы за проведение оценки не является строго установленным, а определяется в зависимости от объема, характера и сложности необходимых процедур в соответствии с положениями приказа Министерства промышленности и торговли Российской Федерации от 11.01.2016 № 9 «Об утверждении методики определения размера платы за оказание услуги по инспектированию GMP». В случае, если проверка потребует проведения значительного объема работы и привлечения большого количества высококвалифицированных экспертов, размер платы за ее проведение может превышать 2,5 миллиона рублей.
Почему наличие сертификата FDA так важно
Мы давно уже привыкли к разнообразной и многочисленной маркировке качества продукции. Речь идет не только о международных стандартах качества (как ISO:9001), но и маркетинговых ходах в духе “Одобрено Ассоциацией Стоматологов”. Конечно, нельзя верить всему, что производитель указывает на упаковке, и следует обязательно разобраться, какие сертификаты действительно важны и нужны. Одним из знаменитых и действительно весомых является сертификат качества FDA. О нем и поговорим.
Что такое FDA?
Некоторые типы медицинского и косметологического оборудования, например лазеры, клинически исследуются только этой организацией. Поскольку исследования могут длится не один год (даже десятилетия), ведомство может со временем отозвать свой сертификат, если в ходе исследований выяснится, что продукт потенциально опасен для пользователей. Поэтому помимо статуса “approved” ведомство может присваивать отметку “regulated”.
Сертификат качества FDA гарантирует безопасность продукта по максимальному перечню критериев. Однако если речь идет о косметике и косметических аппаратах (приборах не медицинского назначения), статус “Approved” может быть получен только после выхода товара на рынок. В дальнейшем крем, сыворотка или косметологическое устройство проходят исследование на предмет нежелательных побочных эффектов для пользователей. Любой из пользователей, испытавший на себе негативный эффект от использования продукта (аллергическую реакцию от крема, например) могут заполнить онлайн-отчет на сайте ведомства. Таким образом Управление собирает огромное количество данных, проанализировав которые, можно выделить эффекты, частотность которых превосходит средние значения статистической вероятности.
Важно также понимать, что стандарты качества для лекарств и косметических средств различаются. Принадлежность товара к той или иной категории определяется законом с учетом способа и цели применения средства. Впрочем, это не мешает некоторым производителям продавать медикаменты под видом косметики и наоборот, классифицировать как медицинские средства косметические составы.
Что гарантирует сертификат FDA?
Высокая вероятность одобрения FDA! Или как искать акции с высоким потенциалом в секторе здравоохранения?
Содержание статьи
Можно ли на фондовом рынке за пару дней заработать 100% прибыли от вложенных средств? Конечно можно. 100%, 200% и даже 300%. Предела на фондовом рынке нет.
Все, что надо трейдеру для получения прибыли – это терпение.
Но мы все знаем, что чем выше прибыль, тем выше риск, а риск в основном связан с использованием кредитного плеча. Однако на фондовом рынке и так есть возможности получить огромную прибыль, не используя плечо. Тогда представляете, что будет если для высокоприбыльных сделок задействовать возможности кредитного плеча?
Например, в платформе R StocksTrader есть возможность использовать кредитное плечо для овернайт позиций 1:4. Таким образом, доходность можно смело умножать в 4 раза. Сразу закрадывается мысль, а в чем же здесь подвох и почему все трейдеры, работающие на фондовом рынке, до сих пор не стали миллионерами.
Да, есть определенного рода барьеры, которые мешают получить такую прибыль. Вся проблема кроется в том, как узнать, какая из примерно 8 000 акций, торгуемых на биржах США, завтра будет стоить на 300% дороже, чем сегодня. То есть вероятность купить такую акцию, ничего не анализируя, составит 1 к 8000. Для начала я покажу вам, что это за акции, и вы сразу поймете, что данную вероятность можно значительно увеличить.
Цена акции и доходность
Итак, если вы обратите внимание на рисунок, то поймете, что высокую доходность за очень короткий промежуток времени, можно получить только от дешевых акций.
Если акция стоит 1 USD, то для того, чтобы получить доходность в 100%, ей достаточно подняться в цене на 1 USD. Данный рост может спровоцировать любая позитивная новость.
Акция стоимостью в 200 USD не сможет показать такую же доходность за этот же период времени. Поэтому круг поиска можно значительно сузить, ограничив отбор максимальной ценой акции. Таким образом выбираем компании с ценой акции дешевле 5 USD. В итоге их количество уменьшается до 1208 штук.
Далее необходимо определить, в каком из секторов находятся акции, которые чаще всего очень сильно вырастают в цене. Забегая вперед скажу, что это сектор здравоохранения. В итоге круг поиска сужается до 389 акций.
В этом секторе можно выделить отрасль, в которой существует наибольшая вероятность найти интересуемую акцию. В данной ситуации — это биотехнологическая отрасль. В итоге мы получаем 260 акций, из которых необходимо найти тот “Бриллиант”, который принесет очень большую прибыль за короткий промежуток времени.
А теперь давайте разберемся, почему я указал вам на сектор здравоохранения и биотехнологические компании.
Наберитесь терпения, начнем издалека.
Сектор здравоохранения
Сектор здравоохранения включает в себя в том числе компании, которые занимаются разработкой, производством и продажей препаратов, предназначенных для лечения заболеваний. Эти компании делятся на два класса.
Фармацевтические препараты
К фармацевтическим препаратам относятся лекарства, которые состоят из растительных и синтетических химикатов и зачастую выпускаются в виде таблеток. Учитывая простоту производства и достаточно маленькие размеры, компания может производить их сотнями тысяч. Если лекарство приобретает статус «блокбастера», то это означает, что годовая прибыль от его продаж может исчисляться миллиардами.
Но простота производства говорит и о том, что это лекарство может стать легкой мишенью для конкуренции.
И как только истекает защита патента, доходы от продаж данного препарата резко падают, так как на рынке появляются более дешёвые препараты от других производителей. В итоге, если у компании есть только один препарат, то по мере приближения к дате истечения патента, акции начнут снижаться и чаще всего они опускаются до тех уровней, с которых начался их рост. Таким образом в эти компании желательно инвестировать в период действия патентов.
Биологические препараты
Биологические препараты представляют собой молекулы на основе белка, полученного из растительных жиров.
Такие лекарства сопровождаются более длительным и сложным процессом производства. В связи с этим вырастают затраты на производство и сохраняется достаточно высокий барьер входа на этот рынок, что могут позволить себе только крупные компании.
В этом сегменте конкуренция очень слабая, а стоимость данного лекарства иногда превышает 10 000 USD. Для того, чтобы выпустить биоаналог подобного препарата, компании необходимо доказать, что между оригиналом и аналогом нет клинически значимой разницы.
В США за последние 9 лет было одобрено только 9 биоаналогов препаратов, при этом они похожи между собой, но все же не являются точными копиями и соответственно не могут рассматриваться, как взаимозаменяемые. Таким образом в этой сфере крайне низкая конкуренция и очень высокие издержки.
Дополнительный риск на такие компании накладывает и внимание политиков, особенно в период предвыборной компании. Высокая стоимость лекарств, которые жизненно необходимы пациентам, используется политиками в своих целях. Они пытаются понизить стоимость этих лекарств, таким образом добиваясь расположения у своих избирателей.
Одним из примеров является препарат EpiPen от компании Mylan (NYSE: MYL), который используется во время анафилактического шока, вызванного аллергией. В 2016 году стоимость препарата достигла 600 USD и руководителя данной компании вызвали в конгресс для дачи показаний. Причиной оказалась высокая цена EpiPen. Сейчас этот препарат можно купить за 110 USD, а акции компании MYL с 2016 года упали с 70 USD до 19 USD за акцию.
Food and Drug Administration
Изобретение любого из препаратов вовсе не означает, что теперь можно отдыхать и смотреть как растет прибыль. Самым сложным этапом, через который нужно пройти биотехнологической компании, чтобы продать лекарство пациенту, это пройти процедуру одобрения от регулирующего органа Food and Drug Administration (FDA), за которую нужно еще и заплатить приличную сумму.
Food and Drug Administration (FDA) – это управление по санитарному надзору за качеством пищевых продуктов и медикаментов. FDA занимается контролем качества пищевых продуктов, косметических средств, лекарственных препаратов, табачных изделий и других товаров, а также осуществляет контроль за соблюдением законодательства и стандартов в этой области.
Компании, которые желают вывести на рынок какой-нибудь из своих лекарственных препаратов, обязаны пройти все стадии испытаний, установленные FDA.
Момент от начала разработки до выхода препарата на рынок может занять от 5 до 15 лет и стоить более 2 млрд USD (препарат Viagra начали испытывать в 1992 году, а в продажу он поступил только в 1998 году).
Фазы испытаний препаратов
Первая стадия испытаний в FDA подразумевает под собой доклиническое тестирование. То есть перед тем, как испытывать препарат на людях, компания должна протестировать его на животных и доказать, что он безопасен для них. Это первый и самый простой барьер. Как только препарат его преодолевает у компании появляется возможность подать заявку на рассмотрение нового лекарственного средства в FDA. Этот шаг называется Investigational New Drug application (IND) и также означает, что компания готова провести тестирование на людях.
Первая фаза испытаний
Далее наступает первая фаза одобрения. Если в течении 30 дней после подачи IND компания не получает отказ, она может начать испытание препарата на здоровых добровольцах (количество добровольцев может быть от 20 до 80), с целью выявить побочные эффекты.
Данный этап длится от 2 месяцев до нескольких лет и около 70% препаратов проходят эту фазу.
Вторая фаза испытаний
Затем наступает вторая фаза испытаний, в которой уже отбираются реальные пациенты, нуждающиеся в этом препарате. В данной фазе участвует несколько сотен человек и здесь определяется насколько эффективно действует препарат. Эту стадию проходит не более 30% препаратов.
Зачастую новости о прохождении второй фазы испытаний уже воспринимаются инвесторами как сигнал к действию и на этом этапе очень дешевые акции могут подниматься в цене на несколько сотен процентов.
Но так как это еще не окончательное испытание, то эти акции обычно в течение недели возвращаются на прежние уровни.
Третья фаза испытаний
Наступает третья фаза тестирования, в которой уже участвуют тысячи пациентов разного демографического происхождения, и длится она несколько лет.
На этом этапе отсеивается еще 50% препаратов.
Если все же препарат прошел данное испытание, компания может подать заявку на лицензию, разрешающую использование лекарства, а также получить одобрение на маркетинговую кампанию.
Четвертая фаза испытаний
Далее условно одобренный препарат проходит 4 фазу, в которой изучается его долгосрочное влияние на пациентов и выявляются возможные риски. В этой ситуации препарат уже продается пациентам, и в случае возникновения побочных эффектов, которые имеют накопительный эффект, FDA может отозвать лицензию и запретить к продаже данный препарат.
По статистике только 1 из 10 препаратов доходит до финала, поэтому этот вид бизнеса очень трудоемкий и затратный, при этом успеха добиваются немногие.
Если вы обратите внимание на биотехнологический сектор, то из 538 компаний акции 354 торгуются дешевле 10 USD. Из этих 538 компаний лишь у 63 рентабельность выше нуля.
Роль Food and Drug Administration в выборе компании
FDA имеет важную роль в анализе компаний и определении возможного потенциала роста стоимости акций.
На стадии одобрения препарата 95% компаний будут работать в убыток, поэтому анализ финансового состояния ничего не покажет.
А вот информация о поданной заявке IND в FDA, которую можно посмотреть на сайте организации www.fda.gov, должна привлечь ваше внимание, потому что акции таких компаний после одобрения могут очень быстро подняться в цене.
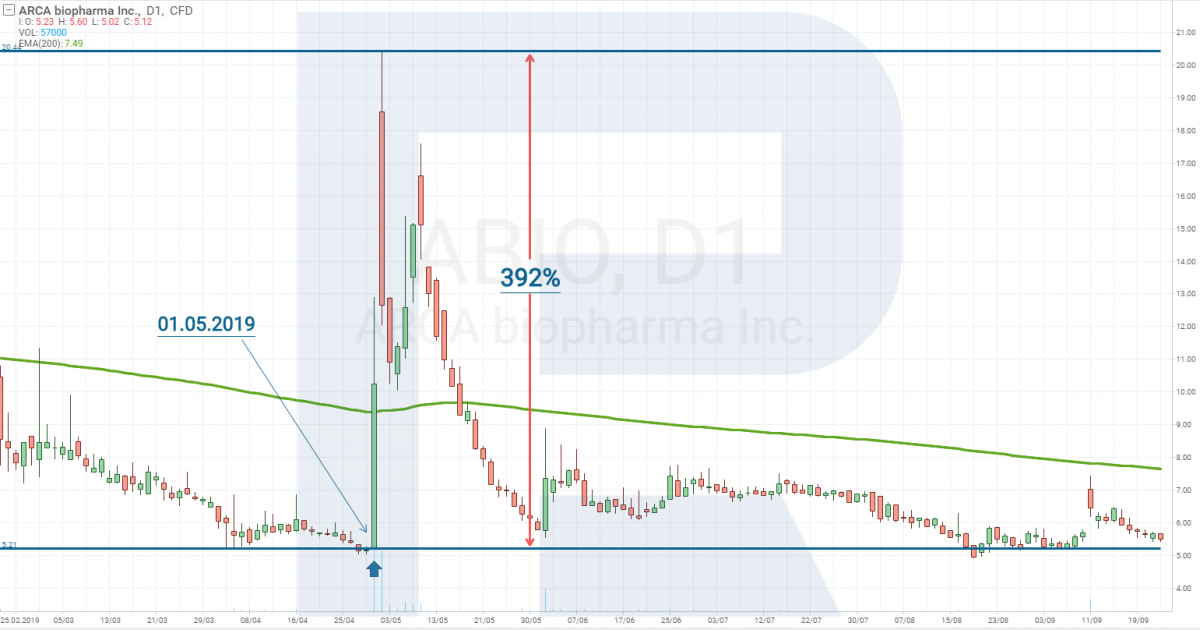
Простой пример: биотехнологическая компания ARCA biopharma, Inc. (NASDAQ: ABIO). 1 Мая 2019 года были опубликованы результаты испытаний 2 фазы препарата Genetic-AF.
На данной новости акции ARCA biopharma за два дня в моменте подорожали на 392%.
Ускоренная процедура одобрения FDA
Для того, чтобы определить насколько высока вероятность получить одобрение препарата от FDA, необходимо обратить внимание на сам препарат. В 1992 году появилась ускоренная процедура одобрения FDA, она относится к препаратам, которые лечат смертельные заболевания и не имеют аналогов в мире. Биотехнологические компании понимают, что, двигаясь в этом направлении, они с большей долей вероятности могут получить одобрение и возможность окупить расходы на разработку, поэтому они все больше берутся за трудноизлечимые болезни.
Именно ускоренная процедура одобрения привела к тому, что на рынке появились препараты для лечения СПИДа и других трудноизлечимых болезней.
Поэтому если в заявке указывается лекарство, аналогов которого в мире нет, и он предназначен для лечения, например, раковых опухолей, то есть очень высокая вероятность, что данный препарат попадет на рынок, а акции компании «взлетят в небеса».
Инвестиции в ETF
Помимо краткосрочной прибыли, акции сектора здравоохранения можно рассматривать и как хороший инструмент для долгосрочных инвестиций, особенно в условиях кризиса.
Люди болеют всегда независимо от того, есть кризис или нет, и они всегда нуждаются в лечении, а значит прибыли фармацевтических компаний, имеющих в продаже хотя бы несколько топовых препаратов, будут расти.
Конечно, все не так просто, как может показаться, ведь в этой ситуации необходимо анализировать и финансовое состояние компании, и сколько препаратов у них находится в продаже, когда истекает срок действия патентов, и многое другое. В данном случае заработать 300% за пару дней кажется гораздо проще, чем выбрать компанию, акции которой будут расти несколько лет.
Но не стоит отчаиваться, можно довериться профессионалам и купить биржевой фонд (ETF). В этой ситуации вы покупаете целый сектор или определенный набор акций и застрахованы от провала некоторых компаний на рынке.
К примеру ETF, торгуемый на бирже NYSE на сектор здравоохранения под тикером XLV, с 2008 года вырос в цене почти на 500%. Аналогично ETF, торгуемый на бирже NASDAQ на биотехнологический сектор под тикером IBB, с 2008 года показал доходность в 650%.
Вывод
Профессия трейдера привлекательна тем, что у вас всегда есть свобода выбора. Только вы решаете акции какой компании приобретать и только от вас зависит какую прибыль вы можете зафиксировать.
Работая с акциями из сектора здравоохранения, вы сами решаете по какому пути вам идти.
В данной статье раскрыта информация о том, какие испытания проходит компания, перед там как их препарат попадет на рынок. Каждая фаза испытаний препарата влияет на стоимость акции, и чем дальше продвинулась компания, тем выше вероятность того, что рост акций продолжится.
Cамой волатильной новостью является вторая фаза испытаний. Обычно после неё акции дорожают в цене на сотни процентов. Однако в последующем их цена резко падает, потому что вторая фаза испытаний не является решающей. В итоге рынок использует данную новость как возможность спекуляций и получения быстрой прибыли.
Однако этот путь очень рискованный, так как в любой момент может произойти непредвиденное событие. Например, выявят побочные эффекты, которые ранее были неизвестны, препарат попадёт под запрет продажи, после чего акции просто рухнут. Поэтому есть и третий вид торговли, консервативный – это инвестирование в ETF.
Инвестируйте в американские акции на выгодных условиях! Реальные акции на платформе R StocksTrader от 0,0045 USD за акцию с минимальной комиссией в размере 0,25 USD. Вы можете попробовать свои навыки торговли в платформе R StocksTrader на демо-счёте или открыть реальный торговый счёт, для этого нужно только зарегистрироваться на сайте RoboForex.com и открыть счёт.
Евгений Савицкий
Работает на валютном рынке с 2004 года. С 2012 года участвует в торговле акциями на американской бирже и публикует аналитические статьи по фондовому рынку. Принимает активное участие в подготовке и проведении обучающих вебинаров RoboForex.