состояние крайне тяжелое в реанимации на ивл что это такое
Реанимация. Понятие, типы состояний, реанимационное оборудование
Реанимация — это комплекс процедур, направленных на возвращение человека к жизни или поддержание жизненных функций организма больного. Пограничное состояние между жизнью и смертью, при котором необходимо проводить реанимацию в медицинской практике носит названием терминальное состояние. Реанимационные мероприятия направлены на выведения человека из терминального состояния.
Состояния требующие проведения реанимационных процедур
Преагональное состояние характеризует себя резким падением артериального давления, вплоть до 0. При этом у человека наблюдается помутнение или потеря сознания. Кожные покровы бледнеют. Пульс на периферических артериях может полностью отсутствовать, при этом на сонных артериях пульс сохраняется. На первоначальных этапах наблюдается учащенное сердцебиение, тахикардия, затем частота ударов резко снижается. Кислородное голодание приводит к серьёзным последствиям, нарушаются метаболические процессы.
Биологическая смерть — это состояние, которое наступает сразу после клинической смерти. Характеризует себя появлением необратимых изменений в работе органов и систем организма человека. Первым признаком биологической смерти врачи считают помутнение и высыхание роговицы глаза. При надавливании на глазное яблоко зрачок вытягивается в длину и напоминает кошачий. На коже появляются трупные пятна, а потом трупное окоченение – это поздние признаки биологической смерти.
Смерть мозга в практике реаниматологов есть случаи, когда удавалось восстановить сердечно-сосудистую деятельность организма, но при этом кислородное голодание вызывало необратимые процессы в головном мозге человека. Даже при проведении успешных реанимационных процедур после мозговой смерти человек способен существовать только в вегетативном состоянии. То есть поддержание жизненных функций, таких как дыхание, возможно, лишь при помощи специальной аппаратуры.
Дефибрилляция
Электрическая дефибрилляция является основным реанимационным мероприятием. Ее цель восстановление сократительной деятельности желудочков сердца и выведение больного из состояния клинической смерти.
Суть электрической дефибрилляции заключается в том, что после остановки сердца, до появления первых признаков биологической смерти на организм производится воздействие мощным одиночным импульсом тока, который оказывает на миокард возбуждающее действие. За счет этого сердце вновь начинает биться. Успех процедуры зависит от состояния больного и оттого, сколько времени прошло после полной остановки сердца.
Реанимационное оборудование
Реанимационное оборудование, как термин, обозначает не только оборудование для непосредственного осуществления оживления пациента, но и весь комплекс технических средств, которыми оборудуются реанимационные отделения клиник и включает в себя:
Краткий обзор моделей реанимационного оборудования
Дефибрилляция сердца проводится при помощи аппарата, который носит название дефибриллятор. Есть стационарные дефибрилляторы, а есть компактные переносные, которыми оснащены бригады скорой помощи.
Аппарат для дефибрилляции должен давать разряд не менее 200 кДЖ. Стационарные дефибрилляторы считаются более мощными, переносные или компактные обладают меньшей мощностью, но для реанимации больного их ресурсов будет достаточно.
Дефибриллятор Mindray BeneHeart D6
Mindray BeneHeart D6 –это аппарат для дефибрилляции нового поколения. Основные преимущества модели:
После реанимации поддерживать жизнь больного необходимо в условиях стационара. Чаще это происходит при помощи специальной аппаратуры. Вентиляции легких и многоканальных наносов. Аппарат ИВЛ помогает младенцу нормализовать дыхание, а многоканальный насос обеспечивает точное ведение необходимого количества медикаментов.
Медицинские насосы от Mindray
Человек, находящийся в реанимационном отделение, как никто другой нуждается в постоянном присмотре. Для того чтобы оптимизировать работу медицинских работников были созданы специальные прикроватные мониторы
Многоканальный шприцевой нанос помогает вводить несколько препаратов одновременно, в указанных дозах, обеспечивая пациенту максимальную безопасность. Кроме того, устройство обладает журналом, оно сохраняет данные и позволяет просмотреть последнюю совершенную манипуляцию. Также возможен беспроводной обмен данными, с другим устройствами.
Кроме этого, одним из способов поддержания жизнедеятельности в реанимации является энтеральное питание. Это процедура проводится при помощи зонда или специальных аппаратов. Энтеральное питание осуществляется специальными смесями. Часто процедура используется в ходе реабилитационных мероприятий, предназначенных для поддержания жизнедеятельности человека.
Пища может поступать в организм человека двумя способами:
Энтеральное питание должно обеспечивать естественные потребности человека в пище. Питание больного может осуществляться исключительно за счет ЭП.
Примеры:
Насос для энтерального питания SK-700 I обеспечивает безопасное введение питательных веществ. Аппарат оснащен специальным мешком, который помогает точно доставить питательные вещества. Кроме того, насос удобен в эксплуатации, благодаря новейшей конструкции. Помимо этого, система оснащена звуковыми и вязальными датчиками тревоги.
Многоканальный шприцевой насос SK-500 III/IIIA/IIIB/IIIC подходит для реанимации новорождённых детей. Устройство предназначено для введения нескольких лекарственных препаратов одновременно.
Мониторинг в реанимационном отделении
Человек, находящийся в реанимационном отделение, как никто другой нуждается в постоянном присмотре. Для того чтобы оптимизировать работу медицинских работников были созданы специальные прикроватные мониторы пациентов.
Монитор пациента Mindray BeneView T5 /T6/T8 осуществляет слежение за деятельностью организма человека, находящегося в отделении реанимации. Обычно подобного рода устройства предназначены для:
Монитор также контролирует показатели температуры тела больного и частоту его дыхания.
Монитор пациента нельзя назвать аппаратурой, предназначенной для оживления людей, попавших в реанимацию, но данное устройство позволяет медикам осуществлять максимально четкий контроль за жизнедеятельностью организма и при необходимости прийти пациенту на помощь.
Часто мониторы пациента подключают к «центральной» станции мониторирования». Такая станция представляет собой большой системный компьютер, который помогает специалистам следить за стоянием не одного, а нескольких пациентов.
Центральная стадия мониторинга Mindray Hypervisor VI позволяет подключать к себе до 64 пациентов и наблюдать за показаниями мониторов пациента. Такой контроль крайне важен для человека, находящегося на грани жизни и смерти, поскольку малейшее изменение в состоянии такого больного может привести к пагубным последствиям.
Реанимационные процедуры, будь то дефибрилляция или энтеральное питание, направлены на возвращение человека к жизни. Но успех процедур зависит не только от состояния больного, но и от качества аппаратуры, с помощью которой производиться реанимация человека. Компания UMETEX поможет в оснащении реанимационных отделений и отделений интенсивной терапии, а современное оборудование Mindray будет контролировать состояние пациента и поможет ему быстрее справиться с заболеванием.
Срочная госпитализация в отделение реанимации и интенсивной терапии
Служба «Спецмедпомощь» предлагает услуги отделения реанимации и интенсивной терапии. Воспользоваться платной реанимацией в Москве могут как жители столицы, так и граждане, прописанные в других регионах, но срочно нуждающиеся в экстренной помощи врачей. В отделении реанимации оказывается помощь больным с такими заболеваниями или травмами, как:
Определение состояния пациента
Больные могут поступать в отделение реанимации в состоянии различной тяжести, а именно:
Точная степень тяжести определяется непосредственно врачами реанимации на основании первичного осмотра, изучения описания болезни / травмы, анализа жалоб пациента (если он находится в сознании) и результатов диагностического обследования на специальном оборудовании.
Определив причину заболевания, а также степень его тяжести, врачи реанимации принимают решение о характере лечения и неотложных мерах.
Больные, направляемые в отделение реанимации и интенсивной терапии в этом состоянии, характеризуются:
Длительность нахождения пациента в тяжелом состоянии в реанимации зависит от скорости восстановления функций организма и, как правило, составляет от нескольких суток до недели.
По симптоматике соответствует тяжелому состоянию, с той лишь разницей, что при нем отсутствует как положительная (в сторону выздоровления), так и отрицательная динамика течения болезни. В отделение реанимации и интенсивной терапии такие пациенты, как правило, находятся до нескольких недель.
Лица в крайне тяжелом состояние, поступающие в реанимацию, характеризуются:
Крайне тяжелое состояние в реанимации сохраняется длительное время и требует наиболее срочного лечения и постоянного наблюдения.
Врачи реанимационного отделения
Врачи реанимации, присутствующие в отделении интенсивной терапии постоянно, – это реаниматолог (проводящий весь комплекс процедур по реанимации) и анестезиолог (отвечающий за анестезию пациентов, если она необходима). Задачами врачей реанимации являются диагностирование состояния больных и оказание им срочной помощи при клинической смерти, отказе органов либо остановке сердца.
Наше оснащение
Отделение реанимации и интенсивной терапии службы «Спецмедпомощь» оснащено дефибриллятором, электрокардиографом и аппаратом принудительной вентиляции легких, что позволяет проводить весь комплекс мероприятий по сохранению и поддержанию жизни пациентов.
Если вашему близкому человеку необходима платная реанимация в Москве, свяжитесь с нами по телефону +7 (495) 145-34-03. Специалисты расскажут вам все важные детали и ответят на вопросы.
| N П/П | НАИМЕНОВАНИЕ ОБОРУДОВАНИЯ | КОЛИЧЕСТВО, ШТ. | ПРИМЕЧАНИЕ |
|---|---|---|---|
| 1 | Дефибриллятор-монитор со встроенным кардиостимулятором, пульсоксиметрией и неинвазивным измерителем артериального давления | 1 | |
| 2 | Электрокардиограф трехканальный с автоматическим режимом | 1 | |
| 3 | Аппарат управляемой и вспомогательной искусственной вентиляции легких для применения в транспортных средствах скорой медицинской помощи | 1 | |
| 4 | Редуктор-ингалятор кислородный с 2-литровым баллоном | 1 | Обеспечение проведения кислородной (кислородно-воздушной) и аэрозольной терапии, а также подключения аппарата ИВЛ на месте происшествия и (или) при транспортировке в условиях скорой медицинской помощи |
| 5 | Аппарат ингаляционного наркоза газовой смесью кислорода и закиси азота портативный в комплекте с баллоном 1 л | 1 | |
| 6 | Портативный компрессорный небулайзер (ингалятор) с электропитанием от бортовой сети напряжением 12 В | 1 | |
| 7 | Определитель объемной скорости потока воздуха при выдохе — пикфлоуметр | 1 | |
| 8 | Экспресс-измеритель концентрации глюкозы в крови портативный | 1 | |
| 9 | Транспортный монитор | 1 | |
| 10 | Пульсоксиметр | 1 | |
| 11 | Насос шприцевой (дозатор лекарственных средств) | 1 | |
| 12 | Тележка-каталка со съемными носилками | 1 | |
| 13 | Приемное устройство с поперечным и продольным перемещением, углом наклона 15° | 1 | |
| 14 | Носилки продольно и поперечно складные на жестких опорах | 1 | |
| 15 | Носилки бескаркасные | 1 | Имеющие четыре пары ручек для переноски и стропы для фиксации пациента |
| 16 | Носилки кресельные складные | 1 | |
| 17 | Комплект шин транспортных складных | 1 | Включает: комплект шин транспортных складных детский, комплект шин транспортных складных взрослый, комплект шин-воротников транспортных |
| 18 | Матрас вакуумный иммобилизационный | 1 | |
| 19 | Укладка врача скорой медицинской помощи | 1 | Приказ Минздрава России от 26 марта 1999 г. N 100 |
| 20 | Штатив разборный для вливаний | 1 | С возможностью крепления к кровати, носилкам и т.п. |
| 21 | Набор акушерский | 1 | |
| 22 | Набор реанимационный большой для скорой медицинской помощи | 1 | |
| 23 | Набор травматологический для скорой медицинской помощи | 1 | Включает комплект шин транспортных складных |
| 24 | Набор при эндогенных отравлениях | 1 | |
| 25 | Контейнер термоизоляционный с автоматическим поддержанием температуры инфузионных растворов | 1 | |
| 26 | Баллон с вентилем под кислород, 10 л | 2 | |
| 27 | Редуктор кислородный | 2 | |
| 28 | Баллон с вентилем под закись азота, 10 л | 1 | |
| 29 | Редуктор закиси азота | 1 |
 |  |  |
 |  |  |
Отделение реанимации имеет хорошую диагностическую базу, благодаря чему постановка диагноза делается за 30-40 минут. А круглосуточная работа позволяет спасать людей независимо от тяжести их травм и заболеваний.
Исследования на магнитно-резонансном томографе проводятся в любое время суток. Транспортировка пациентов в тяжелом состоянии производится с применением транспортного респиратора, что обеспечивает возможность поддерживать интенсивную инфузионную терапию даже по дороге в отделение реанимации.
Звоните прямо сейчас:
Мы работаем круглосуточно, без выходных и перерывов!
Реаниматолог Сергей Винников: «Если человек попал на ИВЛ — это катастрофа»
Реанимация временного госпиталя в «Ленэкспо» заполнена пациентами до 40 лет, у всех минимум 75 процентов поражения легких. Как вирус начал бить по молодым и появилось ли средство, которое лечит ковид.
34 года и 92 процента поражения легких, 33 года — и 78 процентов. Вы все еще думаете, что в реанимацию с новой коронавирусной инфекцией попадают пожилые с букетом сопутствующих заболеваний? К сожалению, в третий и четвертый подъем вирус переключился на молодых и, в целом, здоровых. По какому пути пошел COVID-19? И что будет дальше? «Доктор Питер» поговорил на эту тему с реаниматологом временного госпиталя в «Ленэкспо» заведующим отделения реанимации и интенсивной терапии павильона №5 Сергеем Винниковым.
Сергей Винников
Медицина
Заведующий отделением реанимации и интенсивной терапии №7 павильона №5 «Ленэкспо»
Волна молодых
— Прошлой зимой я не помню среди поступивших 30-летних, — говорит Винников. — Где-то, начиная с лета, все чаще попадаются молодые пациенты, больше половины — от 30 до 40 лет. И беда в том, что у вируса встречаются молниеносные формы. Летом, вероятно, это было связано с жарой, пациенты погибали за 2-3 суток. Это очень тяжелые волны, это совершенно другой вирус.
Врач вспоминает, что в первую волну, если в семье заболевал один человек, то не факт, что заражались другие. Даже муж и жена, спавшие в одной кровати — один болел, а второй оставался совершенно здоров. В последние волны такого уже не происходит, если болеет один — то болеет и вся семья.
— Самое страшное, что начали болеть дети, и стали умирать. Это та вещь, которая называется «доигрались», — говорит Винников.
Читайте также
Сейчас в реанимации лежит сразу несколько пациентов с тяжелым поражением легких. При этом у них нет сопутствующих заболеваний, и им — не больше 40 лет.
— Девушка, 34 года, 92 процента поражения, акушерка молодая — 92 процента, парень, 33 года — 78 процентов, было еще два парня, до сорока, от 80 до 95 процентов, — перечисляет реаниматолог.
Есть в ОРИТ и пациент со 100-процентным поражением легких. Обычно такое пишут в посмертном эпикризе — но этот мужчина жив.
— При этом он в сознании, а на КТ — 100 процентов поражения, — рассказал Сергей Винников. — Он дышит кислородом, причем не на самом высоком потоке, бывают потоки и выше. Кушает, пьет, у него нормальные показатели давления. Не знаю, что будет дальше. Состояние может измениться в течение часа: захлопнется последняя альвеола и все. Очень часто бывают тромбоэмболические осложнения.
Мужчине — 58 лет, заболел он за сутки до поступления в госпиталь. У него было всего 25 процентов поражения легких. Но состояние ухудшалось стремительно, за два дня поражение достигло 100 процентов.
Читайте также
— Есть еще один очень тяжелый пациент, в реанимации он уже 27 суток, у него вторая волна. Не знаю, что с ним будет дальше, пока он дышит сам, без ИВЛ, — говорит врач.
Мытье головы мотивирует к жизни
Конечно, уже отработаны определенные схемы лечения. Врачи определяют группу тяжелых пациентов. Часто лечение проводят с помощью моноклональных антител, они показали довольно высокую эффективность, если их вводить как можно раньше от начала болезни.
— Первую дозу вводят еще на профильных отделениях, — объяснил Сергей Винников. — Даже иногда, пока еще не все анализы по стандартам получены. Приходится действовать на опережение. Если мы ждем анализов, отсрочка введения на пару суток может быть фатальной. Очень важно вовремя выявлять тяжелый больных на отделении. Вовремя начинать терапию моноклональными антителами и именно в отделениях — это не работа реанимации.
Если пациент попал на ИВЛ — это вообще катастрофа. Потому что крайне редко удается снимать пациентов с искусственной вентиляции легких.
Читайте также
Во временном госпитале в «Ленэкспо» есть психолог, она работает с пациентами на отделении, в реанимации. Но и реаниматологу иногда приходится самому выступать в роли психолога — многие заболевшие начинают заранее сдаваться, хандрить.
— Смотрю по обстоятельствам, я давно работаю, давно живу, ко всем нужен разный подход, — говорит Винников. — Очень часто для поднятия духа мы моем голову пациентам. Обычно женщинам — тем, которые уже идут на поправку, и тем, которые начинают совсем хандрить. Кажется, такая простая процедура, а она мотивирует к жизни. Они сразу хотят поправиться, потому что «немытая голова — это просто беда».
Сложнее с большими начальниками. Они привыкли всеми командовать, решают, какое лечение им необходимо, от чего-то отказываются.
— Приходится показывать, что туда — это выход в сторону отделения, а там лежат черные мешки и железная каталка, — объяснил Винников. — Еще они видят, как происходит комплекс реанимационных мероприятий: с закрытым массажем сердца, с интубацией, слышат, как «стреляет» дефибрилятор. Все это достаточно тяжело, мы стараемся ставить ширмы, чтобы они этого не видели, но все же… Многие тут же переворачиваются на живот. И выполняют все предписания врачей.
Читайте также
Люди перестали бояться
Вообще, ситуация, по сравнению с первой волной вируса, сильно поменялась. Если раньше все боялись, слушали и уважали врачей, в больницах работали волонтеры, которые помогали ухаживать за больными, поддерживали их, то сейчас все вдруг резко перестали бояться. Некоторые наотрез отказываются прививаться и носить средства защиты.
— Лежал парнишка, его ребенку только исполнился год. Умолял спасти, но как только стало полегче, на вопрос «почему не привился» начал говорить, что, дескать, в соседнем корпусе лежат привитые знакомые, они тоже болеют. Но они-то ходят сами, без кислорода! А он — в реанимации. Вот в чем разница прививки. Если бы он привился, то и ходил бы со своими знакомыми по корпусу, — рассказывает Сергей Винников.
Конечно, противников прививок достаточно во всем мире. В Италии, где в прошлом году в Палермо тела погибших вывозили грузовиками, а люди сидели, как мыши, сейчас с акциями протеста ходят студенты.
— Я не первый и не последний, кто говорит о прививках. Мы 10 лет показывали фильмы про врачей-убийц, ток-шоу о врачах-убийцах. В кои-то веки мы все успели, сделали вакцину. Но все сразу начали кричать: «Да ну так не бывает». Но это факт — вакцина помогает. А мы дошли до ручки, начали болеть и умирать дети! — эмоционален врач. — Из-за роста заболеваемости профильных специалистов просто не хватает. Инфекционистами уже работают переученные стоматологи. Ситуация очень тяжелая.
Исходы у больных с тяжелым течением COVID-19, госпитализированных для респираторной поддержки в отделения реанимации и интенсивной терапии
Изучение летальности и факторов риска смерти больных с COVID-19, госпитализированных для респираторной поддержки в отделения реанимации и интенсивной терапии (ОРИТ) лечебных учреждений Российской Федерации.
Материалы и методы
Ретроспективное исследование было выполнено в Федеральном дистанционном консультативном центре анестезиологии и реаниматологии для взрослых пациентов с COVID-19 на базе Первого МГМУ им. И.М. Сеченова. В исследование включали всех пациентов с известными исходами (смерть от любых причин или выздоровление) SARS-CoV-2 пневмонии, осложнившейся острым респираторным дистресс синдромом (ОРДС), которые были проконсультированы с 16 марта по 3 мая 2020 г. Факторы риска смерти анализировали с помощью многофакторной регрессионной модели Кокса.
В исследование были включены 1522 пациента, 864 (56,8%) мужчины и 658 (43,2%) женщин. Медиана возраста – 62 года. 922 (60,6%) больных находились в ОРИТ стационаров Москвы и Московской области, 600 (39,4%) – лечебных учреждений в 70 регионах Российской Федерации. У 995 (65,4%) больных диагноз SARS-CoV-2 инфекции был подтвержден с помощью ПЦР. Умерли 995 (65,4%) пациентов, выжили 527 (34,6%). Основными причинами смерти были ОРДС (93,2%), серКЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ И ТЕРАПИЯ, 2020, 29 (3) дечно-сосудистые осложнения (3,7%) и тромбоэмболия легочной артерии (1,0%). Летальность была низкой у пациентов, находившихся на оксигенотерапии (10,1%), и значительно повышалась у больных, которых приходилось переводить на неинвазивную (36,8%) или инвазивную (76,5%) вентиляцию легких. Риск смерти увеличивался с возрастом и в возрастных группах старше 50 лет у мужчин был достоверно выше, чем у женщин. В однофакторных моделях заболеваниями, ассоциировавшимися с развитием летального исхода, были артериальная гипертония, ИБС, инсульт, фибрилляция предсердий, сахарный диабет 2 типа, ожирение и солидные опухоли, однако в многофакторной модели, построенной по всем признакам с коррекцией по полу и возрасту, статистическое значение сохранили только ИБС (отношение рисков [ОР] 1,257, 95% доверительный интервал [ДИ] 1,064-1,485, p=0,007), сахарный диабет 2 типа (ОР 1,300, 95% ДИ 1,131-1,494, p Заключение
Основными факторами риска смерти больных с COVID-19, переведенных в ОРИТ для респираторной поддержки, были тяжесть ОРДС, прежде всего необходимость в ИВЛ, пожилой возраст, мужской пол, а также ИБС, ожирение и сахарный диабет 2 типа.
Вдекабре 2019 г. в Китае началась вспышка инфекции, вызванной SARS-CoV-2 (severe acute respiratory syndrome coronavirus-2) и получившей название COVID-19 (Coronavirus disease 2019) [1]. В течение последующих 6 мес общее число подтвержденных случаев новой коронавирусной инфекции в мире превысило 18 млн и продолжает быстро увеличиваться, особенно в США, странах Южной Америки и Индии. Только в июле 2020 г. в мире было зарегистрировано более 7 млн новых случаев SARS-CoV-2 инфекции. Хотя санитарно-эпидемиологические меры, которые в том или ином объеме предпринимаются во всех странах, охваченных пандемией COVID-19, позволяют ограничить распространение инфекции, их неизбежное ослабление сопровождается новым ростом заболеваемости (“второй волной»). В связи с этим основные надежды в борьбе с пандемией связывают с вакцинацией. В настоящее время в различных странах, включая Россию, разрабатываются почти 200 вакцин-кандидатов против SARS-CoV-2 [2]. Недавно были опубликованы обнадеживающие результаты клинических исследований 1-2 фазы вакцин, разработанных в России, Великобри тании, США или Китае 3. В рандомизированном контролируемом исследовании у 1077 здоровых добровольцев в возрасте 18-55 лет однократное введение рекомбинантной векторной вакцины ChAdOx1, содержащей ген белка S( spike) SARS-CoV-2 (университет Оксфорда, Великобритания), вызывало образование нейтрализующих антител в достаточном титре в 91% случаев и Т-клеточный ответ в 100% [4]. Достигнутый эффект сохранялся через 56 дней. Вакцинация часто вызывала развитие местных и общих нежелательных реакций, однако они не были тяжелыми и обычно контролировались парацетамолом. В августе 2020 г. в Российской Федерации была зарегистрирована первая отечественная вакцина против SARS-CoV-2, которая состоит из двух рекомбинантных аденовирусных векторов, несущих ген белка S вируса SARS-CoV-2. В двух открытых неконтролируемых исследованиях 1/2 фазы у 76 здоровых добровольцев введение вакцины вызывало мощный гуморальный и клеточный ответ и хорошо переносилось [6]. Основными нежелательными явлениями были боль в месте инъекции (58%), повышение температуры тела (50%), головная боль (42%), астения (28%) и боль в мышцах и суставах (24%). Серьезных нежелательных явлений не зарегистрировали.
У большинства больных COVID-19 характеризуется легким или бессимптомным течением, однако у части пациентов наблюдается развитие вирусной пневмонии, которая может осложниться острым респираторным дистресс синдромом (ОРДС) и полиорганной недостаточностью [7]. В Китае доля пациентов, которым потребовался перевод в отделение реанимации и интенсивной терапии (ОРИТ) для респираторной поддержки, среди госпитализированных больных с COVID19 варьировалась от 5% до 32% [8,9], в Ломбардии (Италия) в ОРИТ были госпитализированы 9% из 17713 пациентов с подтвержденной SARS-CoV-2 инфекцией [10], а в Чикаго (США) – 6,1% из 8673 больных [11] По данным исследований, проводившихся в Китае и других странах, риск более тяжелого течения COVID-19 выше у людей старшего возраста, страдающих различными сопутствующими заболеваниями, прежде всего сердечно-сосудистыми, сахарным диабетом и ожирением 16. Сходные результаты были получены в нашем ретроспективном исследовании, в которое были включены более 1000 пациентов с тяжелой и крайней тяжелой SARS-CoV-2 пневмонией, госпитализированных в ОРИТ лечебных учреждений Российской Федерации для респираторной поддержки [17]. Около половины из них были в возрасте старше 60 лет, а более чем у 2/3 пациентов имелись различные сопутствующие заболевания, в том числе артериальная гипертония и другие сердечно-сосудистые болезни, сахарный диабет, ожирение и др. У каждого пятого больного с тяжелым течением COVID-19 наблюдалось раннее развитие септического шока, факторами риска которого были возраст старше 50 лет и наличие трех сопутствующих заболеваний [18]. Мы не анализировали летальность больных в российских ОРИТ, так как исследование проводилось вскоре после начала вспышки SARS-CoV2 инфекции в Российской Федерации, а исходы заболевания у большинства пациентов еще не были известны вследствие непродолжительного срока наблюдения. Необходимо отметить, что в регулярно публикуемые статистические показатели включают данные о летальности больных только с подтвержденной SARS-CoV-2 инфекцией, в то время как у значительной части госпитализированных пациентов со средне-тяжелым или тяжелым течением COVID-19 результаты полимеразной цепной реакции (ПЦР) оказываются отрицательными, а диагноз устанавливают на основании клинической картины, эпидемиологического анамнеза и данных компьютерной томографии (КТ) органов грудной клетки. В нашей когорте доля таких пациентов составила около 40% [17]. Соответственно, исследования, которые проводятся в обычной клинической практике, позволяют получить более точное представление об исходах COVID-19.
Целью настоящего ретроспективного исследования было изучение летальности и факторов риска смерти больных с тяжелым течением COVID-19, госпитализированных для респираторной поддержки в ОРИТ лечебных учреждений Российской Федерации.
Материал и методы
Ретроспективное исследование было выполнено в Федеральном дистанционном консультативном центре анестезиологии и реаниматологии для взрослых на базе Первого МГМУ им. И.М. Сеченова. Анализировали заявки на консультацию больных с тяжелым течением COVID-19, поступавшие в центр по интернет из ОРИТ лечебных учреждений Москвы, Московской области и других регионов Российской Федерации. В исследование включали всех пациентов с COVID-19, которым потребовалась респираторная поддержка, независимо от результата ПЦР. Если результаты вирусологического исследования были отрицательными, сомнительными или отсутствовали, то диагноз устанавливали на основании клинических признаков острой респираторной инфекции, осложнившейся острой дыхательной недостаточностью, в сочетании с характерными данными компьютерной томографии (КТ) органов грудной клетки при отсутствии других этиологических факторов [19].
На основании полученных заявок оценивали демографические показатели, сопутствующие заболевания (артериальная гипертония, ишемическая болезнь сердца [ИБС], инсульт, фибрилляция предсердий, ожирение, сахарный диабет, бронхиальная астма, хроническая обструктивная болезнь легких [ХОБЛ], ревматические аутоиммунные заболевания, злокачественные опухоли, диагностированные в течение последних 5 лет, гемобластозы, ВИЧ-инфекция), данные КТ легких, уровень респираторной поддержки (оксигенотерапия, неинвазивная вентиляция легких [НИВЛ], искусственная вентиляция легких [ИВЛ] без признаков септического шока, ИВЛ в сочетании с септическим шоком [полиорганная недостаточность и необходимость в вазопрессорной поддержке]). Критериями диагноза ИБС считали острый инфаркт миокарда и/или вмешательства на коронарных артериях (стентирование или аорто-коронарное шунтирование) в анамнезе. Хроническую сердечную недостаточность не учитывали в связи с высокой вероятностью гипердиагностики этого состояния. Ожирение диагностировали на основании индекса массы тела: 2 – нормальная масса тела, 25,0-29,9 кг/м 2 – избыточная масса тела, 30,0-34,9 кг/м 2 – ожирение 1 степени, 35,039,9 кг/м 2 – 2 степени и ≥40,0 кг/м 2 – 3 степени. При анализе частоты ревматических заболеваний учитывали только аутоиммунные заболевания, такие как ревматоидный артрит, системная красная волчанка, системная склеродермия, псориатический артрит, анкилозирующий спондилит, системные васкулиты. Степень выраженности изменений на КТ легких оценивали с учетом распространенности и характера поражения [17].
Исходы (смерть или выздоровление) определяли с помощью базы данных COVID-19, которая создана в Российской Федерации по решению Министерства здравоохранения. В эту базу данных включается информация о всех пациентах, у которых установлен диагноз COVID-19, в том числе вероятный. Если исход заболевания в базе данных не был зафиксирован, то запрашивали соответствующее лечебное учреждение. Пациентов, у которых продолжалась респираторная поддержка на момент анализа, в исследование не включали.
Статистический анализ. Описательный статистический анализ проводился с использованием программы IBM SPSS Statistics 22 (IBM Corporation, США). Нормальность распределения определяли с помощью критерия Шапиро-Уилка. Данные для количественных показателей представлены в виде среднего арифметического и стандартного отклонения (при нормальном распределении) или в виде медианы и межквартильного размаха (при отклонении распределения от нормального). Данные для качественных переменных представлены в виде абсолютных значений и доли в процентах. Медианы количественных показателей сравнивали с помощью U-критерия Манна-Уитни (при сравнении двух групп). Сравнение групп по качественным признакам проводилось с помощью критерия χ2-Пирсона (при количестве наблюдений в группе ≥10) и точного критерия Фишера (при количестве наблюдений в группе
Результаты
Демографические показатели. Федеральный дистанционный консультативный центр анестезиологии и реаниматологии для взрослых на базе Первого МГМУ им. И.М. Сеченова был создан по приказу Минздрава РФ 16 марта 2020 г. С этого времени в центр ежедневно поступает по 100-180 заявок на консультацию больных с диагнозом COVID-19, госпитализированных в ОРИТ. В целом на 16 августа 2020 г. в центре проконсультированы 11829 больных, в том числе 3100 из Москвы, 909 из Московской области и 7820 из других регионов Рос сийской Федерации. Из этой когорты были отобраны первые 1522 пациента с известными исходами, которые были проконсультированы до 3 мая 2020 г. Наблюдение за пациентами с момента госпитализации в инфекционный стационар до развития конечной точки (летальный исход или выписка из стационара) проводили до 7 июля 2020 г. Медиана длительности наблюдения составила 16 (9; 27) дней.
Доля мужчин среди обследованных больных несколько превышала долю женщин (табл. 1). Женщины были достоверно старше мужчин (средний возраст 64,4±13,4 и 59,1±13,8 лет, соответственно; р ТАБЛИЦА 1. Демографические и клинические показатели 1522 больных с тяжелым и крайне тяжелым течением COVID-19, госпитализированных в ОРИТ
Клиническая характеристика пациентов. У всех больных наблюдалась картина ОРДС в виде двусторонней полисегментарной пневмонии 3-4 стадии и острой дыхательной недостаточности, требовавшей респираторной поддержки. Примерно 80% больных были переведены на ИВЛ в связи с нарастающей острой дыхательной недостаточностью, которую не удавалось контролировать оксигенотерапией или НИВЛ. Почти у каждого пятого пациента отмечено развитие септического шока, характеризовавшегося полиорганной недостаточностью и необходимостью в вазопрессорной поддержке. Доля пациентов, находившихся на ИВЛ, в Москве и Московской области была выше (86,5% и 88,5%), чем в других регионах Российской Федерации (66,3%), а доля больных, которым потребовалась только оксигенотерапии, в московском регионе была, наоборот, в несколько раз ниже (4,9%, 8,2% и 24,7%, соответственно).
У большинства больных имелись различные сопутствующие заболевания. Чаще всего встречались артериальная гипертония (59,5%), сахарный диабет 2 типа (26,7%) и ожирение (26,0%), несколько реже – ИБС (15,4%), инсульт в анамнезе (7,4%), фибрилляция предсердий (10,6%) и ХОБЛ (5,1%). Частота других заболеваний, в том числе бронхиальной астмы, злокачественных новообразований, ревматических аутоиммунных заболеваний и ВИЧ-инфекций была низкой и не превышала 5%.
У 363 (23,9%) пациентов не были выявлены сопутствующие заболевания, у 395 (26,0%) – имелось по крайней мере одно заболевание, у 383 (25,3%) – два, у 379 (24,9%) – три и более.
Выживаемость пациентов. За период наблюдения умерли 995 (65,4%) пациентов, выжили 527 (34,6%). Медиана выживаемости пациентов, рассчитанная методом Каплана-Майера, составила 17 (15,7; 18,2) дней (рис. 1). С момента госпитализации в стационар 14- и 28-дневная выживаемость пациентов равнялась 56,0% и 36,4%, соответственно. В Москве за период наблюдения умерли 551 (74,5%) из 740 человек, в Московской области – 143 (78,6%) из 182, в других регионах – 301 (50,2%) из 600.
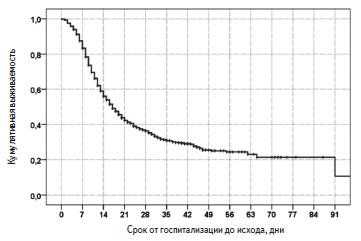
Причины летального исхода включали в себя ОРДС (93,2%), сердечно-сосудистые осложнения (3,7%), тромбоэмболию легочной артерии (1,0%), осложнения онкологических заболеваний (0,9%), “септические» осложнения (0,7%), осложнения цирроза печени (0,3%), осложнения ВИЧ-инфекции (0,1%) и туберкулез (0,1%).
Летальность пациентов, находившихся на оксигенотерапии, составила 10,1% (20/199), НИВЛ – 36,8% (35/95), ИВЛ – 76,5% (940/1228). Самой высокой летальность была среди пациентов, у которых имелись признаки септического шока – 86,6% (246/284). Медиана длительности ИВЛ у умерших пациентов равнялась 6 (3; 12) дней, а медиана длительности ИВЛ до экстубации у выживших пациентов – 13 (7; 21) дней. Среди пациентов, у которых диагноз SARS-CoV-2 инфекции, был подтвержден и не был подтвержден с помощью ПЦР, летальность не отличалась – 63,5% и 68,9%, соответственно.
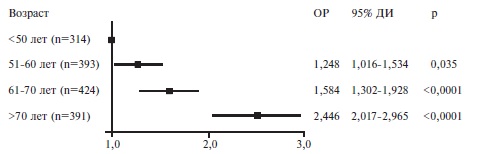
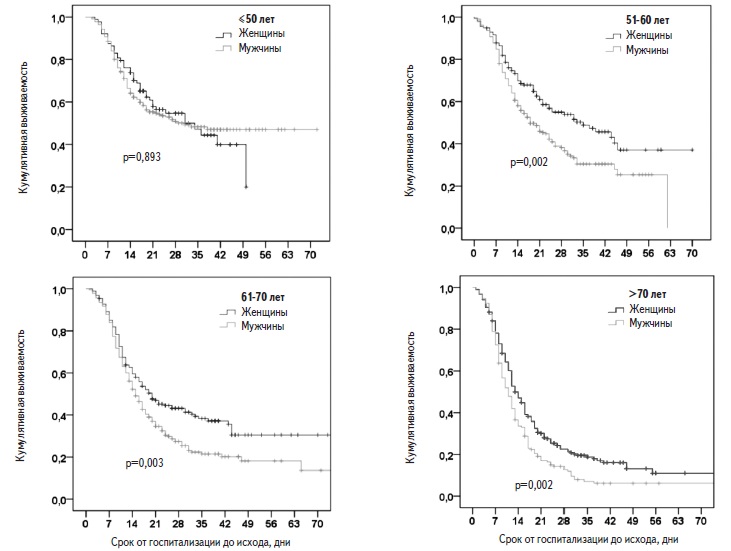
Факторы риска смерти. Пациенты, у которых наступил летальный исход, были старше выживших больных (табл. 2). В регрессионной модели Кокса риск смерти у пациентов старше 50 лет был достоверно выше, чем у больных более молодого возраста, и достигал максимума у пациентов старше 70 лет (рис. 2). Выживаемость в значительной степени зависела как от возраста, так и от пола. Среди пациентов старше 50 лет выживаемость у мужчин была достоверно ниже, чем у женщин, однако среди пациентов в возрасте ≤50 лет выживаемость не различалась у мужчин и женщин (рис. 3).
| Параметры | Выжившие (n=527) | Умершие (n=995) | p | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Возраст, лет; Me (IQR) | 56 (48; 64) | 65 (56; 74) | ТАБЛИЦА 3. Отношение рисков смерти, рассчитанное в регрессионной модели Кокса для сопутствующих заболеваний| Фактор | Исходная модель | Модель 1 | Модель 2 | ОР; 95% ДИ | p | ОР; 95% ДИ | p | ОР; 95% ДИ | p | Примечание: Исходная модель: однофакторный анализ; *анализ двух признаков совместно – пол и возраст; Модель 1: многофакторный анализ каждого признака по отдельности с коррекцией по полу и возрасту; Модель 2: многофакторный анализ по всем признакам с коррекцией по полу и возрасту | | |||||||||
| Пол (мужской) | 1,167; 1,029-1,324 | 0,016 | 1,358*; 1,194-1,545 | 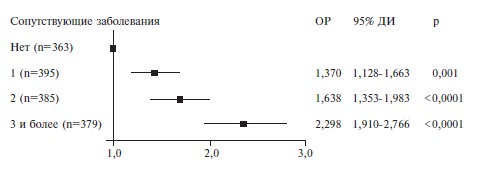 Рис. 4. Отношение рисков смерти пациентов в зависимости от числа сопутствующих заболеваний Рис. 4. Отношение рисков смерти пациентов в зависимости от числа сопутствующих заболеваний | |||||||||||||||||||
Лабораторные показатели. У умерших пациентов количество лейкоцитов, нейтрофилов и содержание глюкозы в крови были выше, чем у выживших больных, а количество тромбоцитов и сывороточное содержание альбумина оказалось ниже (табл. 4). В то же время концентрации С-реактивного белка (СРБ), фибриногена и D-димера достоверно не отличались между двумя группами. Частота острого повреждения почек (ОПП) была достоверно выше в группе умерших пациентов (26,7% и 8,5%, соответственно; p 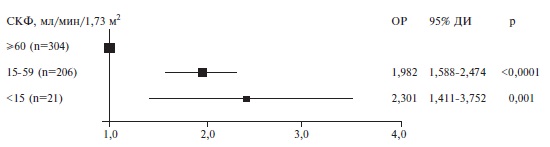
| Параметры | Все пациенты | Выжившие | Умершие | p | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Гемоглобин, г/л | 126 (110; 136), n=449 | 132 (119; 145), n=158 | 125 (110; 135), n=219 | 0,859 | ||||||||||||
| Лейкоциты, ×10 9 /л | 8,1 (5,6; 11,8), n=595 | 7,2 (5,0; 9,9), n=227 | 9,0 (6,3; 12,6), n=368 | 9 /л | 0,9 (0,6; 1,3), n=519 | 1,0 (0,6; 1,3), n=190 | 0,9 (0,6; 1,3), n=329 | 0,167 | ||||||||
| Нейтрофилы, ×10 9 /л | 6,2 (3,9; 8,8), n=351 | 5,3 (3,6; 7,6), n=139 | 6,9 (4,3; 9,3), n=212 | 0,001 | ||||||||||||
| Тромбоциты, ×10 9 /л | 235 (170; 293), n=371 | 191 (144; 268), n=198 | 180 (132; 244), n=304 | 0,050 | ||||||||||||
| Альбумин, г/л | 32,0 (27,9; 36,9), n=278 | 33,1 (28,8; 37,1), n=97 | 31,0 (27,0; 35,7), n=181 | 0,010 | ||||||||||||
| Глюкоза, ммоль/л | 7,3 (5,8; 9,9), n=436 | 6,9 (5,6; 8,5), n=164 | 7,7 (5,9; 10,8), n=272 | 0,001 | ||||||||||||
| СРБ max, мг/л | 131,0 (72,8; 209,0), n=218 | 117,5 (42,0; 207,0), n=86 | 133,5 (96,0; 212,0), n=132 | 0,231 | ||||||||||||
| Фибриноген, г/л | 5,1 (3,9; 7,2), n=234 | 5,1 (4,0; 7,3), n=100 | 5,3 (3,9; 7,1), n=134 | 0,866 | ||||||||||||
| Д-димер, нг/мл | 820 (384; 2348), n=95 | 727 (381; 1957), n=36 | 930 (426; 2682), n=59 | 0,485 | ||||||||||||
| Поражение почек, n (%) | 335/587 (57,1) | 83/210 (39,5) | 252/377 (66,8) | 2 | 64,6 (43,7; 84,0), n=531 | 76,7 (61,0; 92,4), n=197 | 57,0 (36,5; 77,4), n=334 | 2 | 59,0 (36,0; 80,8), n=510 | 75,3 (56,0; 89,4), n=193 | 46,9 (27,5; 72,2), n=317 | Поражение печени, n (%) | 283/1201 (23,6) | 85/433 (19,6) | 198/768 (25,8) | 0,090 |
| АЛТ max, ед/л | 41,1 (28,1; 73,0), n=515 | 43,0 (29,2; 76,0), n=194 | 40,0 (27,3; 69,0), n=321 | 0,320 | ||||||||||||
| АСТ max, ед/л | 56,0 (39,0; 93,0), n=500 | 53 (36,0; 83,5), n=189 | 58,0 (40,0; 101,7), n=311 | 0,040 | ||||||||||||
| Общий билирубин, мкмоль/л | 13 (9; 20), n=88 | 12 (8; 15), n=33 | 14 (9; 27), n=55 | 0,072 | ||||||||||||
| ЛДГ max, ед/л | 619 (418; 875), n=179 | 511,6 (375; 694), n=56 | 675 (495;994), n=123 | 0,003 |
Обсуждение
В нашем исследовании летальность у 1522 больных с тяжелым течением COVID-19, госпитализированных для респираторной поддержки в ОРИТ лечебных учреждений Российской Федерации, составила 65,4%. В течение первых 14 дней после госпитализации в инфек ционный стационар умерли 44,0% больных, а в течение 28 дней – 63,6%. В качестве причины смерти у 93% больных был указан ОРДС. Летальность была низкой (10,1%) у пациентов, находившихся на оксигенотерапии, однако она значительно увеличивалась при прогрессирующем течении заболевании и достигала 76,8% у больных, которых приходилось переводить на ИВЛ. Самой высокой летальность (86,6%) была у пациентов с септическим шоком, характеризовавшися полиорганной недостаточностью и необходимостью в вазопрессорной поддержке. Следует отметить, что у больных с тяжелым течением COVID-19 именно вирус, а не вторичные бактериальные инфекции является ведущей причиной развития сепсиса и септического шока [20]. В пользу этого свидетельствуют раннее развитие септического шока у значительной части пациентов [18] и отрицательные результаты бактериологического исследования крови и выделений из нижних дыхательных путей более чем у 75% больных сепсисом, развившимся на фоне COVID-19 [21].
В исследованной когорте летальность больных, госпитализированных в ОРИТ, была практически одинаковой в Москве и Московской области (74,5% и 78,6%, соответственно) и существенно ниже (50,2%) в других регионах России. Вероятно, это объяснялось тем, что в Московском регионе, где было зарегистрировано максимальное число случаев SARS-CoV-2 инфекции, в ОРИТ переводили пациентов с наиболее тяжелым течением пневмонии, прежде всего нуждавшихся в ИВЛ. Так, частота ИВЛ у больных, поступивших в ОРИТ лечебных учреждений Москвы и Московской области, превышала 85%, в то время как в других регионах России только около 66% больных, переведенных в ОРИТ, нуждались в ИВЛ, а примерно 25% пациентов получали оксигенотерапию.
Для достоверного диагноза SARS-CoV-2 инфекции необходим положительный результат ПЦР, однако в исследованной когорте примерно у трети пациентов диагноз не удалось подтвердить с помощью вирусологического исследования. Тем не менее, во всех этих случаях наличие COVID-19 не вызывало сомнения и подтверждалось как клиническими данными (острая респираторная инфекция, осложнившаяся острой дыхательной недостаточностью, при отсутствии других возможных этиологических факторов), так и типичными результатами КТ органов грудной клетки (двусторонние зоны “матового стекла» ± зоны консолидации и ретикулярные изменения легких). Высокие чувствитель
ность и специфичность КТ органов грудной клетки в диагностике SARS-CoV-2 инфекции подтверждаются результатами исследований, проводившихся в других странах 23. Летальность больных с подтвержденным и неподтвержденным диагнозом SARS-CoV-2 инфекции в нашем исследовании была практически одинаковой.
Хотя пандемия COVID-19 продолжается уже более полугода, данные о летальности больных, которым потребовалась госпитализация в ОРИТ, остаются ограниченными. P. Quah и соавт. провели мета-анализ 15 исследований, в которых оценивали летальность у 3798 больных с COVID-19, поступивших в ОРИТ [25]. Эти исследования проводились в разных странах, в том числе в Китае, США, Италии, Испании, Германии, Дании и Великобритании. Большинство из них были небольшими и включали в себя не более 100 пациентов. В целом летальность составила всего 25,7%, однако более половины больных оставались в ОРИТ на момент публикации, поэтому очевидно, что приведенный показатель является заниженным и его не следует сравнивать с таковым в нашем исследовании, в которое включали только пациентов с известными исходами SARS-CoV-2 пневмонии. Например, в самом крупном итальянском исследовании, в которое были включены более 1500 больных с COVID-19, госпитализированных в ОРИТ, на момент анализа летальность равнялась 26%, однако 58% больных продолжали лечение в ОРИТ, и только 16% пациентов были выписаны [10]. В исследованной нами когорте летальность увеличилась с 44% через 14 дней до 63% через 28 дней. Необходимо также учитывать и различную частоту ИВЛ, которая варьировалась от 35,4% в китайских исследованиях до 89,3% в исследованиях, проведенных в США. В целом частота ИВЛ в исследованиях, включенных в мета-анализ, была ниже (70%), чем в российской когорте (около 80%). В другом мета-анализе были обобщены результаты 24 наблюдательных исследований в целом у 10150 пациентов с COVID-19, госпитализированных в ОРИТ в лечебных учреждениях Азии, Европы и Северной Америки [26]. Летальность варьировалась от 0 до 84,6% и в среднем составила 41,6%. Следует отметить, что только в 7 исследованиях исходы были известны у всех больных, причем только в одно из них было включено достаточно количество больных (n=371), в то время как в остальных оно варьировалось от 1 до 50 (в целом 80). В более крупном исследовании, проводившемся в НьюЙорке, летальность в ОРИТ достигла 78% [27]. Кроме того, авторы мета-анализа не оценивали тяжесть пациентов, поступивших в ОРИТ, в частности частоту ИВЛ.
В опубликованных ранее исследованиях также была выявлена ассоциация между сахарным диабетом и более тяжелым течением COVID-19. Например, в крупном американском исследовании (n=7162) частота сахарного диабета у пациентов, поступивших в ОРИТ, была в несколько раз выше, чем у больных, которым не потребовалась госпитализация [42]. Сходные данные были получены в другом американском исследовании [15]. В итальянском исследовании у 373 госпитализированных больных с COVID-19 сахарный диабет ассоциировался с достоверным увеличением риска летального исхода (относительный риск 1,56; 95% ДИ 1,05-2,02) [43].
ХОБЛ и бронхиальная астма в исследованной нами когорте больных с тяжелым течением COVID-19 встречались реже (5,1% и 2,3%, соответственно), чем в общей российской популяции [44]. Результаты метаанализа 6 исследований у 1558 больных COVID-19 показали, что ХОБЛ является независимым фактором риска прогрессирования SARS-CoV-2 инфекции [45]. В нашем исследовании частота ХОБЛ у умерших пациентов примерно в два раза превышала таковую у выживших. Тем не менее, роль этого заболевания как фактора риска смерти у пациентов, госпитализированных в ОРИТ, не была подтверждена при многофакторном анализе.
Низкая частота бронхиальной астмой у пациентов с COVID-19 была отмечена и в других исследованиях [46]. S. Lovinsky-Desir и соавт. показали, что наличие бронхиальной астмы у больных с COVID-19 не сопровождалось ухудшением прогноза независимо от возраста, наличия ожирения или других сопутствующих заболеваний [47]. В нашем исследовании частота бронхиальной астмы у умерших и выживших пациентов была одинаковой. Высказано предположение, что особенности иммунного ответа у пациентов с бронхиальной астмой или терапия ингаляционными глю ко кор ти костероидами могут препятствовать более тяжелому течению SARS-CoV-2 пневмонии [46,48], хотя благоприятный эффект последних вызывает сомнение. Бронхиальная астма часто асоциируется с увеличением количества эозинофилов, которые обладают как провоспалительными эффектами, так и иммунорегулирующей противовирусной активностью. Однако в настоящее время нет данных о том, что эозинофилы оказывают защитное действие или, наоборот, способствуют поражению легких при SARS-CoV-2 инфекции, хотя эозинопения позволяет предсказать более тяжелое течение заболевания [49]. В нашей когорте абсолютное число эозинофилов в крови было ниже 0,02 × 109/л у большинства больных, госпитализированных в ОРИТ, а случаев эозинофилии крови мы не зарегистрировали [50].
Частота других сопутствующих заболеваний, которые теоретически могут повысить риск смерти больных с тяжелым течением COVID-19, в том числе злокачественных опухолей, гемобластозов, ревматических аутоиммунных заболеваний (таких как ревматоидный артрит, системная красная волчанка и др.) и ВИЧинфекции, в исследованной когорте была низкой. У умерших пациентов частота солидных опухолей, диагностированных в течение последних 5 лет, в несколько раз превышала таковую у выживших больных (5,3% и 1,9%, соответственно), однако роль злокачественных новообразований как фактора риска смерти не была подтверждена при многофакторном регрессионном анализе Кокса. Частота аутоиммунных заболеваний, гемобластозов и ВИЧ-инфекции соответствовала таковой в общей популяции и была практически одинаковой у умерших и выживших пациентов.
Мы не анализировали прогностическое значение лабораторных показателей, так как подробные результаты анализов крови и мочи имелись далеко не во всех случаях. Следует отметить, что концентрации СРБ и Dдимера достоверно не отличались между группами выживших и умерших пациентов. Как и следовало ожидать, частота ОПП, которое служит одним из проявлений сепсиса и септического шока, была достоверно выше у умерших больных. В то же время разница частоты повреждения печени между двумя группами не достигла статистической значимости.
Заключение
В российских ОРИТ летальность больных SARS-CoV-2 пневмонией, нуждавшихся в респираторной поддержки, составила в среднем 65,4%. Летальность в значительной степени зависела от тяжести ОРДС и показаний к госпитализации в ОРИТ. Так, она была значительно выше у пациентов, которых переводили на ИВЛ, особенно при наличии признаков септического шока, и оказалась ниже в регионах Российской Федерации, где, в отличие от Москвы и Московской области, около четверти больных, поступивших в ОРИТ, не нуждались в НИВЛ или ИВЛ. Летальность у пациентов старше 50 лет, особенно мужчин, была выше, чем у больных более молодого возраста. По данным многофакторного анализа Кокса, факторами, ассоциировавшимися с более высоким риском смерти больных тяжелой SARS-CoV-2 пневмонией, осложнившейся ОРДС, были ИБС (инфаркт миокарда и/или вмешательства на коронарных артериях в анамнезе), ожирение (ИМТ≥35 кг/м 2 ) и сахарный диабет 2 типа.




