синдром мелкой передней камеры что это такое
Медицинская энциклопедия (сводная)
Синдром мелкой передней камеры
Синдром мелкой передней камеры
Циклохрусталиковый блок, который может развиваться как в процессе антиглаукомных операций, так и в послеоперационном периоде у больных с закрытоугольной глаукомой (Глаукома), возникает из-за ущемления хрусталика в короне отростков ресничного тела. В результате внутриглазная жидкость, продуцируемая ими, попадает в захрусталиковое пространство и стекловидное тело, что сопровождается повышением внутриглазного давления (Внутриглазное давление), которое, в свою очередь, усугубляется витреальным блоком, обусловленным увеличением объема стекловидного тела. В послеоперационном периоде циклохрусталиковый блок, как правило, ведет к полному исчезновению передней камеры, набуханию и быстрому помутнению хрусталика. Лечебная тактика должна быть направлена на раннее удаление хрусталика. Назначение мидриатических средств, например препаратов атропина, отсасывание стекловидного тела водят лишь к временному незначительному углублению передней камеры.
Относительный зрачковый блок развивается в послеоперационном периоде вследствие затруднения перехода внутриглазной жидкости из задней камеры в переднюю через зрачок или периферическую колобому радужки, произведенную во время операции. Причиной этого может служить тесный контакт зрачкового края или краев периферической колобомы радужки с передней поверхностью хрусталика (после антиглаукомных операций) или с передней гиалоидной мембраной стекловидного тела (после интракапсулярной экстракции катаракты). Эти явления часто усугубляются за заполнением передней камеры стерильным воздухом под давлением при завершении операции. Разобщение камер ведет к скапливанию внутриглазной глазной жидкости в задней камере и в пространстве за хрусталиком, уменьшению глубины передней камеры и смещению вперед радужки хрусталика. При затянувшемся зрачковом блоке пространство передней камеры иногда полностью исчезает. В результате может появиться эпителиально-эндотелиальная дистрофия роговицы, вторичная глаукома, что иногда приводит к слепоте (Слепота).
Лечебные мероприятия направлены на ослабление контакта зрачкового края радужки с передней капсулой хрусталика или стекловидным телом. Это достигается с помощью инстилляции мидриатических средств с преимущественным воздействием на мышцу, расширяющую зрачок. При сформировавшихся задних синехиях показана лазерная или оперативная иридэктомия.
Цилиохориоидальная отслойка развивается после полостных операций на глазном яблоке; сопровождающихся наружной фильтрацией внутриглазной жидкости между швами (экстракция катаракты, сквозные пересадки роговицы) или под конъюнктиву, а также при образовании фистул (после антиглаукомных операций). Дефицит внутриглазной жидкости приводит, в свою очередь, к ее выходу из стекловидного тела. В результате под склерой образуется относительный вакуум, ресничное тело и сосудистая оболочка отслаиваются от нее. В это пространство через фенестры сосудов ресничного тела выходит транссудат, количество которого увеличивается по мере потери жидкости стекловидным телом и уменьшения глубины передней камеры глазного яблока. Контакт радужки с задним эпителием роговицы также как и при циклохрусталиковом и относительном зрачковом блоках, может привести к эндотелиально-эпителиальной дистрофии роговицы, сращениям в радужно-роговичном углу, вторичному повышению внутриглазного давления и к слепоте. Поэтому во время операции необходимо контролировать герметичность шва с помощью флюоресценновой пробы (см. Глаз) в свете кобальтового фильтра осветителя операционного микроскопа, обнаружении наружной фильтрации между швами следует наложить дополнительные швы. После антиглаукомных операций целесообразно прикрыть фистулу в коньюктиве силиконовой лентой или пломбой, фиксируя их с помощью супрамидного шва к эписклеральной пластинке в стороне от фильтрационной подушки. Одновременно проводят патогенетическую лекарственную терапию, включающую подъконъюнктивные инъекции раствора кофеина, аппликации с 0,1% раствором адреналина, прием внутрь этамзилата (дицинона), сосудорасширяющих препаратов (кавинтона, пентоксифиллина, циннаризина). В случае отсутствия положительного эффекта показана супрацилиарная склеротомия. При завершении эвакуации субсклерной жидкости переднюю камеру глазного яблока восстанавливают путем введения стерильного изотонического раствора хлорида натрия через предварительно произведенный роговичный прокол.
Библиогр.: Краснов М.М. Микрохирургия глауком, М., 1974; Микрохирургия глаза, под ред. М.М. Краснова, с. 20, М., 1976; Руководство по глазной хирургии, под ред. М.Л. Краснова, с. 200, М., 1976.
СИНДРОМ МЕЛКОЙ ПЕРЕДНЕЙ КАМЕРЫ
СИНДРОМ МЕЛКОЙ ПЕРЕДНЕЙ КАМЕРЫ — осложнение, развивающееся чаще в послеоперационном периоде после нек-рых операций на глазном яблоке и характеризующееся прогрессирующим уменьшением пространства между задней поверхностью роговицы и передней поверхностью радужки, гипотензией или гипертензией глазного яблока.
Синдром мелкой передней камеры может быть результатом циклохрусталикового блока (так наз. злокачественная глаукома), относительного зрачкового блока, цилиохориоидальной отслойки.
Циклохрусталиковый блок может развиваться как во время выполнения антиглаукома-тозных операций, так и в нослеопе-рационном периоде у больных с закрытоугольной глаукомой (см.). Блок возникает из-за ущемления хрусталика в короне отростков ресничного тела. При этом отростки ресничного тела, продуцирующие внутриглазную жидкость (водянистая влага, Т.), оказываются позади хрусталика, в результате чего внутриглазная жидкость попадает в захрусталиковое пространство и стекловидное тело, что сопровождается повышением внутриглазного давления (см.). При этом циклохрусталиковый блок усиливается в связи с витреальным блоком (увеличением объема стекловидного тела). В послеоперационном периоде (см.) циклохрусталиковый блок, как правило, ведет к полному исчезновению передней камеры, набуханию и быстрому помутнению хрусталика (см.) и отсутствию тенденции к снижению внутриглазного давления. Назначение мидриатиков, напр, р-ра атропина, отсасывание стекловидного тела приводят лишь к временному незначительному углублению передней камеры. Леч. тактика при циклохрусталиковом блоке должна быть направлена на раннее удаление хрусталика (см. Катаракта).
Относительный зрачковый блок может развиться в послеоперационном периоде вследствие затруднения перехода внутриглазной жидкости из задней камеры в переднюю через зрачок или периферическую колобому радужки (см. Колобома), произведенную во время операции. При этом повышается внутриглазное давление, как следствие тесного контакта зрачкового края или краев периферической колобомы радужки с передней поверхностью хрусталика (после антиглаукоматозных операций) или с передней гиалоидной мембраной стекловидного тела (после интракап-сулярной экстракции катаракты). Эти явления часто усугубляются заполнением передней камеры стерильным воздухом под давлением при завершении операции. Такое разобщение камер ведет к тому, что внутриглазная жидкость скапливается в задней камере и в пространстве за хрусталиком. По мере рассасывания воздуха или небольшого количества жидкости передняя камера суживается, в результате чего смещаются вперед радужка и хрусталик, а при его отсутствии— только радужка. При затянувшемся зрачковом блоке пространство передней камеры может полностью исчезнуть. В результате этого развивается эпителиально-эндотелиальная дистрофия роговицы, вторичная глаукома, что может привести к слепоте (см.). Относительный зрачковый блок имеет место и при циклохрусталиковом блоке.
Леч. мероприятия при относительном зрачковом блоке должны быть направлены на ослабление контакта зрачкового края радужки с тканями хрусталика или стекловидного тела путем инстилляций мидриатиков с преимущественным воздействием на дилататор радужки. При невозможности расширить зрачок из-за сформировавшихся задних си-нехий показана лазерная, а в ряде случаев и дополнительная микрохирургическая иридэктомия (см.).
Образованная при этом периферическая колобома радужки позволяет восстановить циркуляцию жидкости из задней камеры в переднюю и нормализовать офтальмотонус и гидродинамику глаза (см.), после чего радужка и хрусталик принимают нормальное анатомическое положение.
Цилиохориоидальная отслойка развивается после полостных операций на глазном яблоке, сопровождающихся наружной фильтрацией между швами (экстракция катаракты, сквозные пересадки роговицы) или усиленной фильтрацией внутриглазной жидкости под конъюнктиву, образованием фистул между разрывами конъюнктивы и неадаптированными краями разреза конъюнктивы после антиглауко-матозных операций. Наружная или усиленная подконъюнктиваль-ная фильтрация ведут к дефициту внутриглазной жидкости, что сопровождается также потерей жидкости и стекловидным телом. В свою очередь, уменьшение объема внутреннего содержимого глаза при ригидной склере ведет к возникновению под ней относительного вакуума, поскольку ресничное тело и сосудистая оболочка не имеют со склерой прочных связей и легко отслаиваются от нее. В это пространство через фенестры сосудов ресничного тела выходит транссудат и развивается цилиохориоидальная отслойка, к-рая увеличивается по мере потери жидкости стекловидным телом и уменьшения глубины передней камеры глазного яблока.
При цилиохориоидальной отслойке развивается гипотония глазного яблока, в результате чего передняя камера глазного яблока становится мельче и даже может полностью исчезнуть. Контакт радужки с задним эпителием роговицы, так же как и при циклохрусталиковом блоке и относительном зрачковом блоке, может привести к эндотелиально-эпителиальной дистрофии роговицы, сращениям в углу передней камеры (радужно-роговичном углу, Т.), вторичному повышению офтальмотонуса и в конечном итоге — к слепоте.
При обнаружении наружной фильтрации между швами после экстракции катаракты или после сквозной пересадки роговицы необходимо наложение дополнительных швов. Во время операции нужно контролировать герметичность шва с помощью флюоресцеиновой пробы (см.) в свете кобальтового фильтра осветителя операционного микроскопа. После антиглаукоматозных операций целесообразно прикрыть фистулу в конъюнктиве силиконовой лентой или пломбой, фиксируя их с помощью супрамидного шва к эписклере (эписклеральной пластинке, Т.) в стороне от фильтрационной подушки. Под контролем флюоресцеиновой пробы решают вопрос о сроках снятия швов. Одновременно целесообразно проводить комплексную патогенетическую медикаментозную терапию, включающую подконъюнктивные инъекции 10% р-ра кофеина, аппликации с 0,1% р-ром адреналина, прием внутрь дицинона (этамзилата), сосудорасширяющих препаратов (кавинтон, трентал, стугерон).
В случае отсутствия положительного эффекта от указанных мероприятий показана супрацилиарная склеротомия с предварительным роговичным тангенциальным проколом ножом-иглой. Супрацилиарную склеротомию целесообразно производить в нижненаружном квадранте глазного яблока после разреза конъюнктивы и теноновой фасции (влагалище глазного яблока, Т.) на расстоянии 4—5 мм от лимба. Из одной точки делают сквозной разрез склеры, образуя лоскут в виде уголка со стороной 1,5—2 мм. При завершении эвакуации субсклерной жидкости переднюю камеру глазного яблока восстанавливают путем введения стерильного изотонического р-ра хлорида натрия через роговичный прокол. На конъюнктиву и те-нонову фасцию накладывают непрерывный шелковый шов. Под конъюнктиву с профилактической целью вводят антибиотики и кортикостероиды. Леч. тактика в послеоперационном периоде такая же, как и при других полостных операциях на глазном яблоке (см. Послеоперационный период).
Библиография: Алексеев Б. Н. Цпкло-хрусталиковый блок при глаукоме, Вести, офтальм., № 3, с. 32, 1972; Краснов М. М. Микрохирургия глауком, М., 1974; Микрохирургия глаза, под ред. М. М. Краснова, с. 20, М., 1976; Руководство по глазной хирургии, под ред. М. Л. Краснова, с. 200, М., 1976.
Синдром мелкой передней камеры
Это осложнение развивающееся после некоторых операций на глазном яблоке, характеризующееся прогрессирующим уменьшением пространства между задней поверхностью роговицы и передней поверхностью радужки, гипотензией или гипертензией глазного яблока.
В его основе обычно лежит циклохрусталиковый блок (так называемая злокачественная глаукома), относительный зрачковый блок или цилиохориоидальная отслойка.
Циклохрусталиковый блок, который может развиваться как в процессе антиглаукомных операций, так и в послеоперационном периоде у больных с закрытоугольной глаукомой, возникает из-за ущемления хрусталика в короне отростков ресничного тела. В результате внутриглазная жидкость, продуцируемая ими, попадает в захрусталиковое пространство и стекловидное тело, что сопровождается повышением внутриглазного давления, которое, в свою очередь, усугубляется витреальным блоком, обусловленным увеличением объема стекловидного тела.
В послеоперационном периоде циклохрусталиковый блок, как правило, ведет к полному исчезновению передней камеры, набуханию и быстрому помутнению хрусталика. Лечебная тактика должна быть направлена на раннее удаление хрусталика. Назначение мидриатических средств, например препаратов атропина, отсасывание стекловидного тела приводят лишь к временному незначительному углублению передней
камеры.
Относительный зрачковый блок развивается в послеоперационном периоде вследствие затруднения перехода внутриглазной жидкости из задней камеры в переднюю через зрачок или периферическую колобому радужки, произведенную во время операции.
Причиной этого может служить тесный контакт зрачкового края или краев периферической колобомы радужки с передней поверхностью хрусталика (после антиглаукомных операций) или с передней гиалоидной мембраной стекловидного тела (после интракапсулярной экстракции катаракты). Эти явления часто усугубляются заполнением передней камеры стерильным воздухом под давлением при завершении операции. Разобщение камер ведет к скапливанию внутриглазной глазной жидкости в задней камере и в пространстве за хрусталиком, уменьшению глубины передней камеры и смещению вперед радужки хрусталика.
При затянувшемся зрачковом блоке пространство передней камеры иногда полностью исчезает. В результате может появиться эпителиально-эндотелиальная дистрофия роговицы, вторичная глаукома, что иногда приводит к слепоте.
Лечебные мероприятия направлены на ослабление контакта зрачкового края радужки с передней капсулой хрусталика или стекловидным телом. Это достигается с помощью инстилляции мидриатических средств с преимущественным воздействием на мышцу, расширяющую зрачок. При сформировавшихся задних синехиях показана лазерная или оперативная иридэктомия.
Цилиохориоидальная отслойка развивается после полостных операций на глазном яблоке, сопровождающихся наружной фильтрацией ВГЖ между швами (экстракция катаракты, сквозные пересадки роговицы) или под конъюнктиву, а также при образовании фистул (после антиглаукомных операций).
Дефицит внутриглазной жидкости приводит, в свою очередь, к ее выходу из стекловидного тела. В результате под склерой образуется относительный вакуум, ресничное тело и сосудистая оболочка отслаиваются от нее. В это пространство через фенестры сосудов ресничного тела выходит транссудат, количество которого
увеличивается по мере потери жидкости стекловидным телом и уменьшения глубины передней камеры глазного яблока.
Контакт радужки с задним эпителием роговицы также как и при циклохрусталиковом и относительном зрачковом блоках, может привести к эндотелиально-эпителиальной дистрофии роговицы, сращениям в радужно-роговичном углу, вторичному повышению ВГД и к слепоте.
Поэтому во время операции необходимо контролировать герметичность шва с помощью флюоресценновой пробы в свете кобальтового фильтра осветителя операционного микроскопа, обнаружении наружной фильтрации между швами следует наложить дополнительные швы. После антиглаукомных операций целесообразно прикрыть фистулу в коньюктиве силиконовой лентой или пломбой, фиксируя их с помощью супрамидного шва к эписклеральной пластинке в стороне от фильтрационной подушки. Одновременно проводят патогенетическую лекарственную терапию, включающую подъконъюнктивные инъекции раствора кофеина, аппликации с 0,1% раствором адреналина, прием внутрь этамзилата (дицинона), сосудорасширяющих
препаратов (кавинтона, пентоксифиллина, циннаризина).
В случае отсутствия положительного эффекта показана супрацилиарная склеротомия. При завершении эвакуации субсклерной жидкости переднюю камеру глазного яблока восстанавливают путем введения
стерильного изотонического раствора хлорида натрия через предварительно произведенный роговичный прокол.
Методы хирургического лечения глаукомы
Врач-офтальмолог отделения микрохирургии №2
Кузьмицкая Л.Н.
Врач-интерн отделения микрохирургии №2
Гибчик А.Р.
Глаукома – распространённая группа заболеваний, характеризующаяся повышением уровня внутриглазного давления (ВГД), поражением зрительного нерва, нарушением полей зрения и приводящая к необратимой слепоте при отсутствии лечения.
Распространенность
По данным ВОЗ, в настоящее время количество страдающих глаукомой в мире доходит до 80–100 млн человек.
К 2020 году показатель может увеличится на 10 млн человек.
К 2030 г. по данным ряда исследований данный показатель может увеличится в два раза.
Несмотря на высокую распространенность заболевания, лишь половина страдающих глаукомой знает о своем диагнозе и получает адекватное лечение на ранних сроках заболевания.
Первичная глаукома имеет три основные формы: закрытоугольная, открытоугольная (ПОУГ) и смешанная. Вне зависимости от формы глаукомы основным фактором, который определяет риск поражения зрительного нерва, является высокое внутриглазное давление (ВГД). Достижение целевого ВГД предотвращает потерю зрительных функций и является основным показанием как медикаментозного, так и для хирургического вмешательств.
При отсутствии стабилизации ВГД в условиях максимального режима медикаментозного лечения и (или) при низкой комплаентности (приверженности) пациента назначенному лечению прибегают к хирургическому или лазерному лечению глаукомы.
Для понимания принципов оперативных вмешательств при глаукоме необходимо знать основные особенности оттока внутриглазной жидкости в глазу
Внутриглазная жидкость (ВГЖ) продуцируется отростками цилиарного тела. Далее она накапливается в задней камере глаза, откуда через зрачок попадает в переднюю камеру глаза.
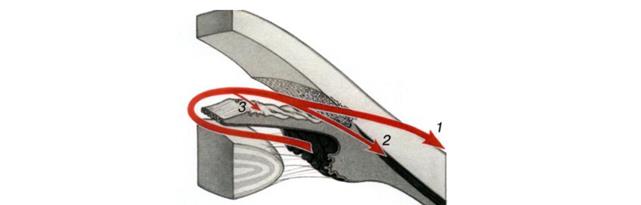
Существуют следующие путти оттока ВГЖ из передней камеры (рисунок 1):
Передняя камера →трабекулярный аппарат → шлеммов канал →выводящие коллекторы канала Шлемма → эписклеральные вены→ передние цилиарные вены.
В связи с тем, что данным способом оттекает около 85% всей ВГЖ, основные операционные манипуляции направлены на улучшение именно данного пути оттока.
Увеальная порция трабекулы → цилиарное тело → супрацилиарное и супрахориоидальное пространства →склеральные эмиссарии→ лимфатические сосуды и вены орбиты.
Рисунок 1 – передние пути оттока ВГД
(1- трабекулярный, 2 – увеосклеральный 3- дренаж через радужку)
4. Задний путь оттока (порция дренируемой ВГЖ незначительна)
Стекловидное тело → Периневральные пространства зрительного нерва и периваскулярные пространства ретинальной сосудистой системы.
Хирургические вмешательства при глаукоме можно разделить на три разновидности:
А) Направленные на образование новых путей оттока (иридэктомия, синустрабекулэктомия, глубокая склерэктомия, имплантация дренажных устройств)
Б) Направленные на улучшение оттока по естественным путям (вискоканалостомия, каналопластика, гониотомия, трабекулотомия)
В) Направленные на снижение продукции внутриглазной жидкости (циклокриотерапия, Nd: Yag laser циклодеструкция, Diode laser циклофотокоагуляция)
Европейское глаукомное общество советует применять следующие типы хирургических вмешательств:
Хирургическое лечение является первым методом выбора только при врожденной глаукоме и глаукоме со зрачковым блоком.
В остальных случаях лечение глаукомы остается «трехкомпонентным»: медикаментозным, лазерным и хирургическим.
Существует большое количество различных методик хирургического лечения глаукомы, а также их модификаций. В данной статье описаны наиболее распространенные варианты. Способ хирургического вмешательства определяется в каждом конкретном случае индивидуально.
Ⅰ Иридэктомия
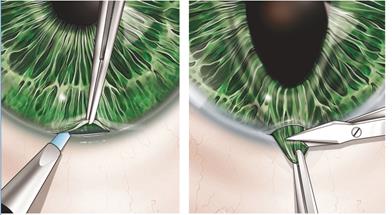
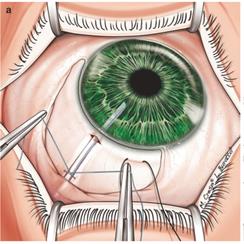
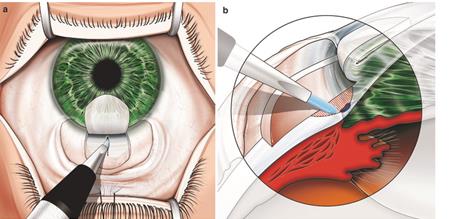
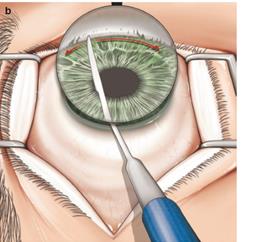
Ход операции. Выполнение разреза у лимба, захват и разрез периферической части радужки (рисунок 2) [1].
Рисунок 2 – Основные этапы иридэктомии.
В результате операции формируется отверстие в радужной оболочке, что способствует улучшению оттока внутриглазной жидкости из задней камеры в переднюю при зрачковом блоке.
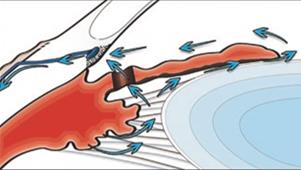
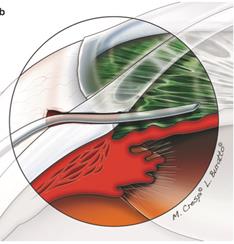
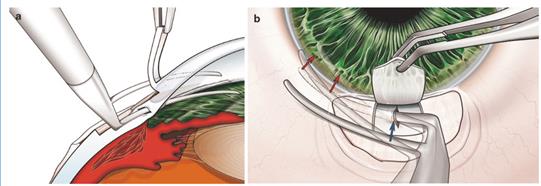
Новый путь оттока: задняя камера → отверстие в радужной оболочке → передняя камера (рисунок 3) [1].
Рисунок 3 – Новый путь оттока из задней камеры в переднюю при зрачковом блоке через отверстие в радужной оболочке (отображен стрелками)
Ⅱ ФИСТУЛИЗИРУЮЩИЕ ОПЕРАЦИИ
Историческая справка. В 1887 А. М. Маклаков предложил первую фистулизирующую операцию, которую он назвал косой склеротомией. Однако лишь с 1906 г фистулизирующие операции стали широко использоваться при лечении глауком ( корнео-склеральная трепанация по Эллиоту в 1906 г. и ириденклейз по Гольту в 1907 г.).
К фистулизирующим операциям при ПОУГ относится метод глубокой склерэктомии, основанный на формировании поверхностного и глубокого лоскутов склеры с иссечением последнего. В таком случае дополнительный отток ВГЖ осуществляется через фенестры в эпителии капилляров цилиарного тела и по супрахориоидальному пространству, а также в сосуды конъюнктивы.
В настоящее время глубокая склерэктомия выполняется редко, т.к. чаще выбор хирургов падает на «золотой стандарт» хирургического лечения глаукомы – синустрабекулэктомию.
Ⅱа СИНУСТРАБЕКУЛЭКТОМИЯ
Историческая справка: метод разработан в 1968 г. J.E. Cairns [2]
Синонимы: трабекулоканалэктомия, синусотрабекулэктомия, секторная синусэктомия, субсклеральная склерэктомия, склерокератэктомия
Принцип методики : Выполнение СТЭ позволяет снизить ВГД путем увеличения оттока водянистой влаги из передней камеры. Создается дополнительный путь оттока через отверстие в стенке склеры в субтеноново пространство.
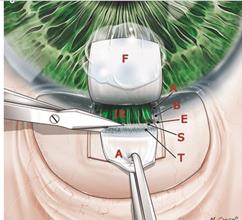
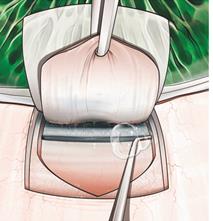
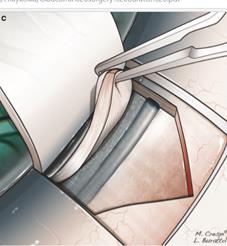
Ход операции. После освобождения эписклерального пространства производят разрез склеры на 2/3 ее толщины треугольной или прямоугольной формы, а затем отсепаровывают данный лоскут до прозрачной роговицы (рисунок 4) [1]. Таким образом формируется склеральный лоскут и склеральное ложе. Выполняется парацентез в верхне-височном квадрате (для восстановления в последующем передней камеры).
Рисунок 4- Формирование лоскута склеры
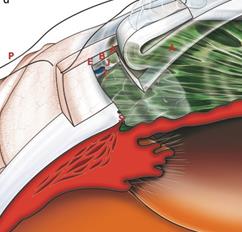
Рисунок 5- Удаление части склеры, шлеммова канала, трабекулярной сети
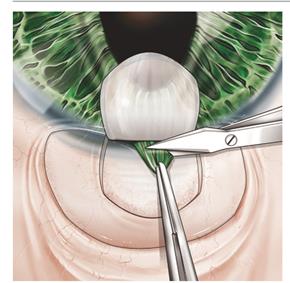
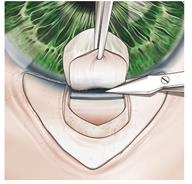
Выполняется базальная иридэктомия – удаление наружного края радужки с целью профилактики «выпадания» радужной оболочки из внутреннего склерального отверстия и формирования блока (рисунок 6) [1].
Рисунок 6 – Выполнение базальной иридэктомии
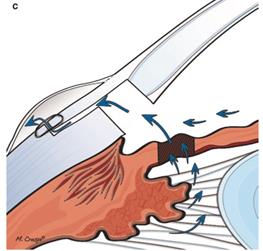
Склеральный лоскут укладывается на сформированное ложе и свободно фиксируется в дистальных углах.
Рисунок 7 – Новый путь оттока, сформированный после СТЭ
Существуют различные модификации данного оперативного вмешательства, например трепанотрабекулоэктомия и метод дополнительного глубокого вскрытия склеры [6,7].
Несмотря на то, что СТЭ является в настоящее время является «золотым стандартом» оперативного вмешательства при глаукоме, в послеоперационном периоде возможно развитие следующих осложнений [8,9]:
Тактика уменьшения количества послеоперационных осложнений
Наиболее высокий интерес вызывают методы, снижающие риск развития рубцевания в послеоперационном периоде. Так, для повышения эффективности СТЭ предлагается применение антиметаболитов, ингибирующих пролиферацию фибробластов: митомицина –С или 5-фторурацила. Обладая цитостастическим действием данные вещества вызывают такие осложнения, как роговичная эпителиопатия, хроническая гипотония и формирование наружной фистулы, в связи с чем их применение строго ограничено.
Некоторые авторы предлагают использование коллагеновых матриц и биоразлагаемых спейсеров для предотвращения образования рубцов. В 2010 году кафедрой офтальмологии ГУО «Белорусской медицинской академии последипломного образования» был предложен метод интра и экстрасклеральной амниопластики для снижения риска послеоперационного рубцевания и профилактики осложнений [10].
В результате поиска оперативных вмешательств, которые наряду с сохранением выраженного гипотензивного эффекта, были бы максимально свободны от недостатков и осложнений, присущих СТЭ, была предложена группа непроникающих фильтрационных вмешательств
Ⅲ НЕПРОНИКАЮЩИЕ ФИЛЬТРАЦИОННЫЕ ВМЕШАТЕЛЬСТВА
История : Принцип, лежащий в основе методов, был впервые предложен Циммерманом, который использовал термин ab externo trabeculectomy для его описания [11].
К непроникающим фильтрационным вмешательствам относятся: вискоканалостомия, непроникающая глубокая склерэктомия, каналопластика.
ⅢА ВИСКОКАНАЛОСТОМИЯ
История : Впервые был описан Робертом Стегманом [13]
Ход операции. Проходит в несколько этапов:
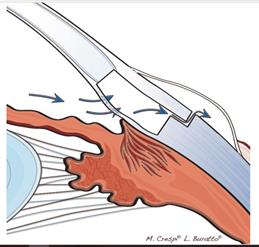
-идентификация и расширение с использованием вискоэластичного препарата шлеммова канала (рисунок 8) [1],
-удаление десцементовой оболочки (рисунок 9) [1],
-формирование интрасклерального «озера» для обеспечения оттока водянитой влаги. При этом хирург удаляет кусочек склеры, после чего остается только тонкий слой ткани, через который происходит фильтрация внутриглазной жидкости. (рисунок 10) [1].
В шлеммов канал вводится вискоэластик
Рисунок 10 – Удаление глубокого склерального лоскута. Поверхностный лоскут укладывается на ложе, прочно фиксируется – формируется склеральное озеро.
В результате оперативного вмешательства отток жидкости: передняя камера → «окно» в десцементовой оболочке → склеральное озеро → шлеммов канал. Вода, собранная в озере, может также стечь в нижнюю сосудистую оболочку, увеличивая увео-склеральный путь оттока
Рисунок 11- Отток жидкости после проведения вискоканалостомии
! Субконъюнктивального фильтрующего пузыря не образуется, т.к. верхняя склеральная пластинка плотно закрыта.
Хотя имеются данные об относительно низком гипотензивном эффекте этой операции, после нее отмечается меньшее количество осложнений по сравнению со СТЭ [13].
Ⅲ Б НЕПРОНИКАЮЩАЯ ГЛУБОКАЯ СКЛЕРЭКТОМИЯ
Рисунок 12 – Непроникающая глубокая склерэктомия
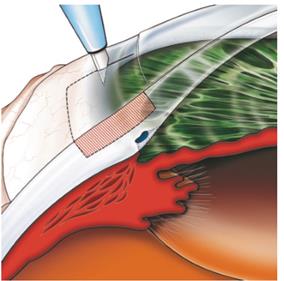
В результате оперативного вмешательства сформирован следующий новый путь оттока жидкости : передняя камера → интрасклеральное озеро → субтеноново пространство (рисунок 13) [1].
Рисунок 13 – Новый путь оттока ВГЖ из передней камеры после глубокой непроникающей склерэктомии
Ⅲ В КАНАЛОПЛАСТИКА
История : Первые сообщения о возможности канализации канала Шлемма с шелковым швом для частичной трабекулотомии опубликованы Р. Смитом в 1960 г. [16].
Прогресс в науке и технике позволил хирургам использовать гибкие микрокатетеры (iTrack, iScience Interventional, USA; Glaucolight, DORC, Netherlands) для атравматического хода по всей длине ШК с последующим стягиванием полипропиленовой нитью 10-0 для восстановления естественного оттока ВГЖ. Данная техника получила название «каналопластика» и используется в мире с 2008 г.
Ход операции. Каналопластика является модификацией метода вискоканалостомии. Однако при выполнении данного хирургического вмешательства после выделения глубокого и поверхностного склеральных локутов и выделения канала Шлемма:
1.Проводят дилатацию канала с помощью катетера;
2. В растянутом канале размещают постоянный шов
Преимущества непроникающих фильтрационных вмешательств.
Связаны с меньшей инвазивностью ( операции выполняются без проникновения в переднюю камеру):
-их использование позволяет расширить показания к раннему хирургическому лечению
-ниже риск развития осложнений
-повышают эффективность естественного пути оттока ВГЖ
Благодаря щадящей технике операции резко снизился риск возникновения интра- и послеоперационных макроперфорирующих осложнений, таких как гифема, резкое обмельчание передней камеры, экспульсивная геморрагия, отслойка сосудистой оболочки и т. д.
Недостатки непроникающих фильтрационных вмешательств :
— Эффективность операций непроникающего типа снижается в позднем послеоперационном периоде до 40-55% из-за рубцевания в зоне вновь сформированных путей.
-Часто в связи с низким гипотензивным эффектом требуется повторное проведение оперативного вмешательства.
-Эффективность операций при развитых стадиях глаукомы крайне низка.
-Техническая сложность операций:
А) Обязателен тщательный подбор пациентов с выполнением провокационной гониоскопии (для выполнения каналопластики)[17];
Б) В некоторых случаях оперативное вмешательство невозможно в связи с непроходимостью шлеммова канала [17 ];
— В связи с технической сложностью выполнения операций высок риск развития интраоперационных осложнений (например, перфорация ШК и миграция катетера в супрахориоидальное пространство, гифема).
Наличие большого числа способов повышения эффективности непроникающих операций свидетельствует об отсутствии удовлетворения хирургов их результатами. Поэтому исследования в этом направлении следует считать актуальными и перспективными.
Ⅳ ДРЕНАЖНЫЕ УСТРОЙСТВА
Историческая справка: Дренажная хирургия берет свое начало с работ M. Rollett, M. Moreau (1906) и A. Zorab (1912), предложивших имплантировать шелковую нить в склеротомическое отверстие для активации оттока ВГЖ из передней камеры под конъюнктиву. Этот принцип лег в основу дренажной хирургии. Первые дренажные устройства для глаукомы были предложены Molteno и Coll в 1968 году для лечения рефрактерной глаукомы
. Данное оперативное вмешательство показано при неэффективности или бесперспективности применения фистулизирующих операций.
Рисунок 14 – Дренажное устройство M. Ahmed
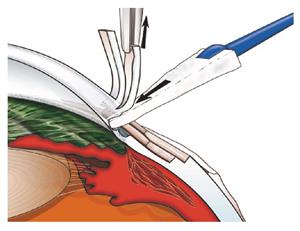
Ход операции. Корпус – резервуар дренажного устройства крепится эписклерально по меньшей мере в 8 мм от лимба (рисунок 15) [1]. Определяют оптимальную длину дренажной трубки, затем ее укорачивают (необходимо, чтобы она на 2-3 мм заходила в переднюю камеру). Для создания доступа в переднюю камеру параллельно плоскости радужки вводится игла (рисунок 16) [1]. Затем через данный доступ вводится трубка дренажного устройства (рисунок 17) [1].
Рисунок15 – Эписклеральная фиксация корпуса- резервуара дренажного устройства
Рисунок 16 – Введение в переднюю камеру иглы для создания доступа
Рисунок 17 – Введение в переднюю камеру силиконовой трубки дренажного устройства
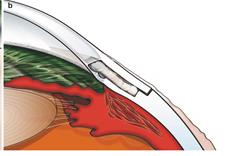
В результате оперативного вмешательства сформирован следующий отток жидкости : передняя камера → силиконовая трубка → эписклеральный клапан-резервуар → субтеноново пространство (рисунок 18) [1].
Рисунок 18 – Отток жидкости из передней камеры после имплантации дренажного устройства M. Ahmed
Преимущества дренажа M. Ahmed [19, 20]:
Недостатки дренажа M. Ahmed:
Высок риск как интраоперационных, так и послеоперационных осложнений [20]:
Преимущества микроинвазивной хирургии с внедрением микродренажей и стентов [23] :
Недостатки микроинвазивной хирургии с внедрением микродренажей и стентов :
Ⅴ ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ВРОЖДЕННОЙ ГЛАУКОМЫ
Гониотомия и трабекулотомия – операции выбора для лечения врожденной глаукомы.
Принцип: создание прямой связи между передней камерой и каналом Шлемма, минуя главное препятствие для фильтрации водянистой влаги, а именно трабекулы. Операции различаются с точки зрения доступа к шлеммову каналу: ab externo («снаружи») для трабекулотомии и ab interno («изнутри») для гониотомии.
Трабекулотомия.
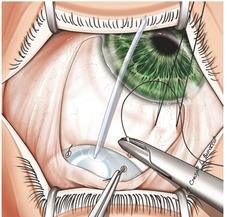
Ход операции. После формирования склерального лоскута выполняется радиальный разрез склеры в области наружной стенки шлеммова канала (рисунок 19) [1]. Разрез стенки трабекулы осуществляется с помощью трабекулотома (рисунок 20) [1].
Рисунок 19–Радиальный разрез склеры в области наружной стенки шлеммова канала.
Рисунок 20 – Выполнение разреза стенки трабекулы с помощью трабекулотома, введенного в шлеммов канал
Высок риск развития интра и послеоперационных осложнений:
Гониотомия.
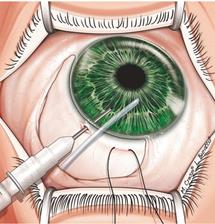
Ход операции. Принцип оперативного вмешательства аналогичен таковому при трабекулотомии. Однако доступ к трабекуле осуществляется непосредственно изнутри передней камеры. На роговицу помещается специальная гониолинза, позволяющая хирургу визуализировать трабекулярный аппарат угла передней камеры. Через парацентез в переднюю камеру вводится гониотомический интрумент или игла, наконечником инструмента трабекула удаляется (рисунок 21) [1].
Рисунок 21 – Гониотомия. Через парацентез в переднюю камеру введен гониотомический инструмент. Стрелкой показан ход движения инструмента при удалении трабекулы.
В связи с технической сложностью выполнения оперативного вмешательства возможны осложнения:
Высок риск возникновения таких ятрогенных осложнений как иридодиализ, циклодиализ
ЗАКЛЮЧЕНИЕ
Хирургическое лечение глаукомы показано при отсутствии гипотензивного эффекта от консервативной терапии и при невозможности или неэффективности проведения лазерной терапии.
В связи с высоким послеоперационным эффектом снижения ВГД «золотым стандартом» хирургического лечения первичной открытоугольной глаукомы остается СТЭ. Разработка неперфорирующих вмешательств позволяет сделать операции менее травматичными, повысить их безопасность и снизить процент осложнений, однако гипотензивный эффект часто бывает непродолжительным.
После оперативного лечения необходимо проведение регулярных исследований, оценивающих ВГД, состояние диска зрительного нерва и полей зрения, так как остается вероятность прогрессирования заболевания даже при нормальных значениях ВГД.
В связи с вышесказанным мы рекомендуем:
А) С целью раннего выявления глаукомы проходить профилактические осмотры у офтальмолога, особенно пациентам в возрасте старше 40 лет (согласно данным литературы заболевание поражает 15-25% всего населения в возрасте старше 40 лет).