симпато адреналовая система что это
Защитные функции симпатоадреналовой системы

По факту – это защитная конструкция, сложившаяся и закрепившаяся на генетическом уровне.
Рассмотрим особенности ее структуры, предназначение и прочие нюансы.
Общая информация
Симпатоадреналовая система (systema nervorum sympathicum) при активации через надпочечники обеспечивает оперативную адаптацию вещественного обмена, скорректированную на сублимацию энергии, обуславливает приспособленность организма к нарушениям гомеостаза, особенно в критических и экстренных ситуациях.
В физиологические опции САС входит коррекция многих функций. В случае развития патологий, активная фаза системы трансформируется, провоцируя реорганизацию некоторых процессов. Сильные и часто повторяющиеся изменения способствуют видоизменению регуляторных реакций физиологического плана в патогенетическую сферу стимуляции адаптационных заболеваний. Они вызывают нарушения в работе следующих систем: нервно-психической, сердечно-сосудистой, эндокринной и некоторых других.
Структура САС
Симпатико-адреналовая система включает в себя три основных узла:
Рассмотрим подробнее каждую из структур.
В этой части системы вырабатываются катехоламины, выброс которых из клеток происходит сразу же, при возникновении «стрессовой» или нестандартной ситуации (несвойственной обычному поведению организма). Проще говоря – это участок «моментальной реакции».
СНС (симпатическая нервная система)
Данное звено связывает внутренние и наружные органы (от кожного покрова до сердечной мышцы). СНС включает в себя нервные ответвления, связываемые между собой при помощи специального гормона (норадреналина). Следовательно, поступление катехоламинов дополнительно стимулирует СНС.
Главное предназначение рассматриваемого звена – объединение различных резервов организма на нивелирование неблагоприятного воздействующего фактора. Активная реакция симпатической нервной системы влияет на образование окислительных и восстановительных реакций, разрушение гликогенов и ликвидацию жиров.
При критических нагрузках физического плана СНС вырабатывает энергетический потенциал, требуемый для сокращения групп или отдельных мышц, способствуя их восстановлению и работоспособности, даже при максимальной утомляемости. Именно этот отдел отвечает за выведение молочной кислоты из печени, что позитивно влияет на активность организма и восстановление его энергии.
Кроме позитивного воздействия на восстановление энергии, СНС корректирует ресурсы среди разных органов.

Например, в случае необходимости выполняется передислокация кровяного потока между условной «рубашкой» и «центром» тела. В результате, сосуды мозга, печении, почек и сердца расширяются, что способствует притоку крови к особо важным элементам организма, посредством отбора ее от значимых органов. Производится, своего рода, пожертвование функционированием определенных частей, для сохранения жизни. Данная приспособленность обусловлена адаптацией механизмов, выработанной в результате процессов эволюции.
Мозговое наполнение надпочечников
Эта структура симпатоадреналовой системы вырабатывает адреналин (уникальное для организма вещество). Оно классифицируется, как гормон и катехоламин. Создается адреналин преимущественно в надпочечниках и ЦНС. Вещество мобилизует энергетические резервы организма и стабилизирует мембранные участки клеток.
Под воздействием этого гормона увеличивается энергетический потенциал мембран клетки с синхронным увеличением проникновения глюкозы. Силовые блоки (митохондрии) устраняют энергетические субстраты в максимально возможном количестве с дополнительным выбросом энергии.
Идентично с указанными процессами минимизируется впитывания мембран для токсических внедрений. Элементы приобретают устойчивость к воздействию электромагнитной направленности, ядам, радиации. Адреналин активно влияет на быструю трансформацию (структурно и физиологически) клеточных мембран, увеличивая жизнеспособность этих элементов. Отмечено, что мозговая субстанция надпочечников способна подавлять активацию злокачественных образований в ткани.
Прямые эффекты катехоламинов
Ключевым фактором, который позволяет определить реакцию какого-либо органа на адреномиметические вещества, является плотность и соотношение соответствующих рецепторов (α и β). Поскольку в гладкой мышечной системе бронхов присутствуют преимущественно адренорецепторы типа «бета2», норадреналин практически не способствует сопротивлению органов дыхания, выступая мощным дилататорами.
В кожных покровах, напротив, наблюдается наличие рецепторов «альфа». В связи с этим, адреналин способствует сужению этих частей, при этом изопреналин практически нейтрален. В скелетной мышечной группе наблюдаются представители обеих категорий, следовательно, активация одной из категорий рецепторов может вызывать сужение либо расширение сосудиков. При физиологической норме адреналин провоцирует второй вариант, а при высокой дозировке преобладает «альфа», что показывает сосудосуживающий эффект.
Конечная реакция
Этот фактор зависит от прямого воздействия и от компенсаторных гомеостатических конструкций. Например, прессорная атака стимуляторов «альфа» провоцирует возбуждение баррорецепторов аортовой дуги вкупе с каротидным синусом. В итоге, увеличивается парасимпатический тонус (рефлекторно), что приводит к снижению частоты сердечных сокращений.
Непрямое действие катехоламинов
Длительное время предполагалось, что эффекты адренергиков имеют только прямое стимулирование соответствующих рецепторов. Как оказалось впоследствии, воздействие многих некатехоламиновых включений фенилэтиламина нейтрализуется, снижается после снабжения кокаином или проявления хронической десимпатизации.
Зато, при аналогичных условиях, эффект норадреналина усиливается. Подобная схема позволяет предположить, что тирамин и его аналоги оказывают также непрямое действие. При этом происходит вытеснение адреналина из симпатических образований. Это приводит к воздействию на постсинаптический рецепторный узел, чем объясняется адренергический эффект тирамина и идентичных веществ:
Особенности
К самому известному способу суммарной оценки непрямого и прямого эффекта адренергических моделей относится сравнение кривых воздействия на конкретный орган до и после проведения резерпинизации. Если показатели идентичны между собой, препараты причисляют к веществам прямого воздействия (фенилэфрин и норадреналин). В случае нейтрализации эффектов, препараты относят к симпатомиметикам (непрямого действия). Типичный представитель – тирамин.
Также известны смешанные препараты, которым присущи обе функции. Для разных животных и органов оба действия от указанных средств могут значительно отличаться. У человека данное соотношение точно определяется не всегда. Норадреналин вызывает стимуляцию адренорецепторов типа α и β1, большинство симпатомиметиков преимущественно влияют на органы сердечнососудистой системы. Некатехоламиновые препараты, напротив, обладают сильным стимулирующим эффектом для рецепторов β2. Характерным представителем этой группы является эфедрин. Он способствует высвобождению норадреналина, при этом способен нейтрализовать бронховый спазм.
Симпатоадреналовая функция при физиологических состояниях
Главное предназначение САС – сублимация энергетических системных и клеточных запасов. Поэтому, мягкое физиологическое стимулирование позволяет создать некий дефицит энергии в тех частях организма, которые наиболее подвержены максимальным нагрузкам. Ответной реакцией на недостаток запасов является структурная гипертрофия. При этом увеличение в них синтеза белка способствует избежать энергетического истощения.
Например, в период наращивания массы мышц, участие симпатоадреналовой системы проявляется особенно заметно. Для роста той или иной мышечной группы требуется явное утомление после тренировки. Именно САС дает возможность мобилизовать энергетические запасы с некоторым физиологическим опустошением резервов мышцы. Сигналы об истощении резервов поступают на рецепторы клеточного ядра, провоцируя активацию генов, отвечающих за белковый синтез. В итоге, мышцы гипертрофируются, а масса их увеличивается.
СИМПАТОАДРЕНАЛОВАЯ СИСТЕМА
Симпатоадреналовая система [лат. (systema nervorum) sympathicum симпатическая нервная система + adrenalis надпочечный] — одна из систем регуляции гомеостаза. Симпатоадреналовая система состоит из нервного звена (см. Вегетативная нервная система) и гормонального, включающего в себя гормоны, синтезируемые мозговым веществом надпочечников (см.), и параганглиями (см.),— адреналин (см.), норадреналин (см.) и дофамин (см. Катехоламины).
Объединение симпатической нервной системы и хромаффинных клеток мозгового вещества надпочечников и параганглиев в единое целое оправдано с морфологической и физиологической позиций. Хромаффинные клетки параганглиев и надпочечников иннервируются холинергическими волокнами клеток боковых рогов спинного мозга (см.), в силу чего секретируемых ими катехоламины, преимущественно адреналин, представляют собой гуморальный эквивалент постганглионарных нервных волокон, продуцирующих местнодействующий норадреналин. При достаточно сильных воздействиях Симпатоадреналовая система реагирует генерализованно, двумя звеньями, обусловливая возникновение в организме сдвигов, известных, по У. Кеннону, как реакция борьбы и бегства. Однако при менее интенсивных воздействиях возможно преимущественное вовлечение в ответную реакцию того или иного звена С. с. или даже отдельных частей ее нервного звена. Причиной этого может быть различие порогов возбудимости разных постганглионарных структур. Быстрая реакция С. с. на изменение какого-либо параметра внутренней среды организма (см.) и быстрое возникновение эффектов активации С. с. обеспечивает возможность постоянной «подстройки» внутренней среды организма в соответствии с требованиями момента. Важной особенностью С. с. является изменение ее активности еще до появления реальных нарушений гомеостаза (см.), что ослабляет их тяжесть для организма. Это обусловлено наличием разнообразных, в т. ч. корковых и гипоталамических, афферентных входов в С. с. на уровне мозгового ствола (см. Головной мозг). Совокупность реакций организма на изменения окружающей или внутренней среды (или лишь на угрозу таких изменений) независимо от специфики действующего фактора во многом определяется сочетанием прямых и опосредованных через другие системы (гл. обр. через эндокринную и сердечно-сосудистую системы) эффектов катехоламинов.
Библиография: Орбели Л. А. Избранные труды, т. 1—5, М.— Л., 1961 —1968; Смиттен Н. А. Симпатоадреналовая система в фило- и онтогенезе позвоночных, М., 1972, библиогр.; Cannon W. В. The wisdom of the body, N. Y., 1939; Landsberg L. Catecholamines and the sympathoadrenal system, в кн.: The year in endocrinol., 1975— 1976, ed. by S. H. Ingbar, p. 177, N. Y.— L., 1976, bibliogr.
Симпато-адреналовые кризы (панические атаки)
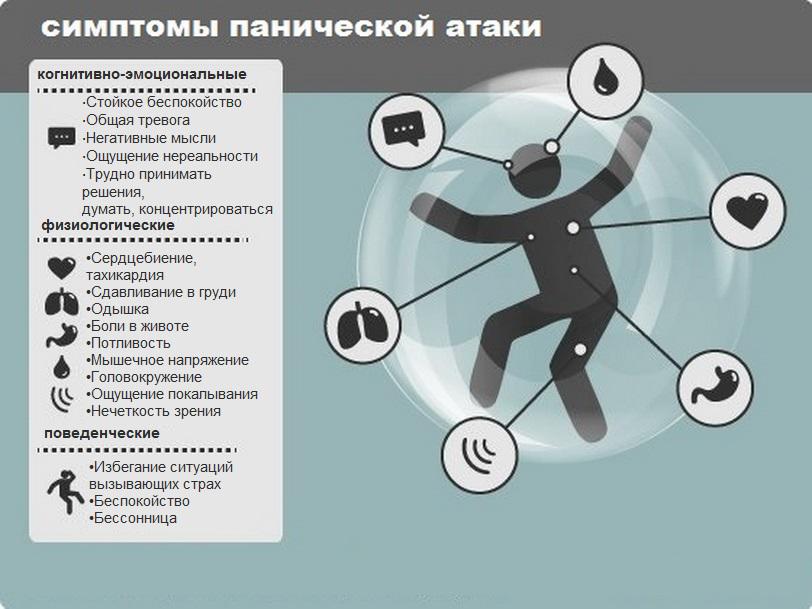
Это неуправляемый, нерациональный, изматывающий и очень интенсивный приступ паники и тревоги, который сопровождается соматическими и психологическими симптомами. Состояние может воздействовать на когнитивные способности и поведенческие реакции.
Они довольно часто встречаются в популяции, примерно в 5% случаев и, что самое интересное, им подвержены молодые работоспособные граждане от 20 до 40 лет, причем женщины страдают этим недугом в 3 раза чаще.
Перед тем, как переходить к проявлению заболевания, обратимся к небольшой классификации для лучшего понимания.
Выделяют 3 типа панических атак.
Немного о симптомах и патогенезе заболевания.
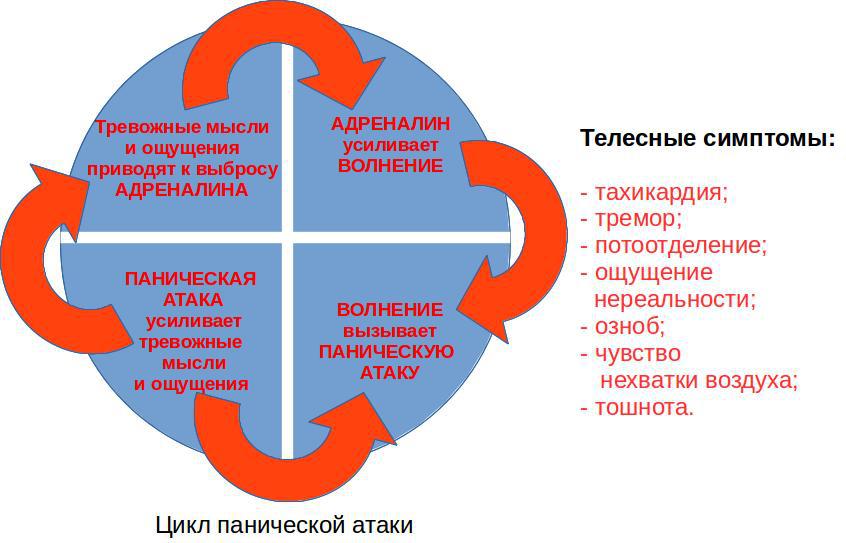
Приступы носят ярко выраженный соматический, т.е. телесный и физический характер, по своим симптомам очень напоминающий классический сердечный приступ сопровождающийся страхом смерти и пр., поэтому пациенты могут предполагать у себя патологию сердца (отсюда и одно из названий – сердечный невроз). Однако, даже самые сильные проявления атак, следствие дисбаланса нервной и гуморальной систем. Основным механизмом развития криза является активация симпатической нервной системы и мощный выброс «гормона стресса» адреналина – отсюда происходит еще одно название «симпато-адреналовый криз».
Так как часто вовлекается психика, то могут наблюдаться ее кратковременные расстройства: человеку кажется, что все это происходит не с ним, возникает ощущение нереальности происходящего, отчуждаются собственные психические процессы, появляется страх перестать контролировать свое поведение – такие процессы называются дереализация и деперсонализация.
Клиническая картина и ее выраженность имеет широкий диапазон и очень варьируется, существует даже так называемая « безстраховая» форма панической атаки или «паника без паники», когда на первый план выходят именно физические нарушения.
Так же, как и симптомы, изменчива длительность приступов. Они могут появляться на несколько минут, а могут длиться часами, но в среднем укладываются в 15 – 30 минут. Частота таких приступов тоже не имеет четкой зависимости: у кого-то это 1 раз в месяц, у кого-то 3 раза в день.
Как таковые причины панических атак до конца не выяснены, вот некоторые из возможных:
Есть интересное мнение, что недугу чаще всего подвержены люди, живущие в городах, интеллектуально развитые, тревожные и ответственные от природы. Практически не встречаются люди с вегетативными кризами среди жителей отдаленных районов и деревень.
Диагностика.
Как осуществляется лечение панических атак в Усть-Каменогорске?
Для восстановления баланса процессов возбуждения и торможения в нервной системе используется иглорефлексотерапия, магнито- и лазеротерапия. Хорошие результаты в лечении панических атак дает транскраниальная стимуляция головного мозга.
Если причина связана с нарушением гемодинамики на уровне брахиоцефальных артерий, то применяется мануальная терапия, массаж, вытяжение позвоночника.
Симпато адреналовая система что это
СОСТОЯНИЕ ПРЕССОРНЫХ И ДЕПРЕССОРНЫХ НЕЙРОГУМОРАЛЬНЫХ СУБСТАНЦИЙ И ФАКТОРЫ ПРОГРЕССИРОВАНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Бобров В.А., Жаринов О.Й., Салам Сааид
Кафедра кардиологии и функциональной диагностики Киевской медицинской академии последипломного образования, Украинский НИИ кардиологии им. Н.Д. Стражеско,
Ключевые слова: хроническая сердечная недостаточность, патогенез, нейрогуморальная система, ренин-ангиотензиновая система, симпато-адреналовая система, альдостерон, эндотелин, предсердный натрийуретический фактор
Хроническая сердечная недостаточность (ХСН) является наиболее частым и серьёзным осложнением заболеваний сердечно-сосудистой системы. ХСН приводит к потере трудоспособности, значительному уменьшению продолжительности жизни больных и остаётся важнейшей проблемой здравоохранения в развитых странах. Несмотря на применение современных лекарственных препаратов, направленных на продление жизни больных с ХСН, около 60 % мужчин и 45 % женщин умирают в течение 5 лет после появления первых клинических симптомов ХСН.
Нейрогуморальная система вовлекается в патологический процесс уже на ранних этапах ХСН. Ее активация, с одной стороны, способствует компенсации сердечной деятельности в ответ на снижение сердечного выброса (СВ), с другой – стимулирует прогрессирование декомпенсации и развитие необратимых изменений в организме. Активация нейрогуморальной системы является важнейшим звеном патогенеза ХСН, маркером наличия и тяжести заболевания, мишенью для терапевтических воздействий. Цель настоящего обзора – представить современное понимание роли нейрогуморальных изменений в развитии ХСН, перспективные возможности диагностики и лечения этого клинического синдрома.
Медиаторы нейрогуморальной системы можно разделить на три группы: вазоконстрикторы, вазодилататоры и факторы роста (таблица) [20]. При развитии ХСН происходят существенные сдвиги баланса воздействия этих медиаторов с преобладанием вазоконстрикции.
Таблица. Медиаторы нейрогуморальной системы при ХСН
Катехоламины: адреналин, норадреналин
Антидиуретический гормон
Предсердный натрийуретический фактор
Каликреин-кининовая система: брадикинин, NO,
эндотелийзависимый фактор гиперполяризации
Фактор некроза опухоли (TNF a )
Свободные радикалы
Факторы роста играют определенную роль в патогенезе ХСН, контролируя механизмы запуска процессов апоптоза (программируемой биологической гибели) кардиомиоцитов и ремоделирования миокарда и сосудов, однако их роль в патогенезе ХСН и диагностическое значение недостаточно изучены [30].
Определение концентрации ряда нейрогормонов, участвующих в патогенезе заболевания, позволяет не только определять степень тяжести ХСН и прогноз больных, но и устанавливать возможные мишени, на какие целесообразно воздействовать при лечении ХСН. Остановимся подробнее на состоянии отдельных звеньев нейрогуморальной системы при ХСН.
Активация ренин-ангиотензиновой системы
Сам по себе АТ I не имеет значительного биологического эффекта, однако в результате отщепления двух аминокислот под влиянием различных ферментов (ангиотензин-превращающий фермент (АПФ), химаза, тканевой активатор плазминогена (ТАП), тонин, катепсин G), преимущественно в легких, превращается в сильно действующее вещество – ангиотензин II (АТ II). Другой путь образования АТ II – непосредственно из ангиотензиногена под влиянием ТАП, катепсина G, тонина и эластазы, минуя АТ I. АТ II в дальнейшем, путём отщепления аминокислот, под действием эндопептидаз и аминопептидаз, преобразуется в менее активные вещества – АТ III и AT IV, которые также играют определенную роль в патогенезе ХСН. АТ III оказывает влияние на синтез альдостерона (АС), а АТ IV регулирует почечный кровоток [13,14].
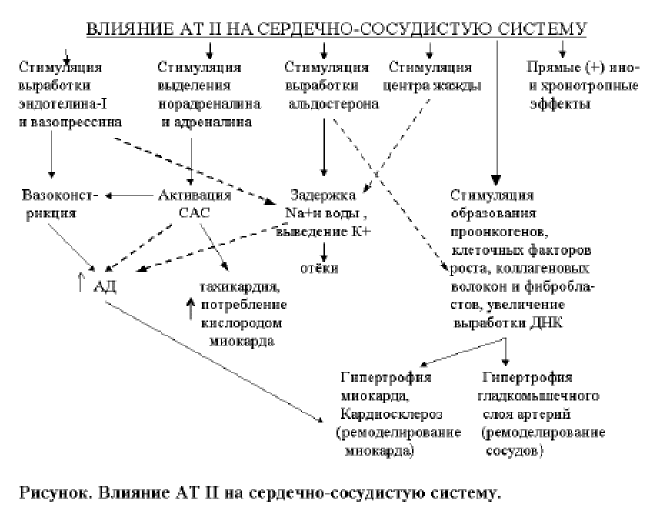
Основной физиологический эффект AT II, повышение АД, связан с сужением сосудов (преимушественно артериол), стимуляцией секреции АС и катехоламинов надпочечниками. АТ II оказывает также влияние на центральные механизмы регуляции АД посредством изменения уровня секреции адренокортикотропного и антидиуретического гормонов, а также активности центральных адренергических механизмов [9] (рисунок).
Следует отметить, что АТ II функционирует и в норме, но при ХСН в условиях снижения активности его антагонистов преобладает отрицательное влияние АТ II на органы и системы.
Влияние ренин-ангиотензиновой системы (РАС) на функцию органов-мишеней, среди которых наиболее важными являются сердце, сосуды, надпочечники и почки, опосредуется специфическими рецепторами, которые разделяются на несколько типов [2,13].
Рецепторы первого типа (АТ 1 ) выявляются в гладкомышечных и соединительнотканных клетках артериол, легких, мозга и мозгового вещества почек. В старческом возрасте количество этих рецепторов оказывается господствующим. Через эти рецепторы реализуется ряд эффектов АТ II, которые являются компенсаторными, однако способствуют прогрессированию ХСН (инотропная стимуляция, гипертрофия миокарда, вазоконстрикция) [2,13,14,32].
Через АТ 1 и АТ 2 действует АТ II, в меньшей степени – АТ III. Рецепторы третьего типа (АТ 3 ) обнаружены на мембранах нейронов; функция их неизвестна. Эти рецепторы обладают сродством лишь к АТ II. Выделяют также рецепторы четвёртого типа (АТ 4 ). Эти рецепторы располагаются на мембранах клеток головного мозга, почек, сердца и эпителиальных тканей. В головном мозге эти рецепторы по-видимому опосредуют познавательные функции, а в почках регулируют кровоток. Другая предполагаемая функция АТ 4 – регуляция роста клеток. АТ 4 взаимодействуют только с АТ IV [13].
АТ II вырабатывается не только в крови (циркуляторная, нейроэндокринная РАС), но и в органах-мишенях (тканевая РАС) как внутри, так и вне клетки. Внутриклеточное образование АТ II влияет на функцию внутриклеточных органелл (интракринная стимуляция). Внеклеточный синтез AT II может происходить на мембране клетки, стимулировать функцию соседних клеток (паракринная стимуляция) или влияя на функцию тех клеток, на мембранах которых он образовался (аутокринная стимуляция) [14,15,32,41].
Для циркуляторной РАС, как системы «быстрого реагирования», характерны кратковременные эффекты контроля системного и перфузионного давления и электролитного гомеостаза (положительный ино-, хронотропный и аритмогенный эффекты, задержка натрия и воды почками, вазоконстрикция) [15]. Чрезмерная активность циркуляторной РАС, наблюдаемая у больных ХСН при декомпенсации, как правило, возвращается к исходному уровню после достижения пациентами состояния клинико-гемодинамической компенсации в условиях коррекции почечного перфузионного давления [26]. В то же время при ХСН происходит активация тканевой РАС, с которой связаны долговременные процессы развития гипертрофии миокарда и гладкой мускулатуры сосудов, пролиферации соединительной ткани и внутриклубочковой гипертензии [15].
Под действием эндопептидаз из АТ I также образуется АТ (1-7), который обладает важными свойствами, отличными от АТ II. Прежде всего, это вазодилатирующее и антипролиферативное действие, опосредуемое стимуляцией образования эндотелием NO и некоторых простагландинов. Кроме того, АТ (1-7) усиливает выделение воды и натрия почками без изменения их кровотока. Выработка АТ (1-7) увеличивается при угнетении образования АТ II и накоплении АТ I в крови и тканях, в частности, при применении ингибиторов АПФ. Предполагают, что в патогенезе ХСН играет роль не только усиленное образование АТ II, но и уменьшение выработки или активности АТ (1-7), который, обеспечивая обратную связь, играет важную роль в регуляции прессорного и белковосинтетического эффектов АТ II [2,13].
Таким образом активация РАС играет ключевую роль в прогрессировании ХСН. Прежде всего это связано с активацией AT II, которая отрицательно сказывается на течении заболевания и, в свою очередь, способствует синтезу различных вазоактивных веществ (альдостерон, норадреналин, эндотелин и вазопрессин), в свою очередь неблагоприятно влияющих на прогноз больных. Активность ренина и уровень АТ II в плазме могут служить диагностическими критериями тяжести ХСН.
Увеличение концентрации АС в крови при ХСН вызывает задержку натрия и воды почками при одновременном повышении экскреции калия, активно влияет на образование коллагена и состояние барорефлекторного аппарата. Альдостероновые рецепторы имеются не только в почках, но и в сердце и периферических сосудах. Циркулирующий и тканевой АС, действуя на рецепторы кардиомицитов, активирует фибробласты, что приводит к увеличению синтеза коллагена, росту коллагенового матрикса и к развитию интерстициального миокардиального фиброза, а это в свою очередь повышает жёсткость левого желудочка, стимулирует диастолическую дисфункцию и прогрессирование ХСН.
АС синтезируется не только под влиянием АТ II, но и разнообразными другими путями (адренокортикотропный гормон, гиперкалиемия и др.) [12]. Его образованию способствует гипоксия тканей, которая развивается в условиях снижения СВ, является стрессовым фактором и активизирует стероидогенез в надпочечниках. При уменьшении минутного объема кровотока (МОК) и объема циркулирующей крови (ОЦК) происходит раздражение объёмных и осмотических рецепторов сердца и сосудов, что стимулирует секрецию АС. Повышение венозного давления путём раздражения барорецепторов правого предсердия и полых вен также может способствовать увеличению образования АС и приводить к перемещению внутрисосудистого Na + и воды в межклеточные пространства. Существенное снижение ОЦК на фоне уменьшения СВ способствует уменьшению внутрисосудистого объёма и приводит к гиперсекреции АС. Так, у больных с ХСН гиперальдостеронизм наиболее выражен при ослаблении функции правого желудочка и венозной гипертензии [11,12].
Важную роль в поддержании концентрации АС в крови играет функциональное состояние печени, где происходит его метаболизм. Замедление метаболизма АС в функционально неполноценной печени при ХСН способствует повышению его уровня в организме. Поэтому вторичный гиперальдостеронизм при ХСН обусловлен не только увеличением секреции, но и нарушениями его инактивации [11].
Таким образом, АТ II является одним из целого ряда факторов, влияющих на активацию синтеза АС и его концентрацию в крови. В то же время при ХСН вазоконстрикция, выброс катехоламинов, секреция вазопрессина – не менее важные эффекты активации РАС, чем гиперальдостеронизм.
Инактивация брадикининовой системы
Помимо стимуляции образования АТ II, другим важным эффектом АПФ (кининазы II, располагающейся в основном на мембранах эндотелиальных клеток) является расшепление до неактивных пептидов мощного эндогенного сосудорасширяющего вещества брадикинина (БК). Последний играет важную роль в процессах контроля АД и регуляции функции эндотелия, который в значительной степени определяет сосудистый тонус путём локального синтеза и высвобождения вазодилататорных и вазоконстрикторных веществ.
БК образуется из брадикининогена под влиянием калликреина, который циркулирует в крови или высвобождается местно из эндотелиальных клеток. БК может снижать АД за счёт дилатации резистивных сосудов, увеличивать скорость местного кровотока, повышать их проницаемость, инициировать болевую реакцию. БК также оказывает натрийуретический и диуретический эффекты. За счёт влияния на состояние сосудистой стенки и непосредственного действия на сердце БК расценивается как фактор сопряжения ряда механизмов регуляции кровообращения. Возможно, кинины осуществляют функциональную связь между тонусом сосудистой стенки и реологическими свойствами текущей по сосудам крови [6,7,9].
БК является мощным стимулятором высвобождения трёх эндотелийзависимых раслабляющих факторов: NO, эндотелийзависимого фактора гиперполяризации (ЭФГ) и простациклина, выполняя таким образом важную роль в регуляции тонуса сосудистой стенки [4,6,7,23,25,39]. Стимуляция эндотелиальных клеток брадикинином регулируется связанным с их мембранами АПФ.
Эндотелиальный релаксирующий фактор, идентичный окиси азота, образуется в эндотелиальных клетках из L-аргинина под действием синтетазы NO. Период полужизни NO составляет менее 5 с, следовательно, она действует локально. NO тормозит деятельность сократительного аппарата гладкомышечных клеток (ГМК) сосудов; стимулируя растворимую гуаниловую циклазу, способствует образованию в ГМК сосудов циклического гуанозин-3’,5’-монофосфата, вызывающего расширение сосудов [4,9,10]. NO также тормозит адгезию тромбоцитов и лейкоцитов к эндотелиальному покрову и пролиферацию ГМК сосудов, угнетает образование эндотелина. NO является физиологическим антагонистом АТ II, улучшает натрийурез и увеличивает экскрецию ренина [4,10].
NO образуется как в базальном состоянии, так и в ответ на стимуляцию брадикинином и другими катехоламинами. При ХСН базальная секреция NO не изменяется, в то время как стимулированная секреция нарушается, особенно в резистивных сосудах [10].
Простациклин образуется в основном эндотелиальными клетками. Он активирует аденилатциклазу ГМК сосудов, увеличивая образование циклического аденозинмонофосфата, расслабляющий эффект которого усиливает вазодилятацию, вызываемую NO. Более того, простациклин обладает синергизмом с NO в отношении торможения агрегации тромбоцитов [4].
Следует принимать во внимание тот факт, что при развитии ХСН и ремоделировании сосудов нарушается функция эндотелия. На фоне эндотелиальной дисфункции нарушается вазодилатация, стимулированная БК, страдает образование вазодилатирующих веществ.
Хотя точная роль брадикининовой системы при ХСН неизвестна, есть доказательства, что по крайней мере некоторые из положительных воздействий ингибиторов АПФ на ремоделирование желудочков могут быть опосредованы увеличением концентрации БК в крови [30].
Установлено, что катехоламины, АТ II, свободные радикалы, гипоксия усиливают продукцию ЭТ-1 [8]. Концентрация ЭТ-1 в крови повышается при ХСН и является возможным маркером повреждения клеток эндотелия и/или миокарда [34,36].
Кроме непосредственных эффектов сужения артерий скелетных мышц, почек, легких, ЭТ-1 имеет положительное митогенное свойство, обладает антидиуретическим действием, усиливает периферическую и центральную симпатическую активацию, способствует действию вазоконстрикторных нейроэндокринных механизмов при ХСН вследствие стимуляции продукции ренина, АТ II, АС и адреналина. К тому же в пороговых и субпорговых концентрациях ЭТ-1 усиливает контрактильный ответ миокарда и сосудов на другие вазоконстрикторы, такие как норадреналин и серотонин [36].
Активация симпато-адреналовой системы
Симпато-адреналовая система (САС) активируется в результате снижения ударного объема, СВ, АД и активации барорецепторов в предсердиях, а также гиперчуствительности барорецепторов, расположенных в области дуги аорты и каротидного синуса. Активация САС усиливает сократимость миокарда и переводит сердце на более интенсивный режим работы [1,11,27].
Гиперактивация САС и спазм артериол усиливают недостаток кровоснабжения органов и тканей. Прогрессирующее повышение систолического сопротивления (постнагрузка) ведёт к увеличению напряжения и уменьшению укорочения миокарда желудочков, что в свою очередь вызывает увеличение потребности миокарда в кислороде. При этом ухудшаются условия кровоснабжения субэндокардиальных слоев, нарастает дефицит кровоснабжения миокарда, что способствует возникновению локальных нарушений его сократимости и усугублению ХСН [22,35]. Тахикардия, возникшая как компенсаторный механизм для поддержания СВ и АД, увеличивает потребность сердечной мышцы в кислороде и быстро истощает энергетические запасы миокарда, усугубляя нарушения сократимости и приводя к дальнейшему снижению СВ.
САС действует на миокард и непосредственно [19,22,35], что обусловлено чрезмерной стимуляцией катехоламинами адренорецепторов миокарда и активацией медленных кальциевых каналов. В дальнейшем возникает перегрузка митохондрий кальцием, что приводит к замедлению процессов рефосфорилирования аденозиндифосфата, истощению запасов креатинфосфата и аденозинтрифосфата с дальнейшим нарушением процессов сокращения и расслабления миокарда. В результате активации фосфолипаз и протеаз разрушается клеточная мембрана, что вместе с дефицитом энергии приводит к гибели кардиомиоцитов.
Активация САС и ишемия играют также ключевую роль в генезе желудочковых аритмий путём усиления нарушений автоматизма, триггерной активации и обратного входа возбуждения в поражённом миокарде [22].
Итак, последствия гиперактивации САС при ХСН можно представить следующим образом: дисфункция и гибель кардиомиоцитов (некроз, апоптоз); ухудшение гемодинамики (снижение плотности и сродства (-рецепторов); гипертрофия миокарда; увеличение частоты сердечных сокращений; провокация ишемии миокарда (тахикардия, гипертрофия, вазоконстрикция); аритмогенез (ухудшение гемодинамики, гипертрофия, гипоксия) [16].
Уровень норадреналина в крови увеличивается при ХСН, отражает нарастание дисфункции левого желудочка и функционального класса ХСН. Определение норадреналина плазмы может быть лучшем ориентиром тяжести ХСН, чем многие гемодинамические параметры [27].
Активация антидиуретического гормона
Увеличение венозного возврата к сердцу и ОЦК обусловленно также компенсаторным увеличением продукции в ядрах гипоталамуса антидиуретического гормона (АДГ, вазопрессина). Это происходит вследствие стимуляции артериальных барорецепторов, повышения активности САС и РАС, а также в связи с повышением осмолярности плазмы из-за увеличения реабсорбции натрия в почечных канальцах под влиянием АС.
В начальный период ХСН повышение активности АДГ имеет адаптационно-компенсаторное значение. Гиперпродукция АДГ, с одной стороны, регулирует скорость клубочковой фильтрации и усиливает реабсорбцию воды на уровне дистальных канальцев и собирательных трубочек, что приводит к задержке жидкости в сосудистом русле и тем самым к увеличению ОЦК, преднагрузки и СВ; с другой стороны способствует артериальной и венозной вазоконстрикции [11]. АДГ также снижает скорость поглощения кислорода миокардом, может индуцировать коронарную вазоконстрикцию и тем самым снижать интенсивность метаболических процессов в миокарде [11].
Повышение общего периферического сосудистого сопротивления под влиянием АДГ происходит из-за задержки Nа + и воды в мышечных клетках артерий, отёка стенок и сужения просвета сосудов, ограничения расширительного резерва, повышения сосудистой реактивности к катехоламинам. Более того, АДГ потенциирует вазоконстрикторные эффекты АТ II и стимуляцию САС. В свою очередь активация САС и РАС усиливают вазоконстрикторный эффект АДГ [18].
АДГ обладает также выраженным отрицательным хроно- и инотропным действием на сердце. Взаимодействие барорецепторов и АДГ повышает активность блуждающего нерва и снижает активность периферических симпатических нервов, что проявляется смягчением прямого вазоконстрикторного эффекта, но необходимо учесть возможность потенциирования АДГ реакции ГМК сосудов на норадреналин [18], что взаимосвязано с прямым угнетением симпатической активности.
Активация предсердного натриуретического фактора
Ещё на ранних этапах развития ХСН активируется секреция предсердного натрийуретического фактора (ПНУФ), который вырабатывается в эндокринных клетках предсердий. Секреция ПНУФ регулируется внутрипредсердным давлением и растяжением предсердий, причём максимальная концентрация ПНУФ в плазме наблюдается у больных со значительным нарушением сократительной функции левого желудочка и патологией митрального клапана.
В крови ПНУФ с помощью циклического гуанозинмонофосфата взаимодействует со специфическими рецепторами, которые находятся на мембране клеток почечного эпителия, ГМК артерий, в коре надпочечников и гипофиза, а также в легких, печени и тонком кишечнике, и вызывает разнообразные физиологические эффекты [3,11].
ПНУФ уменьшает секрецию ренина, снижает секрецию АС, происходящую через стимуляцию АТ II и аденокортикотропного гормона в клетках клубочковой зоны коры надпочечников. Кроме того уменьшается образование и угнетается активность АДГ в органах-мишенях, подавляются некоторые эффекты АТ II (увеличение реабсорбции Na + и воды, замедление клубочковой фильтрации). По действию на органы-мишени ПНУФ является антагонистом РАС и в норме находится в равновесии с этой системой [11].
Действие ПНУФ на различные структуры почек вызывает быстрый и сильный диурез и натрийурез вследствие его релаксирующего действия на сосуды почек, увеличения кровотока и плазмотока, а также в результате непосредственного влияния на почечные канальцы собирательных трубочек, что способствует снижению интенсивности реабсорбции Na + и воды [3]. ПНУФ оказывает выраженное спазмолитическое действие на ГМК сосудов, в связи с чем снижается систолическое АД, а также стимулирует дилатацию коронарных артерий, причем без дополнительного использования энергии, тогда как для процессов вазодилатации необходим определённый уровень энергозатрат [21].
Считают, что у больных ХСН ПНУФ улучшает сократительную функцию миокарда и увеличивает СВ не только в связи с уменьшением сопротивления периферических сосудов (уменьшение постнагрузки на миокард), но и в связи с уменьшением преднагрузки при сохранении адекватного венозного возврата к сердцу. Кроме того, не исключается также прямой инотропный эффект ПНУФ на диастолическую функцию желудочков [3].
При ХСН с увеличением давления в предсердиях и их растяжением, вследствие компенсаторного увеличения венозного возврата к сердцу, наблюдается компенсаторное повышение продукции ПНУФ в 4-6 раз по сравнению с нормой, что противодействует задержке Na + в организме и активации РАС. Однако по мере прогрессирования ХСН ПНУФ теряет компенсаторную роль. Истощаются эндокринные клетки предсердий и, по-видимому, играет роль процесс десенсибилизации: из-за повышенного содержания ПНУФ уменьшается количество свободных рецепторов на клеточных мембранах органов-мишеней, вследствие чего ослабляется реакция на ПНУФ. В то же время активация РАС, САС и ЭТ становится более выраженной, что способствует стабилизации сиптоматики ХСН [3].
Так как гиперпродукция ПНУФ начинается уже на ранней стадии развития ХСН, ПНУФ – единственный нейрогуморальный медиатор, содержание которого рассматривается в рекомендациях по диагностике ХСН Европейского общества кардиологов как возможный диагностический критерий наличия бессимптомной дисфункции миокарда [31].
Нейрогуморальные аспекты лечения ХСН
Цель лечения больных с ХСН заключается не только в уменьшении симптомов заболевания и улучшении качества жизни, но и в продлении жизни больных путём коррекции структурных нарушений сердца и естественного течения ХСН. Важнейшая предпосылка решения этой задачи – снижение активности нейрогуморальной системы.
Важнейшим следствием глубокого изучения нейрогуморальных механизмов прогрессирования ХСН стало появление и дальнейшая разработка медикаментозных средств, которые снижают активность отдельных звеньев нейрогуморальной системы и благодаря этому способны замедлять прогрессирование заболевания. Ведущее место в современном патогенетическом лечении ХСН заняли препараты, блокирующие РАС на различных уровнях. Прежде всего, это ингибиторы АПФ, блокирующие важнейший путь образования АТ II и способствующие увеличению концентрации в плазме БК и NO. Все большее внимание привлекают антагонисты рецепторов АТ II первого типа, обеспечивающие наиболее полную блокаду отрицательных биологических эффектов АТ I I. Возможно, дополнительный эффект обеспечит сочетание препаратов этих двух групп. В настоящее время в эксперименте изучаются также ингибиторы синтеза/высвобождения ренина, которые теоретически представляются лучшими средствами блокады РАС при ХСН. Блокада AT II также способствует уменьшению синтеза норадреналина, ЭТ-1, АДГ и АС.
Подавление эффектов АС с помощью его антагонистов либо антагонистов рецепторов АС, не только уменьшает задержку Nа + и воды почками, но и уменьшает образование соединительной ткани и фиброза в миокарде и сосудов, и таким образом замедлить процессы их ремоделирования. Антагонисты АС имеют самостоятельное значение в лечении рефрактерного отечного синдрома при ХСН. Однако их место в терапии других клинических форм ХСН до конца не установлено.
В настоящее время в эксперименте изучаются также различные препараты, влияющие на рецепторы ЭТ, в частности блокаторы ЭТ А рецепторов и агонисты ЭТ В рецепторов.