семаглутид что это такое
СЕМАГЛУТИД (SEMAGLUTIDE) ОПИСАНИЕ
Фармакологическое действие
Семаглутид является агонистом рецепторов ГИП-1 (ГИП-1Р), произведённым методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae с последующей очисткой.
Семаглутид представляет собой аналог ГПП-1, имеющий 94% гомологичности с человеческим ГПП-1. Семаглутид действует как агонист ГПП-1Р, который селективно связывается и активирует ГИП-1Р. ГПП-1Р служит мишенью для нативного ГИП-1.
ГИП-1 является физиологическим гормоном, оказывающим сразу несколько эффектов на регуляцию концентрации глюкозы и аппетит, а также на CCC. Влияние на концентрацию глюкозы и аппетит специфически опосредовано ГИП-1Р, а расположенными в поджелудочной железе и головном мозге. Фармакологические концентрации семаглутида снижают концентрацию глюкозы крови и массу тела посредством сочетания эффектов, описанных ниже. ГИЙ-1Р представлены также в специфических областях сердца, сосудов, иммунной системы и почек, где их активация может оказывать сердечно-сосудистые и микроциркуляторные эффекты.
В отличие от нативного ГПП-1, продлённый T 1/2 семаглутида (около 1 недели) позволяет применять его п/к 1 раз в неделю. Связывание с альбумином является основным механизмом длительного действия семаглутида, что приводит к снижению выведения его почками и защищает от метаболического распада. Кроме того, семаглутид стабилен в отношении расщепления ферментом дипептидилпептидазой-4. Семаглутид снижает концентрацию глюкозы крови посредством глюкозозависимых стимуляции секреции инсулина и подавления секреции глюкагона. Таким образом, при повышении концентрации глюкозы крови происходит стимуляция секреции инсулина и подавление секреции глюкагона. Механизм снижения уровня гликемии включает также небольшую задержку опорожнения желудка в ранней постпрандиальной фазе. Во время гипогликемии семаглутид уменьшает секрецию инсулина и не снижает секрецию глюкагона.
Семаглутид снижает общую массу тела и массу жировой ткани, уменьшая потребление энергии. Данный механизм затрагивает общее снижение аппетита, включая усиление сигналов насыщения и ослабление сигналов голода, а также улучшение контроля потребления пищи и снижение тяги к пище. Снижается также инсулинорезистентность, возможно, за счёт уменьшения массы тела. Помимо этого, семаглутид снижает предпочтение к приёму пищи с высоким содержанием жиров. В исследованиях на животных было показано, что семаглутид поглощается специфическими областями головного мозга и усиливает ключевые сигналы насыщения и ослабляет ключевые сигналы голода. Воздействуя на изолированные участки тканей головного мозга семаглутид активирует нейроны, связанные с чувством сытости, и подавляет нейроны, связанные с чувством голода.
В клинических исследованиях семаглутид оказывал положительное влияние на липиды плазмы крови, снижал систолическое АД и уменьшал воспаление.
В исследованиях на животных семаглутид подавляет развитие атеросклероза, предупреждая дальнейшее развитие аортальных бляшек и уменьшая воспаление в бляшках.
Фармакокинетика
T 1/2 семаглутида равен приблизительно 1 неделе. T max в плазме составило от 1 до 3 дней после введения дозы лекарственного средства. AUC достигалась спустя 4-5 недель однократного еженедельного применения. После п/к введения семаглутида в дозах 0.5 мг и 1 мг средние показатели его равновесной концентрации у пациентов с СД2 составили около 16 нмоль/л и 30 нмоль/л, соответственно. Экспозиция для доз семаглутида 0.5 мг и 1 мг увеличивается пропорционально введённой дозе. При п/к введении семаглутида в переднюю брюшную стенку, бедро или плечо достигается сходная экспозиция. Абсолютная биодоступность семаглутида после п/к введения составила 89%. Средний объём распределения семаглутида в тканях после п/к введения пациентам с СД2 составил приблизительно 12.5 л. Семаглутид в значительной степени связывался с альбумином плазмы крови (> 99%). Семаглутид метаболизируется посредством протеолитического расщепления пептидной основы белка и последующего бета-окисления жирной кислоты боковой цепи. ЖКТ и почки являются основными путями выведения семаглутида и его метаболитов. 2/3 введённой дозы семаглутида выводится почками, 1/3- через кишечник. Приблизительно 3% от введённой дозы выводится почками в виде неизменённого семаглутида. У пациентов с СД2 клиренс семаглутида составил около 0.05 л/ч. С элиминационным T 1/2 примерно 1 неделя семаглутид будет присутствовать в общем кровотоке в течение приблизительно 5 недель после введения последней дозы лекарственного средства.
Показания активного вещества СЕМАГЛУТИД
Сахарный диабет 2 типа на фоне диеты и физических упражнений для улучшения гликемического контроля в качестве: монотерапии; комбинированной терапии с другими пероральными гипогликемическими препаратами (ПГГП)-метформином, метформином и производным сульфонилмочевины, метформином и/или тиазолидиндионом, у пациентов, не достигших адекватного гликемического контроля при проведении предшествующей терапии; комбинированной терапии с инсулином у пациентов, не достигших адекватного гликемического контроля на терапии данным лекарственным средством и метформином.
Режим дозирования
П/к в живот, бедро или плечо. Применяют 1 раз в неделю в любое время, независимо от приёма пищи. При необходимости день еженедельного введения можно менять при условии, что интервал времени между двумя инъекциями составляет не менее 3-х дней (> 72 часов). Начальная доза составляет 0.25 мг 1 раз в неделю. После 4 недель применения дозу следует увеличить до 0.5 мг 1 раз в неделю.
Побочное действие
Со стороны сердечно-сосудистой системы: увеличение ЧСС.
Местные реакции: реакции в месте введения.
Системные реакции: утомляемость.
Противопоказания к применению
Медуллярный рак щитовидной железы в анамнезе, в т.ч. в семейном; множественная эндокринная неоплазия 2 типа; сахарный диабет 1 типа; диабетический кетоацидоз; беременность и период грудного вскармливания; возраст до 18 лет; печеночная недостаточность тяжелой степени; терминальная стадия почечной недостаточности (КК С осторожностью
У пациентов с почечной недостаточностью и у пациентов с наличием панкреатита в анамнезе.
Применение при беременности и кормлении грудью
Применение при нарушениях функции печени
Препарат противопоказан для применения при нарушении функции печени
Применение при нарушениях функции почек
Препарат противопоказан для применения при нарушении функции почек
Применение у детей
Особые указания
Применение противопоказано у пациентов с СД1 или для лечения диабетического кетоацидоза. Лекарственное средство не заменяет инсулин.
Применение агонистов ГПП-1Р может быть ассоциировано с НР со стороны ЖКТ. Это следует учитывать при лечении пациентов с почечной недостаточностью, так как тошнота, рвота и диарея могут привести к дегидратации и ухудшению функции почек.
При применении агонистов ГИ-1Р наблюдались случаи развития острого панкреатита. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита. Следует соблюдать осторожность у пациентов с панкреатитом в анамнезе.
Пациенты, получающие лекарственное средство в комбинации с производным сульфонилмочевины или инсулином, могут иметь повышенный риск развития гипогликемии.
В пострегистрационном периоде применения другого аналога ГТИП-1, лираглутида, были отмечены случаи медуллярного рака щитовидной железы (МРЩЖ). Имеющихся данных недостаточно для установления или исключения причинно-следственной связи возникновения МРЩЖ с применением аналогов ГГП-1. Необходимо проинформировать пациента о риске МРЩЖ и о симптомах опухоли щитовидной железы (появления уплотнения в области шеи, дисфагии, одышки, непроходящей охриплости голоса). Значительное повышение концентрации кальцитонина в плазме крови может указывать на МРЖЩ (у пациентов с МРЖЩ значения концентрации кальцитонина в плазме крови обычно >50 нг/л). При выявлении повышения концентрации кальцитонина в плазме крови следует провести дальнейшее обследование пациента. Пациенты с узлами в щитовидной железе, выявленными при медицинском осмотре или при проведении УЗИ щитовидной железы, также должны быть дополнительно обследованы. Применение семаглутида у пациентов с личным или семейным анамнезом МРЩЖ или с синдромом МЭН типа 2 противопоказано.
Влияние на способность к управлению транспортными средствами и механизмами
Лекарственное средство не влияет или незначительно влияет на способность управлять транспортными средствами или работу с механизмами. Пациенты должны быть предупреждены о том, что им следует соблюдать меры предосторожности во избежание развития у них гипогликемии во время управления транспортными средствами и при работе с механизмами, особенно в комбинации с производным сульфонилмочевины или инсулином.
Лекарственное взаимодействие
Задержка опорожнения желудка при применении семаглутида может оказывать влияние на всасывание сопутствующих пероральных лекарственных средств. Семаглутид следует применять с осторожностью у пациентов, получающих пероральные лекарственные средства, для которых необходима быстрая абсорбция в ЖКТ.
Вещества, добавленные к лекарственному средству, могут вызвать деградацию семаглутида. Нельзя смешивать с другими лекарственными средствами, в том числе с инфузионными растворами.
Регистрационный номер:
Торговое наименование:
Международное непатентованное наименование:
Лекарственная форма:
раствор для подкожного введения
Состав
В 1 мл препарата содержится:
действующее вещество: семаглутид 1,34 мг;
вспомогательные вещества: динатрия гидрофосфат дигидрат, пропиленгликоль, фенол, хлористоводородная кислота (для коррекции pH), натрия гидроксид (для коррекции pH), вода для инъекций.
Для шприц-ручки Оземпик ® 0,25 мг/доза или 0,5 мг/доза:
В одной предварительно заполненной шприц-ручке объёмом 1,5 мл содержится 2 мг семаглутида.
Для шприц-ручки Оземпик ® 1 мг/доза:
В одной предварительно заполненной шприц-ручке объёмом 3 мл содержится 4 мг семаглутида.
Описание
Прозрачный бесцветный или почти бесцветный раствор.
Фармакотерапевтическая группа
Гипогликемическое средство – аналог глюкагоноподобного пептида-1 (ГПП-1).
Код ATX:
Фармакологические свойства
Семаглутид является агонистом рецепторов ГПП-1 (ГПП-1Р), произведённым методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae с последующей очисткой.
Семаглутид представляет собой аналог ГПП-1, имеющий 94% гомологичности с человеческим ГПП-1. Семаглутид действует как агонист ГПП-1Р, который селективно связывается и активирует ГПП-1Р. ГПП-1Р служит мишенью для нативного ГПП-1.
ГПП-1 является физиологическим гормоном, оказывающим сразу несколько эффектов на регуляцию концентрации глюкозы и аппетит, а также на сердечно-сосудистую систему (ССС). Влияние на концентрацию глюкозы и аппетит специфически опосредовано ГПП-1Р, расположенными в поджелудочной железе и головном мозге. Фармакологические концентрации семаглутида снижают концентрацию глюкозы крови и массу тела посредством сочетания эффектов, описанных ниже. ГПП-1Р представлены также в специфических областях сердца, сосудов, иммунной системы и почек, где их активация может оказывать сердечно-сосудистые (СС) и микроциркуляторные эффекты.
В отличие от нативного ГПП-1, продлённый период полувыведения семаглутида (около 1 недели) позволяет применять его подкожно (п/к) 1 раз в неделю. Связывание с альбумином является основным механизмом длительного действия семаглутида, что приводит к снижению выведения его почками и защищает от метаболического распада. Кроме того, семаглутид стабилен в отношении расщепления ферментом дипептидилпептидазой-4.
Семаглутид снижает концентрацию глюкозы крови посредством глюкозозависимых стимуляции секреции инсулина и подавления секреции глюкагона. Таким образом, при повышении концентрации глюкозы крови происходит стимуляция секреции инсулина и подавление секреции глюкагона. Механизм снижения уровня гликемии включает также небольшую задержку опорожнения желудка в ранней постпрандиальной фазе. Во время гипогликемии семаглутид уменьшает секрецию инсулина и не снижает секрецию глюкагона.
Семаглутид снижает общую массу тела и массу жировой ткани, уменьшая потребление энергии. Данный механизм затрагивает общее снижение аппетита, включая усиление сигналов насыщения и ослабление сигналов голода, а также улучшение контроля потребления пищи и снижение тяги к пище. Снижается также инсулинорезистентность, возможно, за счёт уменьшения массы тела. Помимо этого, семаглутид снижает предпочтение к приёму пищи с высоким содержанием жиров. В исследованиях на животных было показано, что семаглутид поглощается специфическими областями головного мозга и усиливает ключевые сигналы насыщения и ослабляет ключевые сигналы голода. Воздействуя на изолированные участки тканей головного мозга семаглутид активирует нейроны, связанные с чувством сытости, и подавляет нейроны, связанные с чувством голода.
В клинических исследованиях (КИ) семаглутид оказывал положительное влияние на липиды плазмы крови, снижал систолическое артериальное давление (АД) и уменьшал воспаление.
В исследованиях на животных семаглутид подавляет развитие атеросклероза, предупреждая дальнейшее развитие аортальных бляшек и уменьшая воспаление в бляшках.
Фармакокинетика
Препарат подходит для введения 1 раз в неделю, так как период полувыведения семаглутида равен приблизительно 1 неделе.
Абсорбция
Время достижения максимальной концентрации (Сmax) в плазме составило от 1 до 3 дней после введения дозы препарата.
Равновесная концентрация препарата (AUCτ/24) достигалась спустя 4-5 недель однократного еженедельного применения препарата. После п/к введения семаглутида в дозах 0,5 мг и 1 мг средние показатели его равновесной концентрации у пациентов с СД2 составили около 16 нмоль/л и 30 нмоль/л, соответственно.
Экспозиция для доз семаглутида 0,5 мг и 1 мг увеличивается пропорционально введённой дозе.
При п/к введении семаглутида в переднюю брюшную стенку, бедро или плечо достигается сходная экспозиция.
Абсолютная биодоступность семаглутида после п/к введения составила 89%.
Распределение
Средний объём распределения семаглутида в тканях после п/к введения пациентам с СД2 составил приблизительно 12,5 л. Семаглутид в значительной степени связывался с альбумином плазмы крови (>99%).
Метаболизм
Семаглутид метаболизируется посредством протеолитического расщепления пептидной основы белка и последующего бета-окисления жирной кислоты боковой цепи.
Выведение
Желудочно-кишечный тракт (ЖКТ) и почки являются основными путями выведения семаглутида и его метаболитов, 2/3 введённой дозы семаглутида выводится почками, 1/3 – через кишечник.
Приблизительно 3% от введённой дозы выводится почками в виде неизменённого семаглутида.
У пациентов с СД2 клиренс семаглутида составил около 0,05 л/ч. С элиминационным периодом полувыведения примерно 1 неделя семаглутид будет присутствовать в общем кровотоке в течение приблизительно 5 недель после введения последней дозы препарата.
Особые группы пациентов
Не требуется коррекции дозы семаглутида в зависимости от возраста, пола, расовой и этнической принадлежности, массы тела, наличия почечной или печёночной недостаточности.
Возраст
На основании данных, полученных в ходе КИ 3а фазы, включавших пациентов в возрасте от 20 до 86 лет, показано, что возраст не влиял на фармакокинетику семаглутида.
Пол
Пол не влиял на фармакокинетику семаглутида.
Раса
Расовая группа (белая, чёрная или афроамериканская, азиатская) не влияла на фармакокинетику семаглутида.
Этническая принадлежность
Этническая принадлежность (латиноамериканская) не влияла на фармакокинетику семаглутида.
Масса тела
Масса тела влияла на экспозицию семаглутида. Более высокая масса тела приводит к более низкой экспозиции. Дозы семаглутида равные 0,5 мг и 1 мг обеспечивают достаточную экспозицию препарата в диапазоне массы тела от 40 до 198 кг.
Почечная недостаточность
Почечная недостаточность не оказала клинически значимого эффекта на фармакокинетику семаглутида. Это было показано у пациентов с различной степенью почечной недостаточности (лёгкой, средней, тяжёлой или у пациентов, находящихся на диализе) по сравнению с пациентами с нормальной функцией почек в исследовании однократной дозы семаглутида равной 0,5 мг. Это также было показано на основании данных КИ 3а фазы для пациентов с СД2 и почечной недостаточностью, хотя опыт применения у пациентов с терминальной стадией заболевания почек был ограничен.
Печёночная недостаточность
Печёночная недостаточность не влияла на экспозицию семаглутида. Фармакокинетические свойства семаглутида оценивались в ходе исследования однократной дозы семаглутида равной 0,5 мг у пациентов с различной степенью печёночной недостаточности (лёгкой, средней, тяжёлой) по сравнению с пациентами с нормальной функцией печени.
Дети и подростки
Исследований семаглутида у детей и подростков до 18 лет не проводили.
Показания к применению
Противопоказания
Противопоказано применение препарата Оземпик ® у следующих групп пациентов и при следующих состояниях/заболеваниях в связи с отсутствием данных по эффективности и безопасности иди ограниченным опытом применения:
Применение при беременности и в период грудного вскармливания
Беременность
Исследования на животных продемонстрировали репродуктивную токсичность препарата (см. раздел «Доклинические данные по безопасности»).
Данные по применению семаглутида у беременных женщин ограничены. Противопоказано применять семаглутид во время беременности. Женщинам с сохранённым репродуктивным потенциалом рекомендуется использовать контрацепцию во время терапии семаглутидом. Если пациентка готовится к беременности, либо беременность уже наступила, терапию семаглутидом необходимо прекратить. Из-за длительного периода полувыведения терапию семаглутидом необходимо прекратить как минимум за 2 месяца до планируемого наступления беременности (см. раздел «Фармакокинетика»).
Период грудного вскармливания
У лактирующих крыс семаглутид проникал в молоко. Нельзя исключить риск для ребёнка, находящегося на грудном вскармливании. Противопоказано применять семаглутид в период грудного вскармливания.
Способ применения и дозы
Способ применения
Препарат Оземпик ® применяют 1 раз в неделю в любое время, независимо от приёма пищи. Препарат Оземпик ® вводят п/к в живот, бедро или плечо. Место инъекции может изменяться без коррекции дозы. Препарат Оземпик ® нельзя вводить внутривенно и внутримышечно. Дальнейшая информация по способу применения содержится в разделе «Руководство по использованию».
При необходимости день еженедельного введения можно менять при условии, что интервал времени между двумя инъекциями составляет не менее 3-х дней (>72 часов).
Дозы
Начальная доза препарата Оземпик ® составляет 0,25 мг 1 раз в неделю. После 4 недель применения дозу следует увеличить до 0,5 мг 1 раз в неделю. Для дальнейшего улучшения гликемического контроля после как минимум 4 недель применения препарата в дозе 0,5 мг 1 раз в неделю, дозу можно увеличить до 1 мг 1 раз в неделю.
Доза препарата Оземпик ® 0,25 мг не является терапевтической.
Препарат Оземпик ® может применяться в виде монотерапии или в комбинации с одним или более гипогликемическими препаратами (см. раздел «Клиническая эффективность и безопасность»).
При добавлении препарата Оземпик ® к предшествующей терапии метформином и/или тиазолидиндионом терапию метформином и/или тиазолидиндионом можно продолжить в прежних дозах.
При добавлении препарата Оземпик ® к проводимой терапии производным сульфонилмочевины или инсулином следует предусмотреть снижение дозы производного сульфонилмочевины или инсулина с целью снижения риска возникновения гипогликемий (см. раздел «Особые указания»).
Применение препарата Оземпик ® не требует проведения самоконтроля концентрации глюкозы крови. При применении препарата Оземпик ® в комбинации с производным сульфонилмочевины или инсулином, такой самоконтроль концентрации глюкозы крови может потребоваться для коррекции дозы производного сульфонилмочевины или инсулина.
Пропущенная доза
В случае пропуска дозы препарат Оземпик ® следует ввести как можно быстрее в течение 5 дней с момента запланированного введения дозы. Если продолжительность пропуска составляет более 5 дней, пропущенную дозу не нужно вводить. Следующую дозу препарата Оземпик ® следует ввести в обычный запланированный день. В каждом случае пациенты могут возобновить их обычный однократный еженедельный график введения.
Применение препарата в особых клинических группах пациентов
Пациенты пожилого возраста (≥65 лет)
Не требуется коррекции дозы в зависимости от возраста. Опыт применения семаглутида у пациентов в возрасте 75 лет и старше ограничен.
Пациенты с печёночной недостаточностью
Не требуется коррекции дозы у пациентов с печёночной недостаточностью (см. раздел «Фармакокинетика»). Опыт применения семаглутида у пациентов с печёночной недостаточностью тяжёлой степени ограничен; применение препарата Оземпик ® у таких пациентов противопоказано.
Пациенты с почечной недостаточностью
Не требуется коррекции дозы у пациентов с почечной недостаточностью. Опыт применения препарата у пациентов с терминальной стадией почечной недостаточности отсутствует; применение препарата Оземпик ® у таких пациентов противопоказано.
Дети и подростки
Применение препарата Оземпик ® у детей и подростков в возрасте до 18 лет противопоказано в связи с отсутствием данных по безопасности и эффективности.
Побочное действие
Наиболее часто регистрируемыми нежелательными реакциями (HP) во время КИ являлись нарушения со стороны ЖКТ, включая тошноту, диарею и рвоту. В целом, данные реакции были лёгкой или средней степени тяжести и краткосрочными.
HP распределены по системно-органным классам в соответствии с MedDRA с указанием частоты их возникновения согласно рекомендациям ВОЗ: очень часто (≥1/10); часто (≥1/100 до
| Система органов MedDRA | Очень часто | Часто | Нечасто | Редко |
| Нарушения со стороны иммунной системы | Анафилактические реакции | |||
| Нарушения со стороны обмена веществ и питания | Гипогликемия a при совместном применении с инсулином или производным сульфонилмочевины | Гипогликемия a при совместном применении с другими ПГГП Снижение аппетита | ||
| Нарушения со стороны нервной системы | Головокружение | Дисгевзия | ||
| Нарушения со стороны органа зрения | Осложнения диабетической ретинопатии b | |||
| Нарушения со стороны сердца | Увеличение частоты сердечных сокращений (ЧСС) | |||
| Нарушения со стороны ЖКТ | Тошнота Диарея | Рвота Боль в животе Вздутие живота Запор Диспепсия Гастрит Гастроэзофагеальная рефлюксная болезнь Отрыжка Метеоризм | ||
| Нарушения со стороны печени и желчевыводящих путей | Холелитиаз | |||
| Общие расстройства и нарушения в месте введения | Утомляемость | Реакции в месте введения | ||
| Лабораторные и инструментальные данные | Повышение активности липазы Повышение активности амилазы Снижение массы тела |
a Гипогликемия, определенная как тяжёлая (требующая помощи другого человека) или симптоматическая в сочетании с концентрацией глюкозы в плазме крови b Осложнения диабетической ретинопатии – это сочетание из: необходимости в фотокоагуляции сетчатки глаза, необходимости в интравитреальном введении препаратов, кровоизлияния в стекловидное тело, развития слепоты, связанной с СД.
Частота основана на исследовании СС исходов.
2-летнее исследование СС исходов и безопасности
В популяции пациентов с высоким риском развития СС заболеваний профиль HP был аналогичным таковому в других КИ 3а фазы (описаны в разделе «Клиническая эффективность и безопасность»).
Передозировка
В ходе КИ сообщалось о передозировках до 4 мг в однократной дозе и до 4 мг в неделю. Наиболее частой HP, о которой сообщалось, была тошнота. Все пациенты выздоровели без осложнений.
Специфического антидота при передозировке препарата Оземпик ® не существует. В случае передозировки рекомендуется проведение соответствующей симптоматической терапии. Учитывая длительный период выведения препарата (примерно 1 неделя), может потребоваться продолжительный период наблюдения и лечения симптомов передозировки.
Взаимодействие с другими лекарственными средствами
Особые указания
Применение препарата Оземпик ® противопоказано у пациентов с СД1 или для лечения диабетического кетоацидоза.
Препарат Оземпик ® не заменяет инсулин.
Реакции со стороны ЖКТ
Применение агонистов ГПП-1Р может быть ассоциировано с HP со стороны ЖКТ. Это следует учитывать при лечении пациентов с почечной недостаточностью, так как тошнота, рвота и диарея могут привести к дегидратации и ухудшению функции почек.
Острый панкреатит
При применении агонистов ГПП-1Р наблюдались случаи развития острого панкреатита. Пациенты должны быть проинформированы о характерных симптомах острого панкреатита. При подозрении на панкреатит терапия препаратом Оземпик ® должна быть прекращена; в случае подтверждения острого панкреатита терапию препаратом Оземпик ® возобновлять не следует. Следует соблюдать осторожность у пациентов с панкреатитом в анамнезе.
При отсутствии других признаков и симптомов острого панкреатита повышение активности ферментов поджелудочной железы не является прогностическим фактором развития острого панкреатита.
Гипогликемия
Пациенты, получающие препарат Оземпик ® в комбинации с производным сульфонилмочевины или инсулином, могут иметь повышенный риск развития гипогликемии. В начале лечения препаратом Оземпик ® риск развития гипогликемии можно снизить, уменьшив дозу производного сульфонилмочевины или инсулина.
Диабетическая ретинопатия
Наблюдалось повышение риска развития осложнений диабетической ретинопатии у пациентов с наличием диабетической ретинопатии, получающих терапию инсулином и семаглутидом (см. раздел «Побочное действие»). Следует соблюдать осторожность при применении семаглутида у пациентов с диабетической ретинопатией, получающих инсулинотерапию. Такие пациенты должны находиться под постоянным наблюдением и получать лечение в соответствии с клиническими рекомендациями. Быстрое улучшение гликемического контроля было ассоциировано с временным ухудшением состояния диабетической ретинопатии, однако при этом нельзя исключать и другие причины.
Сердечная недостаточность
Отсутствует опыт применения препарата Оземпик ® у пациентов с ХСН IV функционального класса в соответствии с классификацией NYHA. Применение препарата у таких пациентов противопоказано.
Заболевания щитовидной железы
В пострегистрационном периоде применения другого аналога ГПП-1, лираглутида, были отмечены случаи медуллярного рака щитовидной железы (МРЩЖ). Имеющихся данных недостаточно для установления или исключения причинно-следственной связи возникновения МРЩЖ с применением аналогов ГПП-1. Необходимо проинформировать пациента о риске МРЩЖ и о симптомах опухоли щитовидной железы (появления уплотнения в области шеи, дисфагии, одышки, непроходящей охриплости голоса).
Значительное повышение концентрации кальцитонина в плазме крови может указывать на МРЖЩ (у пациентов с МРЖЩ значения концентрации кальцитонина в плазме крови обычно >50 нг/л). При выявлении повышения концентрации кальцитонина в плазме крови следует провести дальнейшее обследование пациента. Пациенты с узлами в щитовидной железе, выявленными при медицинском осмотре или при проведении УЗИ щитовидной железы, также должны быть дополнительно обследованы.
Применение семаглутида у пациентов с личным или семейным анамнезом МРЩЖ или с синдромом МЭН типа 2 противопоказано.
Доклинические данные по безопасности
Доклинические данные, основанные на исследованиях фармакологической безопасности, токсичности повторных доз и генотоксичности, не выявили какой-либо опасности для человека.
В 2-летних исследованиях канцерогенности у крыс и мышей при клинически значимых концентрациях семаглутид стал причиной развития опухолей С-клеток щитовидной железы без смертельного исхода. Опухоли С-клеток щитовидной железы без смертельного исхода, наблюдаемые у крыс, характерны для группы аналогов ГПП-1. Считается, что в отношении людей данный риск является низким, но не может быть полностью исключён.
Фертильность
Действие семаглутида на фертильность у людей неизвестно. Семаглутид не влиял на фертильность самцов крыс. Среди самок крыс увеличение эстрального цикла и незначительное снижение количества овуляций наблюдалось при дозах, сопровождавшихся снижением массы тела самки.
Влияние на способность управлять транспортными средствами и работу с механизмами
Препарат Оземпик ® не влияет или незначительно влияет на способность управлять транспортными средствами или работу с механизмами. Пациенты должны быть предупреждены о том, что им следует соблюдать меры предосторожности во избежание развития у них гипогликемии во время управления транспортными средствами и при работе с механизмами, особенно при применении препарата Оземпик ® в комбинации с производным сульфонилмочевины или инсулином.
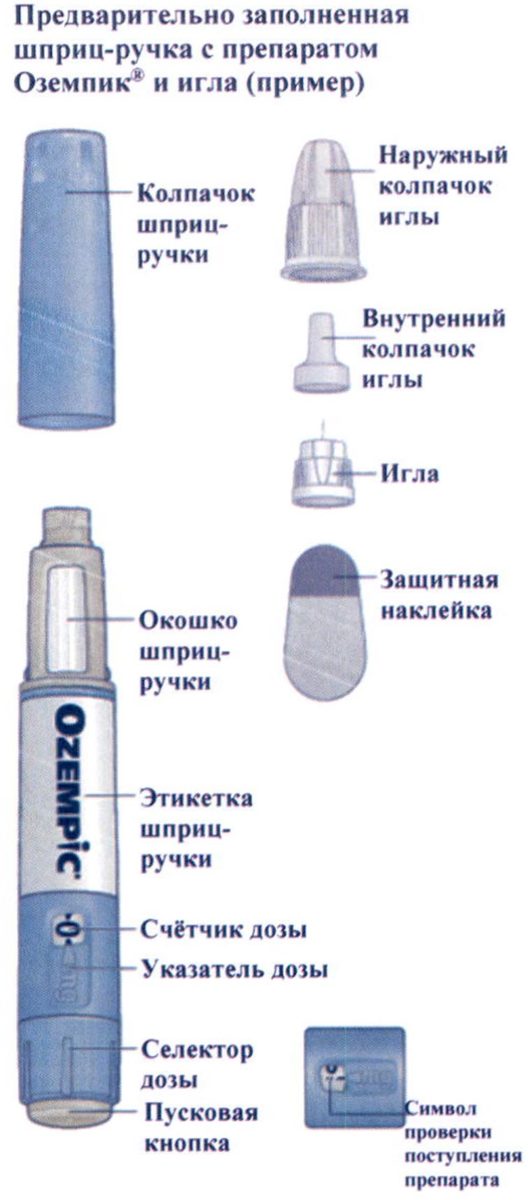
Руководство по использованию
Форма выпуска
Раствор для подкожного введения, 1,34 мг/мл.
1) Шприц-ручка Оземпик ® 0,25 мг/доза или 0,5 мг/доза.
По 1,5 мл препарата в картриджи из стекла, укупоренные поршнями из хлорбутиловой резины с одной стороны и алюминиевыми колпачками с дисками из бромбутиловой резины/полиизопрена, с другой стороны. Картридж встроен в мультидозовую одноразовую шприц-ручку для многократных инъекций из полипропилена, полиоксиметилена, поликарбоната и акрилонитрил бутадиен стирола. 1 шприц-ручка вместе с инструкцией по применению и 6 одноразовыми иглами НовоФайн ® Плюс в картонную пачку.
2) Шприц-ручка Оземпик ® 1 мг/доза.
По 3 мл препарата в картриджи из стекла, укупоренные поршнями из хлорбутиловой резины с одной стороны и алюминиевыми колпачками с дисками из бромбутиловой резины/полиизопрена, с другой стороны. Картридж встроен в мультидозовую одноразовую шприц-ручку для многократных инъекций из полипропилена, полиоксиметилена, поликарбоната и акрилонитрил бутадиен стирола. 1 шприц-ручка вместе с инструкцией по применению и 4 одноразовыми иглами НовоФайн ® Плюс в картонную пачку.
Срок годности
3 года. Не применять по истечении срока, указанного на этикетке шприц-ручки и упаковке.
Условия хранения
Хранить при температуре от 2 °С до 8 °С (в холодильнике), но не рядом с морозильной камерой. Защищать от света. Не замораживать.
Используемую или переносимую в качестве запасной шприц-ручку с препаратом хранить при температуре не выше 30 °С или при температуре от 2 °С до 8 °С (в холодильнике) в течение 6 недель. Не замораживать. После использования закрывать шприц-ручку колпачком для защиты от света.
Препарат Оземпик ® следует предохранять от воздействия избыточного тепла и света. Хранить в недоступном для детей месте.
Условия отпуска
Отпускают по рецепту.
Производитель и владелец регистрационного удостоверения:
Ново Нордиск А/С, Ново Алле, DK-2880 Багсваерд, Дания
Производство готовой лекарственной формы:
Ново Нордиск А/С, Ново Алле, DK-2880 Багсваерд, Дания
Первичная упаковка:
Ново Нордиск А/С, Ново Алле, DK-2880 Багсваерд, Дания
Вторичная/потребительская упаковка:
Ново Нордиск А/С, Бреннум Парк, DK-3400 Хиллерод, Дания
Производитель (Выпускающий контроль качества):
Ново Нордиск А/С, Ново Алле, DK-2880 Багсваерд, Дания
Организация, принимающая претензии от потребителей:
ООО «Ново Нордиск», 121614, Москва, ул. Крылатская, д. 15, офис 41
Оземпик ® и НовоФайн ® – зарегистрированные торговые марки, принадлежащие компании Ново Нордиск А/С, Дания
Инструкция для пациентов по применению препарата Оземпик ® 0,25 мг/доза или 0,5 мг/доза раствор для подкожного введения в предварительно заполненной шприц-ручке.
Важная информация

Аккуратно обращайтесь со шприц-ручкой. Небрежное обращение или неправильное использование могут привести к введению неправильной дозы препарата, следствием чего могут стать высокая концентрация глюкозы крови или дискомфорт в области живота (тошнота или рвота).
Инструкция для пациентов по применению препарата Оземпик ® 1 мг/доза раствор для подкожного введения в предварительно заполненной шприц-ручке.
Уход за шприц-ручкой
Аккуратно обращайтесь со шприц-ручкой. Небрежное обращение или неправильное использование могут привести к введению неправильной дозы препарата, следствием чего могут стать высокая концентрация глюкозы крови или дискомфорт в области живота (тошнота или рвота).