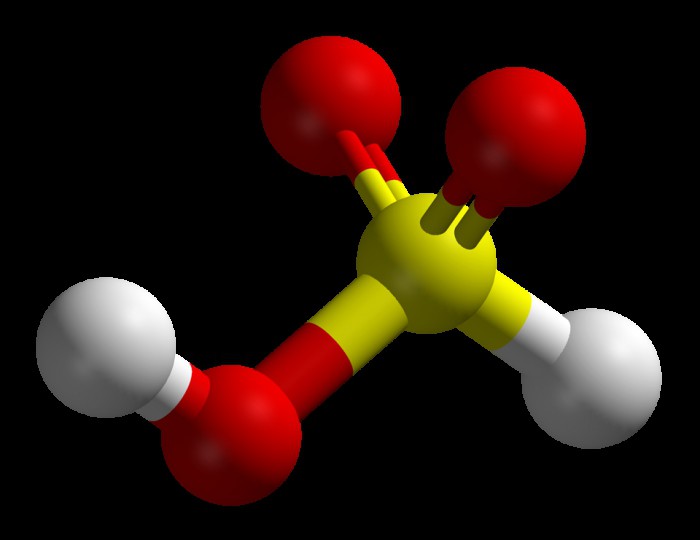
с чем реагирует сернистая кислота
Сернистая кислота: строение и химические свойства
Сернистая кислота H2SO3 – это двухосновная кислородсодержащая кислота. При нормальных условиях — неустойчивое вещество, которое распадается на диоксид серы и воду.
Валентность серы в сернистой кислоте равна IV, а степень окисления +4.
Химические свойства
1. Сернистая кислота H2SO3 в водном растворе – двухосновная кислота средней силы. Частично диссоциирует по двум ступеням:
HSO3 – ↔ SO3 2– + H +
2. Сернистая кислота самопроизвольно распадается на диоксид серы и воду:
3. Сернистая кислота взаимодействует с сильными основаниями и их оксидами.
4. Наиболее ярко выражены восстановительные свойства сернистой кислоты. При взаимодействии с окислителями степень окисления серы повышается.
Азотная кислота очень легко окисляет сернистую:
Озон также окисляет сернистую кислоту:
Качественная реакция на сернистую кислоту – обесцвечивание раствора перманганата калия:
5. В присутствии сильных восстановителей сернистая кислота может проявлять окислительные свойства.
Оксид серы (IV) и сернистая кислота
SO 2 (сернистый ангидрид; сернистый газ)
Обесцвечивает многие красители, убивает микроорганизмы.
1) При сжигании серы в кислороде:
2) Окислением сульфидов:
3) Обработкой солей сернистой кислоты минеральными кислотами:
4) При окислении металлов концентрированной серной кислотой:
1) Сернистый ангидрид — кислотный оксид.
· взаимодействие с водой
При растворении в воде образуется слабая и неустойчивая сернистая кислота H 2 SO 3 (существует только в водном растворе)
Сернистая кислота диссоциирует ступенчато:
H 2 SO 3 ↔ H + + HSO 3 — (первая ступень, образуется гидросульфит – анион)
HSO 3 — ↔ H + + SO 3 2- (вторая ступень, образуется анион сульфит)
H 2 SO 3 образует два ряда солей — средние (сульфиты) и кислые (гидросульфиты).
Качественной реакцией на соли сернистой кислоты является взаимодействие соли с сильной кислотой, при этом выделяется газ SO 2 с резким запахом:
Раствор сернистой кислоты H2SO3 обладает восстановительными свойствами. Сернистая кислота взаимодействует с раствором йода, обесцвечивая его. При этом образуются йодоводородная и серная кислоты.
· взаимодействие со щелочами
Ba ( OH )2 + 2 SO 2 (избыток)→ Ba ( HSO 3)2(гидросульфит бария)
· взаимодействие с основными оксидами
2) Реакции окисления, SO 2 — восстановитель ( S +4 – 2ē → S +6 )
Водные растворы сульфитов щелочных металлов окисляются на воздухе:
3) Реакции восстановления, SO 2 — окислитель ( S +4 + 4ē → S 0 )
SO 2 + С → S + С O 2 (при нагревании)
Свойства сернистой кислоты и её взаимодействие с другими веществами
Сернистая кислота — что она собой представляет
Сернистая кислота — это двухосновная кислородсодержащая кислота.
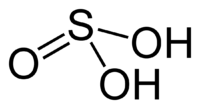
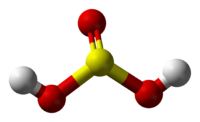
Сернистая кислота является неустойчивым веществом, распадающимся на диоксид серы S O 2 и воду. Валентность серы в сернистой кислоте равна IV, а степень окисления: +4. Структурная формула выглядит так:
Химические и физические свойства
Сернистый ангидрид S O 2 представляет собой бесцветный газ и обладает резким запахом.
Физические свойства сернистой кислоты:
Сернистая кислота в водном растворе является слабым электролитом. Диссоциация протекает обратимо по двум ступеням.
H 2 S O 3 ↔ H S O 3 – + H +
H S O 3 – ↔ S O 3 2 – + H +
В процессе самопроизвольного распада сернистой кислоты образуются диоксид серы и вода.
H 2 S O 3 ↔ S O 2 + H 2 O
Сернистая кислота вступает в химическую реакцию с сильными основаниями и их оксидами.
Взаимодействие сернистой кислоты с гидроксидами таких щелочных металлов, как натрий и калий, описывается уравнениями:
H 2 S O 3 + К О Н → K H S О 3 + H 2 O
H 2 S O 3 + 2 К О Н → К 2 S О 3 + 2 H 2 O
Среди всех химических свойств сернистой кислоты наиболее ярко выражены ее восстановительные свойства. Взаимодействуя с окислителями, сера повышают собственную степень окисления.
Обесцвечивание бромной воды с помощью сернистой кислоты:
H 2 S O 3 + B r 2 + H 2 O → H 2 S O 4 + 2 H B r
Процесс окисления сернистой кислоты азотной протекает достаточно легко по уравнению:
H 2 S O 3 + 2 H N O 3 → H 2 S O 4 + 2 N O 2 + H 2 O
Окисление сернистой кислоты с помощью озона:
H 2 S O 3 + O 3 → H 2 S O 4 + O 2
При контакте с сильными восстановителями могут проявляться окислительные свойства сернистой кислоты.
Взаимодействие сернистой кислоты и сероводорода сопровождается ее восстановлением до элементарной серы:
H 2 S O 3 + 2 Н 2 S → 3 S + 3 H 2 O
Качественная реакция на сернистую кислоту
Качественная реакция на сернистую кислоту представляет собой обесцвечивание раствора перманганата калия:
5 H 2 S O 3 + 2 K M n O 4 → 2 H 2 S O 4 + 2 M n S O 4 + K 2 S O 4 + 3 H 2 O
N a 2 S O 3 + 2 H C l → 2 N a C l + S O 2 ↑ + H 2 O
2 H + + S O 3 2 – → S O 2 ↑ + H 2 O
Способы получения и как применяется
Далее можно наблюдать реакцию, протекающую по уравнению:
C u ( м е д ь ) + 2 H 2 S O 4 ( с е р н а я к и с л о т а ) = C u S O 4 ( с у л ь ф а т с е р ы ) + S O 2 ( с е р н и с т ы й г а з ) + H 2 O ( в о д а )
Затем поток сернистого газа следует направить в пробирку с водой. При нахождении в ней газообразное вещество растворяется, частично протекает химическая реакция с водой. В итоге синтезируется сернистая кислота:
S O 2 ( с е р н и с т ы й г а з ) + H 2 O ( в о д а ) = H 2 S O 3
Таким образом с помощью пропускания сернистого газа через воду получают сернистую кислоту.
В процессе экспериментов с сернистым газом необходимо использовать индивидуальные средства защиты, так как вещество раздражает слизистую оболочку дыхательных путей. Подобное воздействие сопровождается воспалительным процессом и потерей аппетита. Длительное вдыхание сернистого газа приводит к потере сознания.
Сернистая кислота нашла применение в качестве восстановителя. Вещество используют для беления шерсти, шелка и других материалов, которые не способны выдержать отбеливание сильными окислителями в виде хлора. Сернистую кислоту используют в процессе консервирования плодов и овощей, а также для:
Сернистая кислота: что она собой представляет и где применяется?
При растворении в воде диоксида серы (SO2) получается химическое соединение, известное как сернистая кислота. Формула этого вещества записывается так: H2SO3. По правде говоря, данное соединение является крайне нестабильным, с определенным допущением даже можно утверждать, что его на самом деле не существует. Тем не менее данную формулу часто используют для удобства написания уравнений химических реакций.
Где используется сернистая кислота
Получение данного вещества играет большую роль в производстве всевозможных виноматериалов в качестве антисептика, в частности с его помощью удается предотвратить процесс брожения продукта в бочках и тем самым обеспечить его сохранность. Также его применяют для того, чтобы воспрепятствовать ферментации зерна в ходе извлечения из него крахмала. Сернистая кислота и препараты на ее основе обладают широким антимикробным свойством, и поэтому их часто применяют в плодоовощной промышленности при консервировании. Гидросульфит кальция, его еще называют сульфитный щелок, используют для того, чтобы переработать древесину в сульфитную целлюлозу, из которой впоследствии изготавливают бумагу. Осталось добавить, что для человека это соединение является ядовитым, а потому любые лабораторные работы и эксперименты с ним требуют осторожности и повышенного внимания.
Сернистая кислота
| Сернистая кислота | |
 | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | сернистая кислота |
| Химическая формула | H2SO3 |
| Физические свойства | |
| Состояние (ст. усл.) | жидкость |
| Отн. молек. масса | 82.07 а. е. м. |
| Молярная масса | 82.07 г/моль |
| Плотность | 1,03 г/см³ |
| Термические свойства | |
| Химические свойства | |
| pKa | 1,81 |
| Растворимость в воде | 14.73 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7782-99-2 |
| Регистрационный номер EC | 231-973-1 |
| Безопасность | |
| Токсичность |  |
Серни́стая кислота — неустойчивая двухосновная неорганическая кислота средней силы. Химическая формула 
Химические свойства
Кислота средней силы:

Существует лишь в разбавленных водных растворах (в свободном состоянии не выделена):
Растворы H2SO3 всегда имеют резкий специфический запах (похожий на запах зажигающейся спички), обусловленный наличием химически не связанного водой SO2.
Двухосновная кислота, образует два ряда солей: кислые — гидросульфиты (в недостатке щёлочи):
и средние — сульфиты (в избытке щёлочи):
Как и сернистый газ, сернистая кислота и её соли являются сильными восстановителями:
При взаимодействии с ещё более сильными восстановителями может играть роль окислителя:
Качественная реакция на сульфит-ионы — обесцвечивание раствора перманганата калия:
слабая двухосновная кислота, отвечающая степени окисления серы +4
Применение
Сернистая кислота и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора). Сернистую кислоту применяют при консервировании плодов и овощей. Гидросульфит кальция (сульфитный щелок, Са(HSO3)2) используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнин — вещество, связывающее волокна целлюлозы, в результате чего волокна отделяются друг от друга; обработанную таким образом древесину используют для получения бумаги).
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | — | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Сернистая кислота» в других словарях:
СЕРНИСТАЯ КИСЛОТА — H2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в водных растворах. Соли сернистой кислоты сульфиты … Большой Энциклопедический словарь
СЕРНИСТАЯ КИСЛОТА — (H2SO3) слабая двухосновная кислота. Существует лишь в водных растворах. Соли С. к. сульфиты. Применяют в целлюлозно бумажной и пищевой промышленности. См. также Кислоты и ангидриды … Российская энциклопедия по охране труда
сернистая кислота — — [А.С.Гольдберг. Англо русский энергетический словарь. 2006 г.] Тематики энергетика в целом EN sulfurous acid … Справочник технического переводчика
сернистая кислота — Н2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в водных растворах. Соли серной кислоты сульфиты. * * * СЕРНИСТАЯ КИСЛОТА СЕРНИСТАЯ КИСЛОТА, H2SO3, слабая двухосновная кислота. В свободном виде не выделена,… … Энциклопедический словарь
сернистая кислота — sulfito rūgštis statusas T sritis chemija formulė H₂SO₃ atitikmenys: angl. sulfurous acid rus. сернистая кислота ryšiai: sinonimas – vandenilio trioksosulfatas (2–) … Chemijos terminų aiškinamasis žodynas
Сернистая кислота — H2SO3, слабая двухосновная кислота, отвечающая степени окисления серы +4. Известна только в разбавленных водных растворах. Константы диссоциации: K1 = 1,6 · 10 2, K2 = 1,0 · 10 7 (18°C). Даёт два ряда солей: нормальные Сульфиты и кислые… … Большая советская энциклопедия
СЕРНИСТАЯ КИСЛОТА — H2SO3, слабая двухосновная кислота. В свободном виде не выделена, существует в вод. р рах. Соли С. к. сульфиты … Естествознание. Энциклопедический словарь
Сернистая кислота — см. Сера … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
СЕРНИСТАЯ КИСЛОТА — см. Серы диоксид … Химическая энциклопедия