с чего начинается иммунитет
Роспотребнадзор (стенд)
Роспотребнадзор (стенд)
Иммунитет – способность иммунной системы избавлять организм от генетически чужеродных объектов. Иммунитет заложен в человеке с рождения. Эффективность иммунной системы зависит от наследственности, однако правильное питание и здоровый образ жизни могут значительно повысить ее активность.
Иммунная система – это система особых клеток и белков, защищающих организм от болезнетворных микроорганизмов (бактерий, вирусов, грибков, а также от определенных ядов). Иммунная система контролирует развитие раковых клеток, своевременно выявляя и уничтожая те, которые растут бесконтрольно.
Органы, входящие в иммунную систему: лимфатические узлы, миндалины, вилочковая железа (тимус) костный мозг, селезенка. Ученые установили, что большая часть клеток-защитников располагается в кишечнике – 80%.
Различают врожденный иммунитет и приобретенный (активный, пассивный). Иммунитет начинает формироваться еще до рождения человека – в материнской утробе. Пассивный иммунитет формируется в организме после введения вакцины.
Силы иммунитета на 50% зависят от образа жизни, который ведет человек.
Факторы, негативно воздействующие на иммунитет:
· нерациональное питание (голодание, переедание);
· дефицит витаминов и микроэлементов;
· перенесённые травмы, ожоги, операции;
· загрязнение окружающей среды;
бесконтрольное употребление лекарств.Частые простудные заболевания, герпес на губах, продолжительное повышение температуры, синдром хронической усталости, сонливость или бессонница, болевые ощущения в суставах и мышцах, нарушения сна, частые головные боли, появление высыпаний на коже – всё это признаки снижения иммунной активности.
Что необходимо человеку для поддержания иммунитета?
1. Полноценное здоровое питание.
2. Отказ от курения и употребления алкоголя.
3. Бережное отношение к своей психике.
4. Здоровый сон (не менее 8 часов в сутки в хорошо проветренном помещении).
5. Закаливание (обливания и контрастный душ, посещение бани и сауны). Рекомендовано чередование высоких и низких температур.
6. Регулярные занятия спортом, подвижный образ жизни. Доказано, что чрезмерные нагрузки могут негативно влиять на иммунитет.
Всемирный день иммунитета – это ещё одна возможность подчеркнуть важность и значимость здорового образа жизни. Своевременно корректируя нарушения иммунитета, можно предотвратить возникновение заболеваний многих органов и систем. Для хорошего самочувствия и правильной работы внутренних органов необходимо укреплять естественный иммунитет и проводить своевременную вакцинацию.
Что такое иммунитет и как его повысить?
Одна из главных проблем, связанных со здоровьем человека — наша иммунная система. Кандидат медицинских наук и медицинский директор клиники GMS Тогоев Олег Олегович рассказал FashionTime.ru о тонкостях подхода к основополагающему понятию жизнедеятельности.
— Что такое иммунитет и каковы признаки нарушения его функций?
Иммунитет — это биологическая система защиты организма от инфекций. Если иммунитет выключить, например, на несколько дней, то человек погибнет — сразу же будет съеден микробами. Без иммунитета, как и без почек, организм проживет только несколько дней. Признаки нарушения иммунитета — тяжелое заболевание, инфекция, например, пневмония, остеомиелит, гнойное заболевание костей, внутренних органов, постоянная температура, слабость. Такой человек совсем не может функционировать самостоятельно, он вынужден принимать антибиотики, лежит в больницах. Из известных всем дефектов иммунной системы можно назвать СПИД — синдром приобретенного иммунодефицита. Но есть врожденные иммунодефициты, они не заразные, но в то же время там есть дефект иммунной системы.
— Как правильно организовать собственный режим, чтобы укрепить и поддержать иммунитет?
Иммунитет отражает общее состояние здоровья, силы организма — чем крепче здоровье, тем лучше иммунитет. Все, что укрепляет здоровье, укрепляет иммунитет: режим дня, умеренные нагрузки, режим сна и отдыха, переключение деятельности, избегание переутомлений, избегание гиподинамии — сидения на одном месте, отдых, спорт, закаливание.
— Какие современные средства могут помочь восстановить иммунитет и ресурсы организма? Насколько влияет прием витаминов на состояние организма и какие лучше принимать?
Прием витаминов не влияет никак на иммунитет, а средств, помогающих улучшить состояние иммунитета организма, нет. Иммуноповышающие и иммуноукрепляющие препараты — это профанация. Просто люди хотят верить, что иммунитет можно усилить, что есть волшебные лекарства, а фармацевты рады им такую возможность предоставить. Эти лекарства в большинстве своем не проходили настоящих клинических испытаний. Нет достоверно доказанной эффективности в снижении заболеваемости. То, что продается в аптеках, иммунитет не повышает, можно туда даже за этим не обращаться. Тут легких путей нет — только здоровая еда, здоровый образ жизни, правильный режим дня, правильный режим сна, отдых, активность, свежий воздух могут изменить состояние вашего здоровья.
Но есть случаи, когда витамины действительно нужны, например, беременным женщинам, детям, у которых дефицит веса, или они, например, прибыли из дома ребенка.
— Что делать при переутомлении и упадке сил? Как улучшить состояние организма, есть ли какие-то экстренные и эффективные способы?
При переутомлении нужно отдыхать, менять род занятий, брать отпуск, побольше спать, отодвигать какие-то свои неотложные дела, в чем-то побаловать себя — например, не пойти один день на работу, если есть такая возможность. Витамины здесь не очень хороши — нет доказанной эффективности, что они работают. Витамины есть в пище — сегодня люди питаются полноценно, и если человек живет не в тюрьме и не в детском доме, то, в принципе, он получает все витамины, авитаминоза у него быть не должно.
— Если человек болеет с частотой раз в месяц, значит ли это, что у него проблемы с иммунитетом? Что должно послужить причиной обратиться к врачу?
Поводом обратить свое пристальное внимание на здоровье и обратиться к врачу может стать заболевание, появляющееся в одном и том же месте. Например, если это гайморит или если это 25-й раз пневмония (воспаление в легком), то надо пойти к врачу. Если это ангина, если заболевания стали протекать тяжелее (раньше вы за 3 дня выздоравливали, а теперь за неделю), если кашель не проходит, если нос постоянно заложен или горло постоянно болит, если есть температура и она держится месяц, тогда надо обязательно пойти к врачу.
Частые ОРЗ, особенно у детей, школьников, говорят о том, что иммунитет снижен, но это временное снижение иммунитета. К сожалению, от такого снижения иммунитета средств тоже не существует. И даже при лабораторном обследовании иммунитета у такого человека больших проблем не находят. И бежать исследовать иммунитет — делать иммунограмму — почти всегда бессмысленно.
— Помимо экологии, стресса и вредных привычек что влияет на состояние иммунитета?
Наследственность. Еще может влиять рабочее место, где ты физически проводишь время, — есть ли там окна, есть ли там циркуляция воздуха, много ли там людей одновременно работают, сам режим работы, делаешь ли ты прививки от гриппа или от других болезней.
— Обычно люди придерживаются полярных позиций — кто-то считает, что делать прививки надо, а кто-то не делает их категорически. Каково мнение врачей на этот счет?
Делать прививки надо обязательно! Прививки — огромное достижение человечества, одно из самых важных открытий медицины. И, к счастью, прививок будет больше — сегодня уже находят прививки от новых болезней, даже пытаются найти от гепатита С, может быть, ВИЧ-инфекции и, возможно, от некоторых видов рака.
— Те прививки, которые делали предыдущему поколению, и те, которые делают детям сейчас, принципиально отличаются?
Принципиальных отличий нет, но вакцины стали лучше. Менее реактогенные, но эффект от вакцины такой же. То есть вакцины стали лучше, прививки стали даже безопаснее, чем были. Плюс появились еще новые вакцины.
— Нужно ли принимать жаропонижающие препараты при температуре до 38, или иммунная система должна справиться сама?
Считается, что организм должен справляться сам. Но если вы принимаете жаропонижающие препараты, то лучше себя чувствуете и легче переносите болезнь, можете работать. Для взрослых это важно. Они не хотят быть разбитыми, им проще принять препарат. По большому счету, если вы принимаете жаропонижающий препарат даже при температуре ниже 38, чтобы просто не быть разбитым, вы лишь немного удлиняете заболевание. Если ничего не принимать, то иммунитет выработается быстрее, и вы поправитесь на полдня или день быстрее, чем с приемом жаропонижающих. Но зато в те дни, когда вы болеете, будете ли вы комфортно себя чувствовать? Нужно всегда применять здравый смысл, общих советов в таких вопросах не бывает.
Важно соблюдать ряд предосторожностей во время болезни: не ходить в это время в спортзал, теплее одеваться, уменьшить активность, принимать панадол, нурофен. Порошки типа «Терафлю» и «Колдрекса» тоже не вредны, их также можно принимать.
— Можно ли самостоятельно выбрать в аптеке иммуностимуляторы и прочие специальные лекарства для поднятия иммунитета?
Нет. Иммуностимуляторы вообще не надо покупать. Это трата денег, возможность побочных реакций, пустые ожидания в надежде на результат. Могут быть только проблемы. Слово «иммуностимулятор» нужно забыть.
— Есть какие-то народные или подручные средства, чтобы поддержать организм в холодный период при снижении иммунитета?
Например, если болит горло, больно глотать, то теплое молоко с медом очень хорошо помогает. Если заболели, то все знают, что нужно пить как можно больше — например, клюквенный морс, потому что там есть витамин С. Конечно, радикально он самочувствие не улучшит, но общая польза от него есть. Есть мысль, что если пьешь витамин С, то быстрее поправляешься. Были такие исследования, и витамин приводил быстрее к выздоровлению, но в огромных дозах, которые опасны для почек. А в обычных дозах — никакого эффекта. Но если вы употребляете продукты, содержащие витамин С: лимон, малину, огурцы (в них, как ни странно, много витамина С), шиповник, — это немного может улучшить ваше самочувствие. Потом есть разные народные средства, например, нутряной жир — он прекрасно помогает от болей в горле и уменьшает кашель. Волшебных народных средств, приводящих к быстрому излечению, к сожалению, тоже нет.
Иммунитет
Иммунная система осуществляет защиту организма от инфекционных и неинфекционных чужеродных агентов. При появлении и накоплении в организме клеток, отличающихся генетически, запускается каскад иммунных реакций и формируется иммунный ответ.
Основное назначение иммунной системы — это обезвреживание потенциально опасного антигена и формирование резистентности к нему.
Строение
Иммунная система состоит из совокупности лимфоидных органов и тканей, суммарная масса которых составляет 2% от массы тела и которые разрознены между собой в анатомическом смысле. Однако благодаря наличию медиаторов, сигнальных молекул и клеток, способных к миграции в различные органы и ткани, иммунная система представляет четко организованную структуру в функциональном смысле.
Иммунная система включает центральные и периферические органы. К центральным относят тимус и костный мозг. В этих органах начинается созревание зрелых лимфоцитов.
Периферические органы объединяют селезенку, лимфатические узлы и лимфоидную ткань, печень, кровь, лимфу. Наиболее известными структурами являются миндалины и пейеровы бляшки.
Лимфоциты — основные функциональные клетки иммунной системы. Они образуются в костном мозге, а затем проходят созревание. В зависимости от того, в каком органе лимфоциты проходят созревание, они подразделяются на две гетерогенные популяции: Т-лимфоциты (тимус) и В-лимфоциты (лимфоузлы). Т-лимфоциты ответственны за клеточный иммунитет, В-лимфоциты отвечают за гуморальный. В-лимфоциты являются предшественниками антителообразующих клеток.
Благодаря существованию механизма «иммунологической памяти», иммунный ответ при повторном взаимодействии с теми же антигенами возникает в более короткие сроки и имеет более яркое выражение. Индукция иммунитета является благоприятным исходом иммунных реакций и ведет к восстановлению гомеостаза организма.
Виды иммунитета
Состояние иммунитета обеспечивают наследуемые и индивидуально формируемые механизмы.
К первому относится невосприимчивость человека или определенных видов животных к возбудителям некоторых инфекционных болезней. Например, люди невосприимчивы к возбудителю чумы собак, многие животные — к вирусу кори, гонококку и т.д. Устойчивость к соответствующей инфекции наследуется, как видовой признак, и проявляется у всех представителей данного вида. Это врожденный иммунитет или видовой.
Приобретенный иммунитет формируется в течение всей жизни индивидуума. Примером естественного приобретенного иммунитета является невосприимчивость к инфекции после перенесенного заболевания. Так называемый постинфекционный иммунитет. Например, ветряная оспа.
Приобретенный иммунитет может быть активным и пассивным. Активно приобретенный иммунитет возникает в результате перенесенного инфекционного заболевания или введения в организм вакцины. Пассивно приобретенный иммунитет формируется при передаче антител от матери к плоду или может быть искусственно создан путем парентерального введения в организм готовых иммунореагентов. К ним относят специфические иммуноглобулины, иммунные сыворотки и лимфоциты, способные защитить организм от антигенов.
Иммунитет может быть генерализованным и местным. При местном иммунитете происходит защита покровов организма, которые контактируют с внешней средой: слизистые оболочки мочеполовых органов, желудочно-кишечного тракта и т.д.
Иммунный статус
Характеристику состояния иммунной системы организма, выраженную количественными и качественными показателями ее компонентов, называют иммунным статусом. Определение иммунного статуса проводят с целью правильной постановки диагноза заболевания, прогнозирования его течения и выбора метода лечения.
Что такое иммунитет и нужно ли его «поднимать»?
Для некоторых из нас первые вспышки ОРВИ и необходимость вакцинации от гриппа являются сигналом о том, что нужно бежать в аптеку за чудодейственными лекарствами, которые якобы защитят нас от вирусов и бактерий на протяжении всего холодного сезона. Фармкомпании представляют широкий спектр препаратов подобного рода: иммуномодуляторы, иммуностимуляторы, адаптогены, корректоры, препараты растительного происхождения и синтетические, дорогие и дешевые, в таблетках, каплях, сиропах и т.д. Действительно ли есть необходимость в применении этих средств?
Давайте разберемся, что же такое иммунитет и как он работает.
Дефицит отдельного звена иммунитета приводит к возникновению различных заболеваний. Проявляется он повторными, тяжёлыми, рецидивирующими инфекциями. Нарушение же противоопухолевого иммунитета приводит к развитию злокачественных новообразований. Иногда иммунные клетки начинают разрушать клетки собственного организма, это аутоиммунные заболевания. Когда наша иммунная система чрезмерно реагирует на некоторые вещества, возникают аллергические заболевания.
В здоровом организме слаженно работают все звенья иммунитета: защита от инфекции, противоопухолевый иммунитет, феномен иммунологической толерантности. Равновесие всех трёх звеньев обеспечивает сбалансированную работу иммунной системы, которая у большинства взрослых людей в дополнительной стимуляции не нуждается.
Таким образом, если у человека не диагностирован дефект отдельного звена иммунной системы, нет рецидивирующих длительных бактериальных или вирусных инфекций или тяжелой сопутствующей патологии, целенаправленно «поднимать» иммунитет ему не надо.
Стимуляция иммунитета сегодня – вопрос очень спорный. В западных странах иммуномодуляторы не применяются, так как эффективность этих препаратов не доказана. Лечебное воздействие должно быть направлено на конкретное звено иммунитета, а не на всю иммунную систему. Не существует волшебных таблеток, препаратов, способных укрепить иммунную систему в целом. Для того чтобы создать иммунитет против конкретной инфекции проводится вакцинация, с целью восполнения недостающего звена иммунитета при иммунодефицитах проводят заместительную терапию. Но вариант «поднять иммунитет» с помощью таблеток является лишь ловушкой для доверчивых и ленивых людей, которые хотят быть здоровыми, не прилагая никаких усилий для этого.
Давайте подробнее поговорим о препаратах, которые предлагает нам фармрынок. Большинство среди них (например, рибавирин, эргоферон, ингавирин) – противовирусные, т.е. воздействуют непосредственно на ДНК и РНК вирусов. На иммунитет они воздействуют лишь косвенно. Таким образом, противовирусные препараты необходимы именно при вирусной инфекции! С целью профилактики нужды в их использовании нет!
Если вы вдруг заболели, это вовсе не означает, что «снизился иммунитет». Это указывает на то, что снизились защитные свойства организма, с чем и нужно разбираться, а вот с иммунитетом все в порядке. Иногда мы ошибочно воспринимаем частые ОРВИ за нарушения в работе иммунной системы. Например, в случае с часто болеющими детьми, которые болеют более 4-6 раз в год. На самом деле это может быть обусловлено началом посещения детского сада (дети взаимодействуют с флорой других детей и заболевают, что не является патологией), недолеченной персистирующей инфекций в носоглотке, бесконтрольным приемом антибиотиков, «по каждому чиху». Прием иммуномодуляторов в таком случае переводит инфекцию в подострое течение с периодическими обострениями.
Так чем же мы можем помочь нашей иммунной системе? Иммунитет здорового человека не нуждается во вмешательствах. Необходимо создать условия для его нормальной работы.
Существует несколько рекомендаций, которые помогут поддержать работу иммунитета на нормальном уровне:
1. Не пренебрегайте календарем прививок, в том числе ежегодной вакцинацией против гриппа.
2. Полноценное по количеству и составу питательных веществ, витаминов и микроэлементов (с акцентом на белок, который является основным строительным материалом для клеток иммунной системы).
3. Обеспечьте нормальный ночной сон. Во сне образуются новые иммунные клетки.
4. Необходимо избегать стрессов, поскольку они также ведут к снижению сопротивляемости организма. Мнение о том, что хорошее настроение является залогом здоровья – не миф, ведь наши иммунная, нервная и гормональная системы работают в постоянном взаимодействии.
5. Поддерживайте себя в нормальной физической форме, больше бывайте на свежем воздухе. Хорошее кровообращение позволяет клеткам иммунной системы достичь всех уголков нашего организма и выполнять свою защитную функцию.
6. Своевременно и полностью лечитесь от любых инфекционных заболеваний.
Иммунная система является одной из самых малоизученных систем в организме, поэтому нужно очень разборчиво подходить к вмешательствам в ее работу. Если появились подозрения на серьезное нарушение в работе иммунитета, не откладывайте визит к врачу – возможно, произошла поломка конкретного звена иммунитета, и без специфического лечения не обойтись.
Иммунитет: борьба с чужими и… своими
Автор
Редакторы
Рецензент
Около 5% населения Земли страдают аутоиммунными заболеваниями — состоянием, при котором собственные клетки иммунной системы организма вместо того, чтобы бороться с патогенами, уничтожают нормальные клетки органов и тканей. В этой статье, предваряющей спецпроект по аутоиммунным заболеваниям, мы рассмотрим основные принципы работы иммунной системы и покажем, почему возможна такая диверсия с ее стороны.
Аутоиммунные заболевания
Этой статьей мы начинаем цикл по аутоиммунным заболеваниям — болезням, при которых организм начинает бороться сам с собой, вырабатывая аутоантитела и/или аутоагрессивные клоны лимфоцитов. Мы расскажем о том, как работает иммунитет и почему иногда он начинает «стрелять по своим». Некоторым самым распространенным заболеваниям будут посвящены отдельные публикации. Для соблюдения объективности мы пригласили стать куратором спецпроекта доктора биологических наук, чл.-корр. РАН, профессора кафедры иммунологии МГУ Дмитрия Владимировича Купраша. К тому же у каждой статьи есть свой рецензент, более детально вникающий во все нюансы. Рецензентом этой — вводной — статьи стал Евгений Сергеевич Шилов, кандидат биологических наук, научный сотрудник этой же кафедры.
Партнеры проекта — Михаил Батин и Алексей Маракулин (Open Longevity / «Объединенные Консультанты Финправо»).
Иммунитет — система реакций, призванная защитить организм от вторжения бактерий, вирусов, грибов, простейших и других вредоносных агентов — так называемых патогенов. Если представить, что наше тело — это страна, то иммунную систему можно сравнить с ее вооруженными силами. Чем более слаженным и адекватным будет их ответ на интервенцию патогенов, тем надежнее окажется защита организма.
В мире существует великое множество патогенов, и для того чтобы эффективно бороться со всеми ними, в результате длительной эволюции сформировалась замысловатая система из иммунных клеток, каждая из которых имеет свою стратегию борьбы. Клетки иммунной системы взаимно дополняют друг друга: применяют разные способы уничтожения патогена, могут усиливать или ослаблять действие других клеток, а также привлекать всё новых бойцов на поле битвы, если сами не справляются.
Нападая на организм, патогены оставляют молекулярные «улики», которые «подбирают» иммунные клетки. Такие улики называются антигенами.
Антигены — любые вещества, которые организм воспринимает как чужеродные и, соответственно, отвечает на их появление активацией иммунитета. Самыми важными для иммунной системы антигенами являются кусочки молекул, расположенных на внешней поверхности патогена. По этим кусочкам можно определить, какой именно агрессор напал на организм, и обеспечить борьбу с ним.
Цитокины — азбука Морзе организма
Для того чтобы иммунные клетки могли скоординировать свои действия в борьбе с врагом, им необходима система сигналов, сообщающих, кому и когда вступать в бой, или заканчивать битву, или, наоборот, возобновлять ее, и многое-многое другое. Для этих целей клетками вырабатываются небольшие белковые молекулы — цитокины, например, различные интерлейкины (IL-1, 2, 3 и т.д.) [1]. Многим цитокинам сложно приписать однозначную функцию, однако с некоторой степенью условности их можно разделить на пять групп: хемокины, факторы роста, провоспалительные, противовоспалительные и иммунорегуляторные цитокины.
Упомянутая выше условность классификации означает, что цитокин, входящий в одну из перечисленных групп, при определенных условиях в организме может сыграть диаметрально противоположную роль — например, из провоспалительного превратиться в противовоспалительный.
Без налаженной связи между видами войск любая хитроумная военная операция обречена на провал, поэтому клеткам иммунной системы очень важно, принимая и отдавая приказы в виде цитокинов, правильно их интерпретировать и слаженно действовать. Если цитокиновые сигналы начинают вырабатываться в очень большом количестве, то в клеточных рядах наступает паника, что может привести к повреждению собственного организма. Это называется цитокиновым штормом: в ответ на поступающие цитокиновые сигналы клетки иммунной системы начинают продуцировать всё больше и больше собственных цитокинов, которые, в свою очередь, действуют на клетки и усиливают секрецию самих себя. Формируется замкнутый круг, который приводит к разрушению окружающих клеток, а позже и соседних тканей.
По порядку рассчитайсь! Иммунные клетки
Как в вооруженных силах существуют разные рода войск, так и клетки иммунной системы можно разделить на две большие ветви — врожденного и приобретенного иммунитета, за изучение которых в 2011 году была вручена Нобелевская премия [3], [4], [5]. Врожденный иммунитет — та часть иммунной системы, что готова защищать организм немедленно, как только совершилось нападение патогена. Приобретенный же (или адаптивный) иммунный ответ при первом контакте с врагом разворачивается дольше, так как требует хитроумной подготовки, но зато после может осуществлять более сложный сценарий защиты организма. Врожденный иммунитет очень эффективен в борьбе с единичными диверсантами: он обезвреживает их, не беспокоя специализированные элитные воинские подразделения — адаптивный иммунитет. Если же угроза оказалась более существенной и есть риск проникновения патогена всё глубже в организм, клетки врожденного иммунитета немедленно сигнализируют об этом, и в бой вступают клетки иммунитета приобретенного.
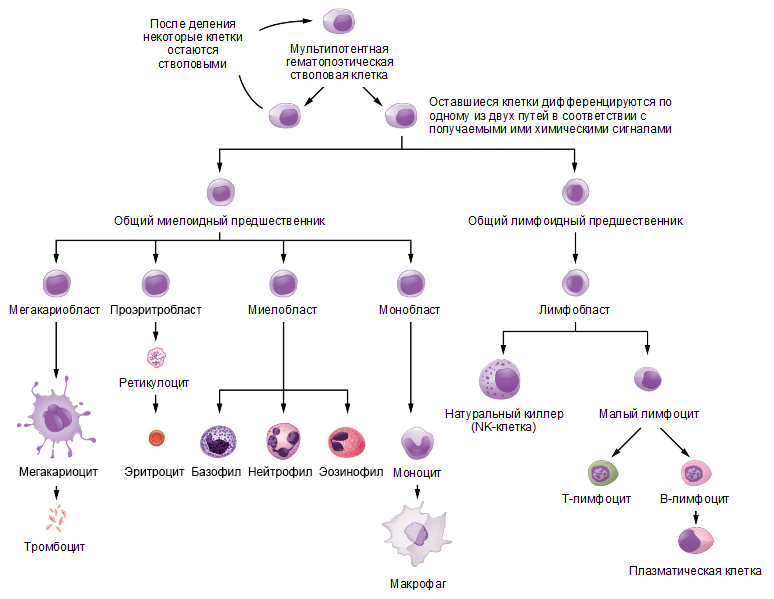
Все иммунные клетки организма образуются в костном мозге от кроветворной стволовой клетки, которая дает начало двум клеткам — общему миелоидному и общему лимфоидному предшественникам [2], [6]. Клетки приобретенного иммунитета происходят от общего лимфоидного предшественника и, соответственно, называются лимфоцитами, тогда как клетки врожденного иммунитета могут брать начало от обоих предшественников. Схема дифференцировки клеток иммунной системы изображена на рисунке 1.
Рисунок 1. Схема дифференцировки клеток иммунной системы. Кроветворная стволовая клетка дает начало клеткам — предшественницам миелоидной и лимфоидной линий дифференцировки, из которых дальше образуются все типы клеток крови.
Сайт opentextbc.ca, рисунок адаптирован.
Врожденный иммунитет — регулярная армия
Клетки врожденного иммунитета распознают патоген по специфичным для него молекулярным маркерам — так называемым образам патогенности [7]. Эти маркеры не позволяют точно определить принадлежность патогена к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с чужаками. Для нашего организма подобными маркерами могут служить фрагменты клеточной стенки и жгутиков бактерий, двухцепочечная РНК и одноцепочечная ДНК вирусов, и т.д. При помощи специальных рецепторов врожденного иммунитета, таких как TLR (Toll-like receptors, Толл-подобные рецепторы) и NLR (Nod-like receptors, Nod-подобные рецепторы), клетки взаимодействуют с образами патогенности и приступают к реализации своей защитной стратегии.
Теперь подробнее рассмотрим некоторые клетки врожденного иммунитета.
Макрофаги и дендритные клетки поглощают (фагоцитируют) патоген, и уже внутри себя при помощи содержимого вакуолей растворяют его. Такой способ уничтожения врага очень удобен: осуществившая его клетка не только может и дальше активно функционировать, но и получает возможность сохранить в себе фрагменты патогена — антигены, которые при необходимости послужат сигналом активации для клеток адаптивного иммунитета. Лучше всего с этим справляются дендритные клетки — именно они работают связистами между двумя ветвями иммунной системы, что необходимо для успешного подавления инфекции.
Видео 1. Нейтрофилы (обозначены зеленым) приходят в очаг повреждения ткани. Видео снято при помощи прижизненной двухфотонной микроскопии.
Эозинофилы, базофилы и тучные клетки выделяют в окружающую ткань содержимое своих гранул — химическую защиту против крупных патогенов, например, паразитических червей. Однако, как это часто бывает, химикатами может отравиться и мирное население, и эти клетки широко известны не столько своей прямой физиологической ролью, сколько вовлеченностью в развитие аллергической реакции.
Помимо вышеупомянутых миелоидных клеток, во врожденном иммунитете работают и клетки лимфоидного ряда, которые так и называются — лимфоидные клетки врожденного иммунитета. Они продуцируют цитокины и, соответственно, регулируют поведение других клеток организма.
Один из типов этих клеток — так называемые натуральные киллеры (natural killers, или NK-клетки). Они — пехота в вооруженных силах организма: борются с зараженными клетками один на один, вступая с ними в рукопашный бой. NK-клетки выделяют белки перфорин и гранзим В. Первый, как следует из названия, перфорирует клеточную мембрану мишени, встраиваясь в нее, а второй, подобно картечи, проникает через эти бреши и запускает гибель клетки, расщепляя белки, ее образующие.
Удивительно, но на разных стадиях своего развития некоторые клетки иммунной системы могут выполнять функции, противоположные друг другу. Так, выделяют гетерогенную группу предшественников различных иммунных клеток врожденного иммунитета, которые в таком незрелом виде подавляют иммунный ответ. Их так и назвали: миелоидные супрессорные клетки. Их количество увеличивается в организме в ответ на появление хронической инфекции или рака. Роль таких клеток очень важна, ведь они не позволяют другим бойцам армии иммунитета слишком сильно бороться с врагом, повреждая тем самым мирное население — ни в чем не повинные клетки, находящиеся поблизости.
Адаптивный иммунитет — спецподразделения вооруженных сил организма
Для того чтобы понять, как работает Т-клеточный рецептор, надо вначале немного обсудить еще одно важное семейство белков — главный комплекс гистосовместимости (MHC, major histocompatibility complex) [9]. Эти белки — молекулярные «пароли» организма, позволяющие клеткам иммунной системы отличать своих соотечественников от неприятеля. В любой клетке постоянно идет процесс деградации белков. Специальная молекулярная машина — иммунопротеасома — расщепляет белки на короткие пептиды, которые могут быть встроены в MHC и, как яблочко на тарелочке, преподнесены Т-лимфоциту. Тот при помощи TCR «видит» пептид и распознает, принадлежит ли он собственным белкам организма или является чужеродным. Одновременно TCR проверяет, знакома ли ему молекула MHC, — это позволяет отличать собственные клетки от «соседских», то есть клеток того же вида, но другой особи. Именно совпадение молекул MHC необходимо для приживления пересаженных тканей и органов, отсюда и такое мудреное название: histos по-гречески означает «ткань». У человека молекулы MHC также называются HLA (human leukocyte antigen — человеческий лейкоцитарный антиген).
Видео 2. Кратковременные взаимодействия Т-клеток с дендритной клеткой (обозначена зеленым). Видео снято при помощи прижизненной двухфотонной микроскопии.
T-лимфоциты
Для активации Т-лимфоцита нужно, чтобы он получил три сигнала. Первый из них — взаимодействие TCR с MHC, то есть распознавание антигена. Второй — так называемый костимуляторный сигнал, передающийся антигенпрезентирующей клеткой через молекулы CD80/86 на СD28, находящуюся на лимфоците. Третий же сигнал — продукция коктейля из множества провоспалительных цитокинов. Если какой-то из этих сигналов ломается, это чревато серьезными последствиями для организма, например, реакцией аутоиммунитета.
Существует два типа молекул главного комплекса гистосовместимости: MHC-I и MHC-II. Первый присутствует на всех клетках организма и несет на себе пептиды клеточных белков или же белков заразившего ее вируса. Специальный подтип Т-клеток — Т-киллеры (их еще называют CD8+ Т-лимфоциты) — своим рецептором взаимодействует с комплексом «MHC-I—пептид». Если это взаимодействие достаточно сильное, значит, пептид, который видит Т-клетка, не характерен для организма и, соответственно, может принадлежать внедрившемуся в клетку врагу — вирусу. Необходимо срочно обезвредить нарушителя границ, и Т-киллер отлично справляется с этой задачей. Он, подобно NK-клетке, выделяет белки перфорин и гранзим, что приводит к лизису клетки-мишени.
Т-клеточный рецептор другого подтипа Т-лимфоцитов — Т-хелперов (Th-клетки, CD4+ T-лимфоциты) — взаимодействует с комплексом «MHC-II—пептид». Это комплекс есть не на всех клетках организма, а в основном на иммунных, и пептиды, которые могут презентироваться молекулой MHC-II, являются фрагментами патогенов, захваченных из внеклеточного пространства. Если Т-клеточный рецептор взаимодействует с комплексом «MHC-II—пептид», то Т-клетка начинает продуцировать хемокины и цитокины, помогающие другим клеткам эффективно осуществлять свою функцию — борьбу с врагом. Потому-то эти лимфоциты и называются хелперами — от английского helper (помощник). Среди них выделяют множество подтипов, которые различаются спектром вырабатываемых цитокинов и, следовательно, ролью в иммунном процессе. Например, существуют Th1-лимфоциты, эффективные в борьбе с внутриклеточными бактериями и простейшими, Th2-лимфоциты, помогающие В-клеткам в работе и потому важные для противостояния внеклеточным бактериям (о чём мы скоро поговорим), Th17-клетки и многие другие.
Видео 3. Движение Т-хелперов (красные) и Т-киллеров (зеленые) в лимфоузле. Видео снято при помощи прижизненной двухфотонной микроскопии.
Среди CD4+ T-клеток существует особый подтип клеток — регуляторные Т-лимфоциты. Их можно сравнить с военной прокуратурой, сдерживающей фанатизм рвущихся в бой солдат и не дающей им причинить вред мирному населению. Эти клетки продуцируют цитокины, подавляющие иммунный ответ, и таким образом ослабляют иммунную реакцию, когда враг повержен.
То, что Т-лимфоцит распознает только чужеродные антигены, а не молекулы собственного организма, является следствием хитроумного процесса, называемого селекцией. Она происходит в специально созданном для этого органе — тимусе, где завершают свое развитие Т-клетки. Суть селекции такова: клетки, окружающие юный, или наивный, лимфоцит, показывают (презентируют) ему пептиды собственных белков. Тот лимфоцит, который слишком хорошо или слишком плохо узнает эти белковые фрагменты, уничтожается. Выжившие же клетки (а это менее 1% всех предшественников Т-лимфоцитов, пришедших в тимус) обладают промежуточным сродством к антигену, следовательно, они, как правило, не считают собственные клетки мишенями для атаки, но имеют возможность среагировать на подходящий чужеродный пептид. Селекция в тимусе — механизм так называемой центральной иммунологической толерантности.
Всё вышесказанное относится к αβ-Т-лимфоцитам, однако существует еще один тип Т-клеток — γδ-T-лимфоциты (название определяет состав белковых молекул, образующих TCR) [11]. Они относительно малочисленны и в основном заселяют слизистую оболочку кишечника и другие барьерные ткани, играя важнейшую роль в регуляции состава обитающих там микробов. У γδ-T-клеток механизм распознавания антигенов отличается от αβ-Т-лимфоцитарного и не зависит от TCR [12].
B-лимфоциты
В-лимфоциты несут на своей поверхности В-клеточный рецептор [13]. При контакте с антигеном эти клетки активируются и превращаются в особый клеточный подтип — плазматические клетки, обладающие уникальной способностью секретировать свой B-клеточный рецептор в окружающую среду — именно эти молекулы мы называем антителами. Таким образом, как BCR, так и антитело имеет сродство к распознаваемому им антигену, как бы «прилипает» к нему. Это дает возможность антителам обволакивать (опсонизировать) клетки и вирусные частицы, покрытые молекулами антигена, привлекая макрофаги и другие иммунные клетки для уничтожения патогена. Антитела также умеют активировать специальный каскад иммунологических реакций, называемый системой комплемента, который приводит к перфорации клеточной мембраны патогена и его гибели.
Для эффективной встречи клеток адаптивного иммунитета с дендритными клетками, несущими в составе MHC чужеродные антигены и поэтому работающими «связными», в организме существуют специальные иммунные органы — лимфоузлы. Распределение их по организму неоднородно и зависит от того, насколько уязвимой является та или иная граница. Бόльшая их часть находится вблизи пищеварительного и дыхательного трактов, ведь проникновение патогена с пищей или вдыхаемым воздухом — наиболее вероятный способ заражения.
Видео 4. Перемещение Т-клеток (обозначены красным) по лимфоузлу. Клетки, образующие структурную основу лимфоузла и стенки сосудов, помечены зеленым флуоресцентным белком. Видео снято при помощи прижизненной двухфотонной микроскопии.
Развитие адаптивного иммунного ответа требует достаточно много времени (от нескольких дней до двух недель), и для того чтобы организм мог защищаться от уже знакомой инфекции быстрее, из Т- и В-клеток, участвовавших в прошлых битвах, формируются так называемые клетки памяти. Они, подобно ветеранам, в небольшом количестве присутствуют в организме, и если появляется знакомый им патоген, вновь активируются, быстро делятся и целой армией выходят на защиту границ.
Логика иммунного ответа
Когда организм атакуют патогены, в бой в первую очередь вступают клетки врожденного иммунитета — нейтрофилы, базофилы и эозинофилы. Они выделяют вовне содержимое своих гранул, способное повредить клеточную стенку бактерий, а также, например, усилить кровоток, чтобы как можно больше клеток поспешило в очаг инфекции.
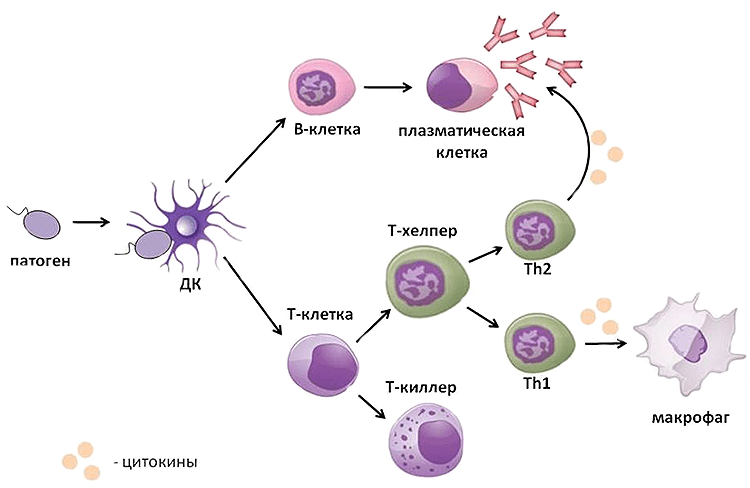
Одновременно с этим дендритная клетка, поглотившая патоген, спешит в ближайший лимфоузел, где передает информацию о нём находящимся там Т- и В-лимфоцитам. Те активируются и путешествуют до местонахождения патогена (рис. 2). Битва разгорается: Т-киллеры при контакте с зараженной клеткой убивают ее, Т-хелперы помогают макрофагам и В-лимфоцитам осуществлять их механизмы защиты. В итоге патоген гибнет, а победившие клетки отправляются на покой. Бόльшая их часть погибает, но некоторые становятся клетками памяти, которые поселяются в костном мозге и ждут, когда их помощь снова понадобится организму.
Рисунок 2. Схема иммунного ответа. Проникший в организм патоген обнаруживается дендритной клеткой, которая движется в лимфоузел и там передает информацию о враге Т- и В-клеткам. Те активируются и выходят в ткани, где реализуют свою защитную функцию: В-лимфоциты продуцируют антитела, Т-киллеры при помощи перфорина и гранзима В осуществляют контактный киллинг патогена, а Т-хелперы продуцируют цитокины, помогающие другим клеткам иммунной системы в борьбе с ним.
Схема составлена автором статьи.
Так выглядит схема любого иммунного ответа, однако она может заметно видоизменяться в зависимости от того, какой именно патоген проник в организм. Если мы имеем дело с внеклеточными бактериями, грибами или, скажем, глистами, то основными вооруженными силами в этом случае будут эозинофилы, В-клетки, продуцирующие антитела, и Th2-лимфоциты, помогающие им в этом. Если же в организме поселились внутриклеточные бактерии, то на помощь в первую очередь спешат макрофаги, которые могут поглотить инфицированную клетку, и Th1-лимфоциты, помогающие им в этом. Ну а в случае вирусной инфекции в бой вступают NK-клетки и Т-киллеры, которые уничтожают зараженные клетки методом контактного киллинга.
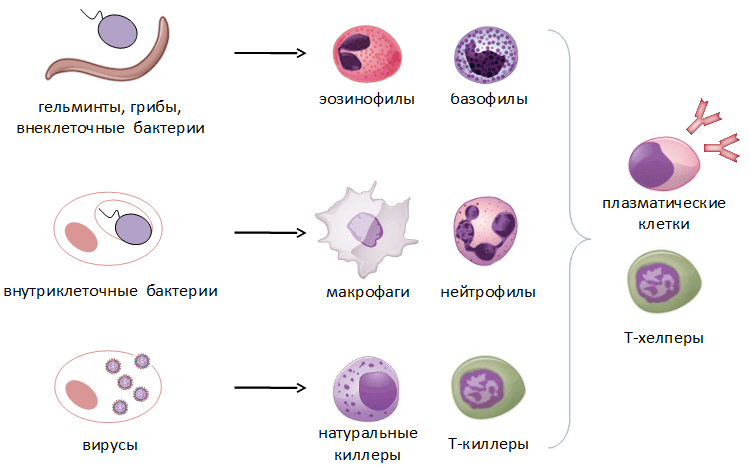
Как мы видим, многообразие типов иммунный клеток и механизмов их действия неслучайно: на каждую разновидность патогена у организма припасен свой эффективный способ борьбы (рис. 3).
Рисунок 3. Основные типы патогенов и клетки, принимающие участие в их уничтожении.
Схема составлена автором статьи.
А теперь все вышеописанные иммунные перипетии — в коротком видео.
Видео 5. Механизм иммунного ответа.
Громыхает гражданская война.
К сожалению, ни одна война не обходится без потерь среди гражданского населения. Долгая и интенсивная защита может дорого стоить организму, если агрессивные высокоспециализированные войска выйдут из-под контроля. Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом [3]. Заболеваниями этого типа страдает около 5% человечества.
Селекция Т-лимфоцитов в тимусе, а также удаление аутореактивных клеток на периферии (центральная и периферическая иммунологическая толерантность), о которых мы говорили ранее, не могут полностью избавить организм от аутореактивных Т-лимфоцитов. Что же касается В-лимфоцитов, вопрос о том, насколько строго осуществляется их селекция, до сих пор остается открытым. Поэтому в организме каждого человека обязательно присутствует множество аутореактивных лимфоцитов, которые в случае развития аутоиммунной реакции могут повреждать собственные органы и ткани в соответствии со своей специфичностью.
За аутоиммунные поражения организма могут быть ответственны как Т-, так и В-клетки. Первые осуществляют непосредственное убийство безвинных клеток, несущих на себе соответствующий антиген, а также помогают аутореактивным В-клеткам в продукции антител. Т-клеточный аутоиммунитет хорошо изучен при ревматоидном артрите, сахарном диабете первого типа, рассеянном склерозе и многих других болезнях.
В-лимфоциты действуют куда более изощренно. Во-первых, аутоантитела могут вызывать гибель клеток, активируя на их поверхности систему комплемента или же привлекая макрофаги. Во-вторых, мишенями для антител могут стать рецепторы на поверхности клетки. При связывании такого антитела с рецептором тот может или блокироваться, или же активироваться без реального гормонального сигнала. Так происходит при болезни Грейвса: В-лимфоциты производят антитела против рецептора к ТТГ (тиреотропному гормону), мимикрируя действие гормона и, соответственно, усиливая продукцию тиреоидных гормонов [14]. При миастении гравис антитела против рецептора к ацетилхолину блокируют его действие, что приводит к нарушению нейромышечной проводимости. В-третьих, аутоантитела вместе с растворимыми антигенами могут образовывать иммунные комплексы, которые оседают в различных органах и тканях (например, в почечных клубочках, суставах, на эндотелии сосудов), нарушая их работу и вызывая воспалительные процессы.
Как правило, аутоиммунное заболевание возникает внезапно, и невозможно точно определить, что стало его причиной. Считается, что триггером для запуска может послужить практически любая стрессовая ситуация, будь то перенесенная инфекция, травма или переохлаждение. Значительный вклад в вероятность возникновения аутоиммунного заболевания вносит как образ жизни человека, так и генетическая предрасположенность — наличие определенного варианта какого-либо гена.
Предрасположенность к тому или иному аутоиммунному заболеванию часто ассоциирована с определенными аллелями генов MHC, о которых мы уже много говорили. Так, наличие аллеля HLA-B27 может служить маркером предрасположенности к развитию болезни Бехтерева, ювенильного ревматоидного артрита, псориатического артрита и других заболеваний. Интересно, что присутствие в геноме того же самого HLA-B27 коррелирует с эффективной защитой от вирусов: например, носители этого аллеля имеют пониженные шансы заразиться ВИЧ или гепатитом С [15], [16]. Это еще одно напоминание о том, что чем агрессивнее воюет армия, тем вероятнее потери среди гражданского населения.
Кроме того, на развитие болезни может влиять уровень экспрессии аутоантигена в тимусе. Например, продукция инсулина и, соответственно, частота презентации его антигенов Т-клеткам различается от человека к человеку. Чем она выше, тем ниже риск развития сахарного диабета первого типа, так как это позволяет удалить специфичные к инсулину Т-лимфоциты.
Все аутоиммунные заболевания можно разделить на органоспецифические и системные. При органоспецифических болезнях поражаются отдельные органы или ткани. Например, при рассеянном склерозе — миелиновая оболочка нейронов, при ревматоидном артрите — суставы, а при сахарном диабете первого типа — островки Лангерганса в поджелудочной железе. Системные аутоиммунные заболевания характеризуются поражением многих органов и тканей. К таким болезням относятся, например, системная красная волчанка и первичный синдром Шегрена, поражающие соединительную ткань. Более подробно об этих заболеваниях будет рассказано в других статьях спецпроекта.
Заключение
Как мы уже убедились, иммунитет — это сложнейшая сеть взаимодействий как на клеточном, так и на молекулярном уровнях. Создать идеальную систему, надежно защищающую организм от атак патогенов и одновременно ни при каких условиях не повреждающую собственные органы, не смогла даже природа. Аутоиммунные заболевания — побочный эффект высокой специфичности работы системы адаптивного иммунитета, те издержки, которыми нам приходится платить за возможность успешно существовать в мире, кишащем бактериями, вирусами и другими патогенами.
Медицина — творение рук человека — не может в полной мере исправить то, что было создано природой, поэтому на сегодняшний день ни одно из аутоиммунных заболеваний полностью не излечивается. Поэтому цели, которых стремится достичь современная медицина, — это своевременная диагностика заболевания и эффективное купирование его симптомов, от которого напрямую зависит качество жизни пациентов. Однако для того чтобы это было возможно, необходимо повысить информированность населения об аутоиммунных заболеваниях и способах их лечения. «Предупрежден — значит вооружен!» — вот девиз общественных организаций, созданных для этого по всему миру.