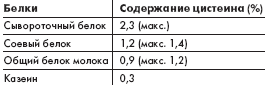интактный протеин что это
Интактный протеин что это
Протеин С; ПС; коагуляционный белок С.
Синонимы английские
Protein C; PC; coagulation protein С.
Кинетический колориметрический метод.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Протеин С является одним из наиболее важных белков – факторов антикоагулянтной (противосвертывающей) системы крови. Синтез данного белка происходит в печени и является витамин К – зависимым. Протеин С находится в постоянной циркуляции в крови в неактивном состоянии. Его активация происходит при воздействии комплекса тромбина и тромбомодулина на поверхности неповрежденных эндотелиальных клеток и тромбоцитов. В активной форме протеин С частично разрушает и инактивирует неферментные факторы свертывания крови Va и VIIIa. Осуществление ферментативного действия протеина С происходит в присутствии его кофактора – протеина S. Он представляет собой витамин К – зависимый неферментный кофактор, синтезируемый в печени и циркулирующий в кровотоке. В результате описанных взаимодействий происходит угнетение процессов свертывания крови, а также косвенно активируются процессы противосвертывающей системы (фибринолиза).
Определение концентрации или активности протеина С в крови является важным в диагностике различных патологических состояний и заболеваний. Снижение данных показателей может быть связано с нарушением синтеза протеина С, его быстрым расходованием или с нарушением структуры белка и его функциональной неполноценностью. Синтез протеина С может быть снижен в результате врождённой недостаточности, дефицита витамина К, при патологиях печени, нарушении ее синтетической функции, в период новорождённости и у пожилых людей. Чрезмерное расходование белка может отмечаться при тромбозах, тромбоэмболиях, коагулопатиях потребления, синдроме диссеминированного внутрисосудистого свертывания (ДВС-синдроме), после обширных операций и травм. Нарушение функциональной активности протеина С может наблюдаться при приеме антикоагулянтных препаратов, в частности при пероральном приеме варфарина. Повышение концентрации протеина С может отмечаться при беременности, при приеме пероральных контрацептивов на основе эстрогенов, при заболеваниях почек.
Врождённая недостаточность протеина С встречается в 0,2-0,5 % случаев, характеризуется тяжелым течением. Она требует проведения профилактических и лечебных мероприятий для предупреждения развития тромбозов и фатальных осложнений. Редкий вариант гомозиготного дефицита протеина С проявляется молниеносным ДВС-синдромом у новорождённых и требует неотложных диагностических мероприятий и лечения.
У беременных женщин дефицит протеина С приводит к ряду тяжелых патологических процессов и осложнений. Могут развиваться тромбозы и тромбоэмолии с поражением глубоких вен нижних конечностей, органов малого таза, сосудов головного мозга, возможно осложнение в виде тромбоэмболии легочной артерии. Может отмечаться внутриутробная задержка развития плода в результате фетоплацентарной недостаточности, спонтанные аборты и повторные выкидыши. Увеличивается риск развития преэклампсии, эклампсии и ДВС-синдрома.
При приеме антикоагулянтов непрямого действия и при значительном снижении активности протеина С до или менее 50 % от нормы могут развиваться некрозы кожи. Такие «варфариновые некрозы» развиваются редко, но характеризуются тяжелым течением и требуют тщательного врачебного контроля. Следовательно, рекомендуется проводить лечение непрямыми антикоагулянтами под контролем активности протеина С. Контрольные и повторные определения протеина С необходимо осуществлять не менее чем через месяц после отмены препаратов.
Основными проявлениями дефицита протеина С являются артериальные и венозные тромбозы различной локализации. Могут отмечаться инфаркты миокарда, инсульты, тромбоэмболия легочной артерии при отсутствии других предрасполагающих факторов и у лиц молодого возраста. Определение концентрации/активности протеина С также может быть рекомендовано при онкологических заболеваниях, гнойно-воспалительных заболеваниях, при сепсисе и септических процессах.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Причины повышения уровня протеина С:
Причины понижения уровня протеина С:
Что может влиять на результат?
Прием антикоагулянтных препаратов непрямого действия, варфарина.
Кто назначает исследование?
Терапевт, врач общей практики, гематолог, гинеколог, неонатолог, педиатр, акушер-гинеколог, хирург, анестезиолог-реаниматолог.
Смеси на основе пептидов у больных с патологией желудочно-кишечного тракта: современные позиции
За последние 20 лет распространенность болезней пищеварительного тракта значительно возросла. В структуре болезней детского населения преобладают хронические воспалительные заболевания желудочно-кишечного тракта (ЖКТ) [1, 5–7].
За последние 20 лет распространенность болезней пищеварительного тракта значительно возросла. В структуре болезней детского населения преобладают хронические воспалительные заболевания желудочно-кишечного тракта (ЖКТ) [1, 5–7].
Принципиально важным моментом в комплексе общей терапии пациентов с указанной патологией является своевременное назначение патогенетически обоснованного питания [2, 3, 7]. К наиболее распространенным заболеваниям пищеварительной системы, при которых используется лечебное питание, относятся язвенная болезнь желудка, 12-перстной кишки, хронический панкреатит и т. д. Часто течение этих и других заболеваний сопровождается формированием синдрома мальабсорбции и развитием мальдигезии.
На сегодняшний день установлено, что для сохранения нормальной функции слизистой оболочки различных отделов кишечника, экзокринной функции поджелудочной железы и других желез пищеварительного тракта необходимо поступление питательных субстратов в просвет ЖКТ. Нутриенты, поступающие энтеральным путем, создают условия для роста и регенерации эпителия, нормализуют, а в ряде случаев восстанавливают функциональную активность кишечника, способствуют нормализации выработки энтеральных гормонов [4, 5].
Существует целый ряд клинических ситуаций (синдром короткой кишки, нарушение нормальных взаимоотношений процессов всасывания и секреции воды и электролитов, изменения, гастриты с секреторной недостаточностью, выраженные изменения функций печени, поджелудочной железы, гипокинезии желчного пузыря, панкреатит и т. д.), когда применение традиционного лечебного питания не всегда успешно [2, 7].
Преимуществами специализированного питания перед традиционной диетотерапией являются:
Среди немалого разнообразия продуктов для энтерального и перорального применения особое внимание затрагивают продукты с умеренно или полностью гидролизованным белком (полуэлементные диеты). Пептидные смеси лучше всасываются и усваиваются организмом, чем питание на основе цельных белков или свободных аминокислот [11–13].
Поэтому полуэлементные диеты рекомендованы для клинического применения у большинства пациентов с нарушенной функцией ЖКТ.
Существуют три формы белка, в которых он может присутствовать в смесях для энтерального питания:
Согласно современным научным представлениям, форма белка, поступающего с пищей в организм человека, страдающего болезнями органов пищеварения, может иметь особенное значение для всасывания и усвоения этого питательного вещества и оказать влияние на общее состояние системы пищеварения больного [11, 15, 17]. По мнению большинства исследователей, для больных с нарушениями пищеварения и всасывания в качестве источника белка предпочтительна диета на основе пептидов.
Большая часть белка в форме пептидов и свободных аминокислот всасывается активным транспортом в тощей кишке. По современным оценкам, примерно две трети (30–75%) азота всасывается в виде пептидов [20]. Многие аминокислоты всасываются в кишечнике, в основном, в форме пептидов, а не как свободные аминокислоты [13, 14]. Свободные аминокислоты переносятся специфическими системами активного транспорта, в то время как пептиды имеют самостоятельные механизмы всасывания [12–14].
Фактические данные указывают на то, что при некоторых заболеваниях, таких как белково-энергетическая недостаточность и целиакия, нарушается всасывание аминокислот, но пептиды всасываются нормально [8, 22, 23]. Имеются данные о прямом всасывании более крупных нерасщепленных пептидов [22]. В обзоре механизмов всасывания белка в кишечнике описываются два потенциальных пути всасывания пептидов — чрезклеточный и параклеточный (межклеточный) [13, 20]. При чрезклеточном всасывании пептиды проникают в кровь через мембраны ворсинок, используя следующие механизмы: транспортные системы с участием молекул-переносчиков, водные поры, диффузию через липидные участки в мембранах и пиноцитоз. Чрезклеточный путь — основной путь всасывания пептидов. При параклеточном всасывании молекулы пептидов могут проходить между ворсинками стенки кишечника, возможно, в тех точках, где есть дефекты. Повышению всасывания азота у больных с нарушениями работы ЖКТ может в значительной степени способствовать питание на основе пептидов, предполагающее использование механизмов переноса как аминокислот, так и пептидов.
Таким образом, основными показаниями для назначения полуэлементных смесей в терапевтической практике являются заболевания органов пищеварения, ассоциированные с метаболическим синдромом, диареей, нарушениями внешнесекреторной функции поджелудочной железы, недостаточностью питания, ранний послеоперационный период, связанный с оперативными вмешательствами на органах ЖКТ, а также с ослабленной иммунной системой, белково-энергетической недостаточностью.
Одними из современных полуэлементных продуктов, используемых у пациентов с заболеваниями органов пищеварения, следует выделить питательные смеси «Пептамен Юниор» (Peptamen Junior ® ) для детей с 1-го года до 10 лет и для лиц, старше 10 лет, — «Пептамен» (Peptamen ® ), которые могут использоваться как для перорального, так и энтерального зондового питания.
Белковый компонент смесей технологически создан на основе пептидов (олигопептидов, полученных при гидролизе сывороточных белков).
Сывороточный белок обладает высокой питательной ценностью и отличается большим содержанием незаменимых аминокислот.
Сравнение содержания аминокислот в сывороточном белке Пептамена с нормами, рекомендованными ФАО/ВОЗ (ФАО — Продовольственная и сельскохозяйственная организация ООН (Food and Agriculture Organization), свидетельствует в пользу этой смеси на основе пептидов [19].
При сравнении эффектов смесей на основе гидролизатов молочных белков и аминокислот, имеющих один и тот же аминокислотный состав, отмечено, что по питательной ценности пептидная диета превосходила аминокислотную. Это можно объяснить тем, что пептиды более равномерно всасываются и имеют более однородный состав на момент доставки их к тканям, тогда как аминокислоты усваиваются ими неравномерно. Различия в кинетике аминокислот, по-видимому, и обусловливают более низкую питательную ценность питания на их основе. Питание на основе пептидных смесей также является хорошим источником цистеина. Цистеин — предшественник глютатиона, являющегося в организме главным антиоксидантом. Глютатион играет ключевую роль в обезвреживании чужеродных веществ и нейтрализации молекул реакционноспособного кислорода и свободных радикалов [18, 28, 32] Свободные радикалы участвуют в окислительном стрессе, влекущем за собой гибель клеток и повреждение тканей. Глютатион, синтезируемый в печени, представляет собой трипептид, состоящий из глутамата, глицина и цистеина. Поскольку концентрация цистеина в печени ниже, чем концентрация двух других аминокислот, цистеин ограничивает скорость производства глютатиона. Поэтому поступление с пищей достаточного количества цистеина будет способствовать образованию глютатиона и, следовательно, усилению антиоксидантной защиты организма [18, 28] Данные по содержанию цистеина в обычных пищевых белках приведены в таблице [18].
Из данных табл. видно, что самым лучшим из указанных белковых источников цистеина, используемых в смесях для энтерального питания, является сывороточный белок.
Пептидная диета также оказывает благотворное действие на работу печени. Последствиями нарушения работы печени могут быть снижение иммунной функции, эффективности переработки эндогенных продуктов обмена веществ и способности организма к синтезу жизненно важных белков. Имеющиеся на сегодня данные свидетельствуют о том, что пептидная диета более эффективно поддерживает работу печени и, следовательно, способствует висцеральному синтезу белков. Висцеральный белковый статус оценивают путем измерения концентраций отдельных транспортных белков, синтезируемых в печени (альбумина, трансферрина и преальбумина), уровень которых, как было показано, отражает нутритивный статус организма в целом.
Жировой состав смеси Пептамен представлен среднецепочечными и длинноцепочечными триглицеридами (50% medium chain triglycerides (МСТ), 50% long chain triglycerides (LCT)), что улучшает усвоение смеси в желудочно-кишечном тракте, а также позволяет назначать в ранние сроки после операций, в том числе на желудочно-кишечном тракте, при ограниченном усвоении жиров у пациентов в критических состояниях с нарушениями функции пищеварительной системы. Всасывание МСТ не требует дополнительных ферментативных усилий, что обеспечивает функциональный относительный покой печени и поджелудочной железы. В состав жирового компонента входят эссенциальные жирные кислоты (линолевая и альфа-линоленовая), что позволяет добиться максимального усвоения смеси при хорошей энергетической обеспеченности. В смесях содержатся L-карнитин, необходимый для полноценного усвоения жирных кислот, и таурин — эссенциальная аминокислота для больных, получающих интенсивную терапию.
Углеводный компонент сформирован смесью мальтодекстринов с различным декстрозным эквивалентом (степенью гидролиза). Такое соотношение углеводных компонентов обеспечивает невысокую осмолярность (280 мОсм/л) и хорошие органолептические свойства продукта. Смесь имеет сбалансированный витаминно-минеральный состав, что делает возможным ее применение в течение длительного времени. К настоящему времени проведен целый ряд клинических исследований, посвященных изучению эффективности применения смеси Пептамен (Peptamen ® ) в качестве лечебного питания у разных категорий больных. В работе McClave S. A. et al. была показана безопасность и эффективность диеты на основе пептидов сывороточного белка при остром панкреатите [24]: Пептамен, вводимый через тощую кишку, столь же эффективно, как и парентеральное питание, снимал стресс, вызванный панкреатитом. В группе Пептамена отмечена тенденция к снижению продолжительности пребывания в стационаре и отделении интенсивной терапии, а также длительности периода до перехода к физиологическому приему пищи и восстановления нормального уровня амилазы. У хирургических больных, получавших Пептамен [18], отмечено статистически значимое улучшение показателей концентрации преальбумина и холестерина и уровня трансферрина. А у больных, оперированных на брюшной полости [32], периферическая биодоступность аминокислот была достоверно выше и более гомогенной на пептидной диете, чем на смесях на основе цельных белков
В другой работе, посвященной задержке опорожнения желудка у детей [19], было показано, что у больных, получающих смесь на основе сывороточного белка, отмечено снижение частоты рвоты по сравнению с теми, кто получал казеиновую смесь. Смеси на основе сывороточного белка снижают частоту рвоты за счет ускорения опорожнения желудка.
Анализ клинической эффективности использования полуэлементной смеси у разных групп пациентов с патологией ЖКТ указывает на результативность использования пептидных диет, использование которой предпочтительно для больных с нарушениями работы ЖКТ. Данные клинических и экспериментальных исследований, в том числе тех, в которых изучали всасывание азота и кинетику, позволяют сделать следующие выводы относительно энтерального питания больных с нарушением функции ЖКТ:
Смеси на основе пептидов превосходят смеси на основе свободных аминокислот, так как при их переваривании и всасывании задействуются все транспортные системы, как пептидные, так и аминокислотные, в результате чего максимально повышается всасывание азота.
Смеси на основе пептидов превосходят смеси на основе свободных аминокислот или цельных белков, так как содержащийся в них азот легко всасывается и поступает к тканям в обычной физиологический форме, что способствует синтезу белков, а не катаболизму.
Таким образом, проведенные исследования с использованием смеси Пептамен (Peptamen ® ) у больных с нарушением работы желудочно-кишечного тракта показали следующие преимущества пептидных смесей:
Протеин С
Прием биоматериала по данному исследованию может быть отменен за 2-3 дня до официальных государственных праздников, в связи с технологической особенностью производства! Информацию уточняйте в контакт-центре.
Добавить в корзину
Дефицит протеина С (врожденный или приобретенный) приводит к состоянию гиперкоагуляции и развитию венозных тромбоэмболических осложнений. Используется для выявления риска развития тромбозов, в том числе при подготовке к плановым оперативным вмешательствам, подборе оральных контрацептивов у женщин, а также при невынашивании беременности.
Активированный протеин С — это особый вид белка в организме человека. В крови он содержится в активном и неактивном состоянии. Формируется этот белок в печени — основой для его выработки является витамин К. Если коагулянты крови способствуют её свёртыванию, то данный белок, в комплексе с другими, участвует в процессах её разжижения.
Описание исследования
Обычно протеин С (другие его названия — фактор коагуляции XIV, аутопротромбин IIА) находится в неактивном состоянии и начинает действовать лишь на поверхности эндотелия, когда его активируют коагулянты крови, в частности, тромбин в комплексе с тромбомодулином. Полураспад активной формы белка занимает 20–30 минут, а неактивной — длится намного дольше (5–6 часов).
Протеин С в комплексе с другими белками участвует в процессе поддержания крови в жидком состоянии. Также он оказывает эффективное противовоспалительное действие и принимает участие в процессе отмирания клеток организма. Низкий уровень протеина С в крови может спровоцировать развитие состояния гиперкоагуляции и развитие тромбоэмболии в венах. Если повышен протеин С в крови, это свидетельствует о заболевании почек или о наступившей беременности.
По сравнению с антитромбином III уровень Протеин С не так тесно коррелирует с риском ухудшения проходимости сосудов, но его уменьшение усиливает действие остальных факторов, приводящих к данному заболеванию.
Показания к исследованию крови на протеин С
Результаты этого лабораторного анализа используются для:
Узнать концентрацию протеинов С в крови необходимо при:
Дефицит этого антикоагулянта может быть приобретённым (острым или хроническим) и врождённым. В ходе диагностики последнего изучают степень активности белка, а только после этого количественный состав. Дефицит передаётся независимо от половой принадлежности всем потомкам. В этом случае коагулянты крови не встречают должного противодействия и способствуют возникновению тромбозов кожных сосудов, а у молодых людей локация заболевания может быть крайне опасной — лёгочная артерия.
Вероятность появления спонтанного тромбоза коррелирует с типом носительства дефицита.
Гетерозиготный проявляет себя, в основном, после полового созревания. Оно ослабляет ответ организма на терапию, направленную на разжижение крови, провоцирует образование сгустков в сосудах. Науке известны свыше 200 мутаций этого белка, что также является фактором, провоцирующим тромбообразование.
При нехватке Протеин С факторами риска ухудшения проходимости сосудов являются:
Интерпретация результатов
Увеличение содержания и активности данного белка не связывают с проблемами со здоровьем.
Уменьшение активности и уровня Протеин С свидетельствует о повышенном риске тромбоза, так как коагулянты крови не ограничены в своём действии.
Его снижение наблюдается при:
В «МобилМед» качественно и быстро определят содержание протеина С в вашей крови.
ОБЩИЕ ПРАВИЛА ПОДГОТОВКИ К АНАЛИЗАМ КРОВИ
Кровь берется из вены. Необходимо соблюдать общие рекомендации:
Интактный протеин что это
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Протеин S – белок плазмы крови, относящийся к системе физиологических антикоагулянтов (веществ, препятствующих свертыванию крови). Он синтезируется в печени, эндотелиальных клетках и мегакариоцитах. Синтез протеина S протекает с участием витамина К. Протеин S циркулирует в крови в двух формах: свободной (около 40 % от общего количества) и в комплексе с регуляторным белком системы комплемента (C4b-binding Protein) – около 60 % соответственно. Доли свободной и связанной форм протеина S регулируются количеством С4bBP. Антикоагулянтной активностью обладает только свободный протеин S. Он ускоряет разрушение протеином С активированных V и VIII факторов свертывания, тем самым приводя к угнетению тромбообразования. Таким образом, протеин S играет важную роль в предотвращении излишнего образования тромбов: при его дефиците баланс в свертывающей системе крови сдвигается в сторону гиперкоагуляции. Недостаточность протеина S может носить приобретенный или наследственный характер.
Степень увеличения риска тромботических осложнений при приобретенном дефиците неизвестна. Снижение плазменной концентрации свободного протеина S может происходить при аутоиммунных, острых воспалительных заболеваниях или обострении хронических. Это объясняется увеличением уровня С4-компонента комплемента и, соответственно, С4b-переносящего белка (С4bBP) – доля связанного с ним протеина S увеличивается, а свободного – снижается. При болезнях почек, сопровождающихся нефротическим синдромом, также нарушается соотношение между свободной и общей формами протеина S из-за потерь свободной через почки. Тяжелые поражения печени, гиповитаминоз витамина К, терапия варфарином приводят к нарушению витамин К – зависимого синтеза протеина S, однако в связи с наличием других локаций синтеза протеина S значительного его дефицита в этом случае не отмечается. Уровень протеина S может также снижаться при беременности, однако это не обязательно приводит к тромботическим событиям.
Гораздо более серьезное клиническое значение имеет наследственный дефицит протеина S. Ген, кодирующий данный белок, находится на третьей хромосоме. К настоящему моменту описано около 200 различных его мутаций. Недостаточность протеина S наследуется аутосомно-доминантно и является редким заболеванием. Человек получает от каждого из родителей по одному варианту (аллелю) гена протеина S. Если мутация имеет место в обоих аллелях, говорят о гомозиготной форме заболевания. Она встречается крайне редко (на данный момент в литературе описано всего два случая), проявляется у новорождённых и характеризуется развитием тяжелого диссеминированного свертывания крови – молниеносной пурпурой. При гетерозиготном варианте один из аллелей нормальный, а второй отсутствует или имеет мутацию, что приводит к синтезу только 50 % нормального протеина S (количественная и качественная недостаточность). Мутация в одном из аллелей приводит к синтезу дефектного белка, который не может выполнять свою антикоагулянтную функцию. Гетерозиготный дефицит протеина S в 10 раз увеличивает риск возникновения венозных и артериальных тромбозов, а также различных осложнений беременности (повторные выкидыши, преэклампсия, эклампсия, задержка внутриутробного развития плода).
В зависимости от содержания в крови общего количества протеина S и его свободной формы, различают три типа наследственного дефицита:
I и III являются наиболее распространенными типами и могут быть диагностированы при исследовании уровня свободного протеина S.
Уровень свободного протеина S исследуется с помощью метода иммунотурбидиметрии. Метод основан на классическом взаимодействии антиген-антитело. К исследуемой плазме добавляется первый латексный реагент, на поверхности которого адсорбирован С4bBP. Он с высоким сродством связывается со свободным протеином S, и этот комплекс запускает реакцию агглютинации со вторым латексным реагентом, содержащим моноклональное антитело против человеческого протеина S. Образовавшиеся агглютинаты изменяют мутность реакционной среды, которая будет прямо пропорциональна концентрации свободного протеина S в исследуемом образце плазмы. Это детектируется специальным фотометрическим прибором, который пересчитывает параметры изменения оптической плотности в цифры концентрации свободного протеина S.
Для чего используется исследование?
Исследование назначается для выявления дефицита протеина S, прежде всего наследственного характера. Несмотря на то что тактика ведения острого тромботического события не зависит от выявленного наследственного дефицита протеина S, его диагностика важна для проведения в последующем профилактических мер, которые позволят минимизировать риск повторных тромбозов.
Когда назначается исследование?
При комплексной диагностике тромбофилии, при наличии эпизодов артериальных или венозных тромбозов, а также тромбоэмболических осложнений, которые не имеют каких-либо других очевидных причин, особенно если они возникают у людей молодого возраста (моложе 50 лет), носят семейный характер, а также постоянно рецидивируют. Определение уровня свободного протеина S целесообразно также при комплексной диагностике причин развития тромботических осложнений в период беременности.
Что означают результаты?
Повышенный уровень свободного протеина S обычно не связан с медицинской проблемой и считается клинически незначимым.
Снижение свободного протеина S наблюдается при врождённом дефиците, заболеваниях печени с нарушением ее синтетической функции, нефротическом синдроме, синдроме диссеминированного внутрисосудистого свертывания крови, некоторых системных заболеваниях (красная волчанка), лечении L-аспарагиназой, приеме непрямых антикоагулянтов (антагонистов витамина К), приеме эстрогенов (оральные контрацептивы), во время беременности и в послеродовом периоде.
Кто назначает исследование?
Гематолог, акушер-гинеколог, ангиохирург, генетик, врач общей практики, терапевт.