индуцированная атрезия фолликулов что это
Индуцированная атрезия фолликулов что это
Далеко не все растущие фолликулы сохраняются до овуляции. Обычно у женщины овулирует лишь один фолликул в каждые четыре недели. Однако обследование яичника, перед тем как должна наступить овуляция, выявляет присутствие нескольких развитых фолликулов. К концу периода своего роста все фолликулы, кроме одного, внезапно прекращают развитие и начинают испытывать регрессивные изменения.
Дегенерация фолликулов называется атрезией. Атрезия фолликулов происходит не только у тех животных, которые обычно рождают лишь одного детеныша. Среди животных, у которых множественные роды являются правилом, фолликулы также образуются в избытке и редуцируются при помощи атрезии, после чего овулирует только такое количество яйцеклеток, которое соответствует числу детенышей, обычному для потомства данного вида.
Иногда у женщины избегают атрезии не один, а два или больше фолликулов. Если в это время произошло совокупление, сопровождавшееся оплодотворением, то возникает несколько эмбрионов.
Желтое тело
История фолликула отнюдь не заканчивается выделением содержавшегося в нем яйца. В яичнике остается большое количество фолликулярных клеток и соединительнотканная оболочка, окружавшая фолликул до его разрыва. Эти структуры начинают участвовать в развитии желтого тела. Желтое тело, называемое так из-за своего желтого цвета, видимого на свежем материале, в течение некоторого времени быстро увеличивается в объеме и становится органом внутренней секреции.
Другими словами, оно продуцирует секрет, который не выделяется через протоки, как при обычной секреции, а поступает непосредственно в кровяное русло. Секрет, диффундирующий из железы, не имеющей протоков, кровеносные сосуды и разносимый током крови в другие части организма, где он проявляет определенное физиологическое действие, называется гормоном.
Возможное влияние данного гормона, продуцируемого желтым телом, на подготовку слизистой оболочки матки к восприятию и имплантации зародыша является вопросом, к которому мы еще вернемся позднее в связи с половым циклом. Сейчас мы рассмотрим лишь происхождение и строение самого желтого тела.
При разрыве фолликула, вытекании большей части жидкости и сжатии стромы яичника размер просвета фолликула уменьшается. Кровотечение из мелких кровеносных сосудов, поврежденных при разрыве фолликула, может частично наполнить спавшуюся полость кровью, которая вместе с остатком фолликулярного содержимого быстро превращается в сгусток. Лопнувший фолликул, наполненный полужидким материалом кровянистого цвета, называется геморрагическим тельцем (corpus haemorrhagicum).
Недавние исследования показали, что в дополнение к небольшому количеству крови, появившемуся в результате кровотечения, вызванного разрывом фолликула, имеет место вторичная геморрагия из мелких сосудов в желтое тело во время следующей затем менструации.
Сгусток в центре вновь образованного желтого тела вскоре начинает прогрессивно уменьшаться под воздействием фагоцитирующих лейкоцитов. Вместе с этим фолликулярные клетки stratum granulosum сильно увеличиваются как в числе, так и в размере и прорастают в область, занятую раньше сгустком. В то же время мелкие сосуды из соединительнотканной оболочки пронизывают увеличившуюся массу фолликулярных клеток и разветвляются среди них.
Эти сосуды доставляют с собой множество мелких клеток, происходящих из внутренней оболочки фолликула, которые начинают располагаться среди более заметных фолликулярных клеток, образовавшихся из stratum granulosum. Таким образом, в создании желтого тела участвуют оба слоя фолликулярной стенки, хотя наиболее заметные и характерные клеточные элементы образуются из фолликулярных клеток stratum granulosum. Желтое тело в норме развивается из каждого прорвавшегося фолликула, но если освободившаяся яйцеклетка не будет оплодотворена, то оно вскоре дегенерирует. Если же произойдет оплодотворение и зародыш имплантируется в матку, то желтое тело будет расти и существовать очень долго, прежде чем дегенерирует. Это различие в судьбе желтых тел отражено в названии недолговечных желтых тел желтыми телами овуляции, а тех, которые существуют дольше, — желтыми телами беременности. Их гистологическая структура почти одинакова, и различие, вероятно, скорее количественное, чем качественное.
При дегенерации желтого тела регрессивные изменения носят фиброзный характер — клеточная часть органа распадается, а ее место занимает волокнистая соединительная ткань. Последняя разрастается, уплотняется и постепенно принимает характерный белесоватый вид рубцовой ткани. Наконец на том месте, где был вначале фолликул, а затем желтое тело, остается лишь сморщенный участок рубцовой ткани, называемый corpus albicans.
Прорыв в лечении бесплодия
Прорыв в лечении бесплодия
Овуляция и дальнейшее оплодотворение возможны при наличии в яичниках женщины абсолютно жизнеспособных фолликулов
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Процент женщин, лишенных радости материнства, с каждым годом возрастает. Среди причин бесплодия всё чаще выделяют первичную недостаточность яичников (ПНЯ). Данная патология заключается в отсутствии фолликулов или нарушении их созревания в ответ на гормональную стимуляцию. Решение проблемы эндокринного бесплодия вследствие синдрома истощения яичников предложили ученые из США и Японии. Им удалось активировать фолликулы яичников в условиях in vitro и имплантировать фрагменты ткани в верхний отдел фаллопиевых труб, что дает женщине шанс стать матерью.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучшее новостное сообщение».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Корни проблемы
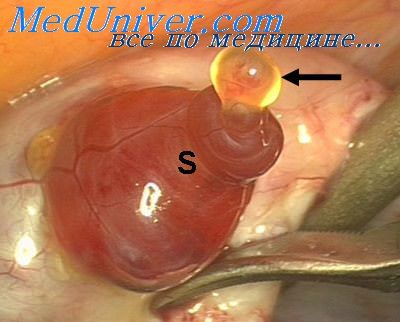
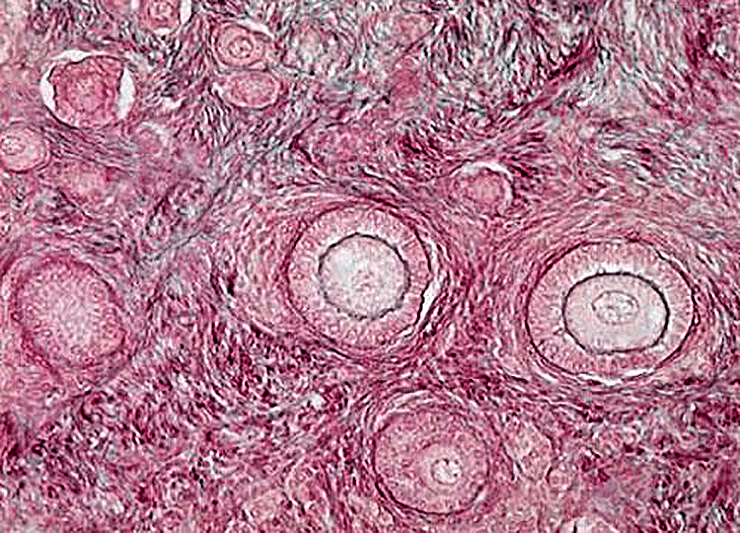
Яичник — уникальная эндокринная система, в которой ежемесячно возникает новая секреторная структура — граафов фолликул (рис. 1). Он развивается из микроскопического примордиального фолликула, потенциальная функциональность которого и определяет регулярность менструального цикла женщины.
Рисунок 1. Фолликулы яичников
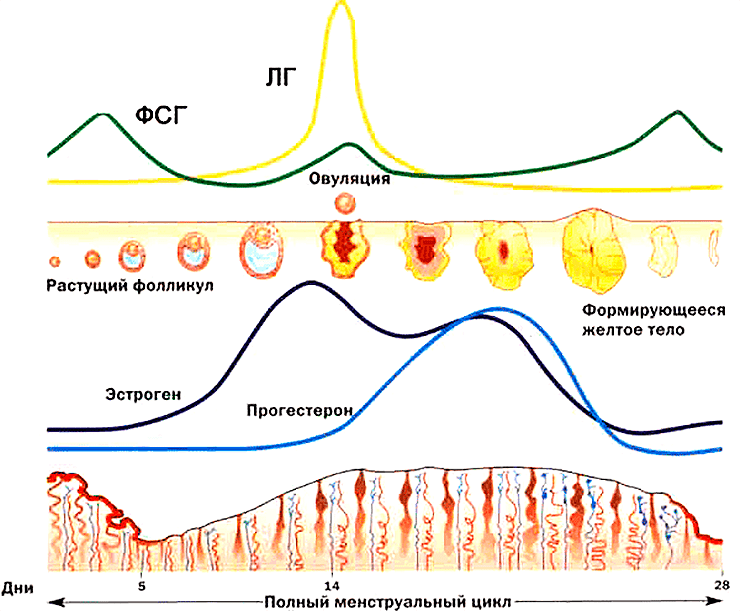
Функция яичников регулируется двумя гормонами гипофиза: фолликулостимулирующим гормоном (ФСГ) и лютеинизирующим гормоном (ЛГ) (рис. 2). В свою очередь, яичники продуцируют гормоны, регулирующие секрецию ФСГ и ЛГ по принципу отрицательной обратной связи: эстрогены, ингибины и прогестерон [1].
Рисунок 2. ФСГ стимулирует рост и созревание фолликула в яичнике. ЛГ стимулирует выход созревшей яйцеклетки из фолликула (овуляцию).
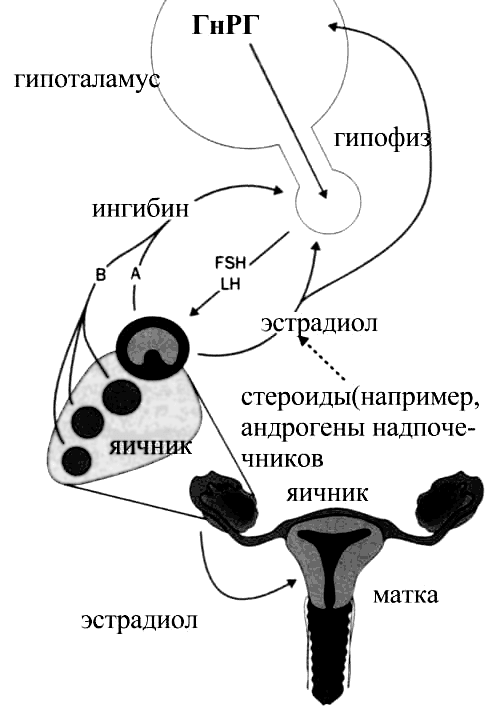
При недостаточности функции яичников для поддержания снижающейся концентрации яичниковых гормонов происходит резкое повышение секреции гонадотропинов. За их выработку отвечает гипоталамус (рис. 3).
Рисунок 3. Связь функционирования яичников с эндокринной системой
Причины, приводящие к развитию первичной недостаточности яичников (ПНЯ), весьма гетерогенны: генетические, ферментативные, аутоиммунные, инфекционно-токсические, психогенные. Кроме того, в эту группу относят и дефекты в структуре гонадотропинов. В последние годы большое внимание исследователей уделяется молекулярно-генетическим аспектам этой патологии яичников, поскольку выявлен определенный набор генов, который может отвечать за развитие ПНЯ.
Стоит отметить, что термин «первичная недостаточность яичников» в настоящее время применяется для определения состояния, которое ранее называли «преждевременной менопаузой». Ключевое различие заключается в том, что термин «ПНЯ», предложенный еще в 1942 году, характеризует нарушение функции яичников в динамике, а не конечное состояние, что наблюдается при менопаузе [1].
Диагностика
Яичниковая недостаточность диагностируется по повышенному уровню ФСГ и ЛГ в крови при сниженном уровне эстрогенов. Самый чувствительный гормон — ФСГ; он является самым ранним маркером преждевременного старения яичников. При двукратном превышении уровня ФСГ (20 Ед/л) наступление и благополучный исход беременности маловероятны.
Клинические характеристики состояния: аменорея (отсутствие менструации) ≥4 месяцев у женщин моложе 40 лет, бесплодие и повышение уровня ФСГ до менопаузальных значений (дважды с промежутком не менее 1 месяца).
Частота спонтанной недостаточности яичников у женщин с хромосомным набором 46 ХХ составляет около 1%; при этом эпидемиологические исследования указывают на тесную связь данного нарушения с возрастом. Так, у женщин в возрасте до 20 лет ПНЯ встречается с частотой 1:10000, а в возрасте от 30 до 40 — 1:1000.
Что происходит на гормональном уровне
Один из половых гормонов — 17β-эстрадиол (рис. 4), который играет важную роль в выполнении репродуктивной функции женщины, — вырабатывается преимущественно в яичниках из мужских половых гормонов — андростендиона и тестостерона [2]; небольшое количество этого гормона также вырабатывается надпочечниками. В процессе угасания функций яичников количество растущих фолликулов в них уменьшается, что приводит к значительному понижению выработки 17β-эстрадиола. Поэтому у женщин с так называемым синдромом истощения яичников наблюдается нехватка этого гормона, которая частично компенсируется большей выработкой 17β-эстрадиола в надпочечниках. Так как менструации становятся нерегулярными, уровень 17β-эстрадиола начинает колебаться, и с прекращением менструаций резко понижается, что приводит к повышению фолликулостимулирующего гормона (ФСГ).
Рисунок 4. β-эстрадиол (кристаллы). Поляризация LM X100.
Механизм активации незрелых фолликулов
Для женщин, страдающих бесплодием по причине рассмотренного заболевания, существует единственная возможность материнства — имплантация оплодотворенной донорской яйцеклетки. Однако группа специалистов из Стэнфордского университета (США) и Медицинского факультета Университета им. Святой Марианны (Япония) предложили альтернативу — метод, позволяющий исключить известные хирургические вмешательства для стимуляции овуляции, такие как клиновидная резекция яичников или лазерное сверление. Врачи удалили яичники у участниц исследования, поделили их на несколько частей, а затем воздействовали на фрагменты яичников препаратами, стимулирующими рост. Спустя несколько дней некоторые из фрагментов ткани были имплантированы в фаллопиевы трубы женщин. Затем специалисты наблюдали за развитием фолликулов. У некоторых участниц исследования сформировались зрелые яйцеклетки, что позволило провести им стандартную процедуру экстракорпорального оплодотворения (ЭКО [3]). Результаты исследования опубликованы в журнале Proceedings of the National Academy of Sciences [4].
Важно отметить, что возможность провести подобное лечение возникла благодаря изучению сигнального клеточного пути под названием Hippo [5], который представляет собой один из ключевых компонентов регуляции таких важных процессов, как контактное ингибирование роста клеток и связанного с ним контроля размера внутренних органов [6]. Первоначально белковый комплекс Hippo был открыт у дрозофил. Мухи, у которых его функционирование было нарушено, буквально увеличивались в размерах (из-за чего регулятор и получил своё название: «Hippo» происходит от слова «гиппопотам»). Затем его обнаружили и у млекопитающих.
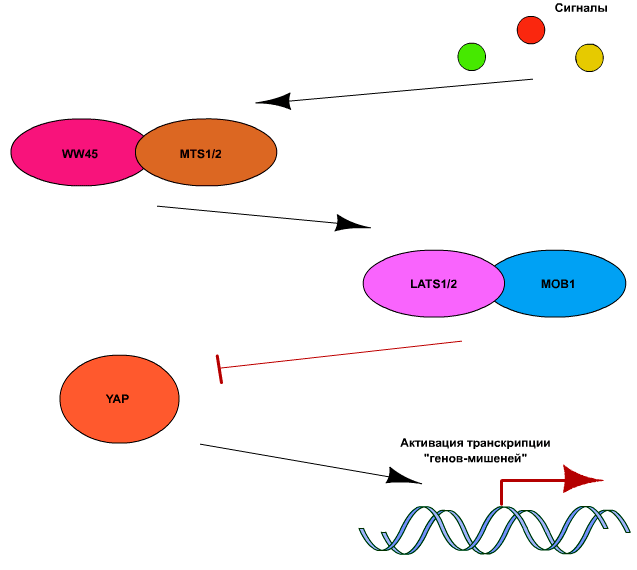
Ключевым компонентом пути Hippo является киназа Yap (Yes-activated protein), которая в активном состоянии способна связывать ряд факторов транскрипции, таких как p73, p53-binding protein-2 (p53BP2), RUNX2, SMAD7, ERBB4, PEBP2а и TEAD/ТЕF [7]. Регуляция активности YAP осуществляется в основном за счет ингибирующего действия киназ LATS1 и 2 (large tumor supressor-1 и −2). Они, в свою очередь, активируются киназами МSТ1 и МSТ2 (mammalian sterile-20-like kinases). Для полной активации LATS и МSТ необходимо также, чтобы они были связаны с адапторными белками WW45 и МОB1, соответственно. Вышеописанная часть сигнального пути Hippo является высококонсервативной у млекопитающих, в то время как сигналы активации или ингибирования LATS и МSТ могут быть достаточно разнообразными. В общих чертах сигнальный путь Hippo представлен на рис. 5.
Рисунок 5. Схематичное изображение работы сигнального белкового регулятора Hippo
Развитие эмбриона, деление эмбриональных клеток и рост тканей и органов эволюционно контролируются работой различных регуляторов. По словам одного из авторов исследования Арона Сюэ (Aaron Hsueh) — акушера-гинеколога из Стэнфордского Университета в Калифорнии — у женщин с синдромом истощения яичников наблюдается повышенная активность регулятора Hippo [8]. Другими словами, он блокирует созревание практически всех фолликулов яичника, что минимизирует возможность наступления овуляции и дальнейшего оплодотворения.
Ученые нарушили работу сигнального пути Hippo в удаленных яичниках и, таким образом, предотвратили преждевременную остановку развития фолликулов. Далее специалисты стимулировали активность другого сигнального пути, называемого Akt, что способствовало ускорению роста фолликулов [9], [10].
Клинические исследования проводились сначала на лабораторных животных. На следующем этапе в эксперименте согласились принять участие 27 женщин, страдающих от первичной дисфункции яичников. В ходе исследования выяснилось, что у некоторых женщин в яичниках не было фолликулов. В яичниках 13 пациенток обнаружили незрелые фолликулы; из них у восьми женщин применение нового метода лечения способствовало росту жизнеспособных фолликулов. Для 14 женщин лечение оказалось неэффективным.
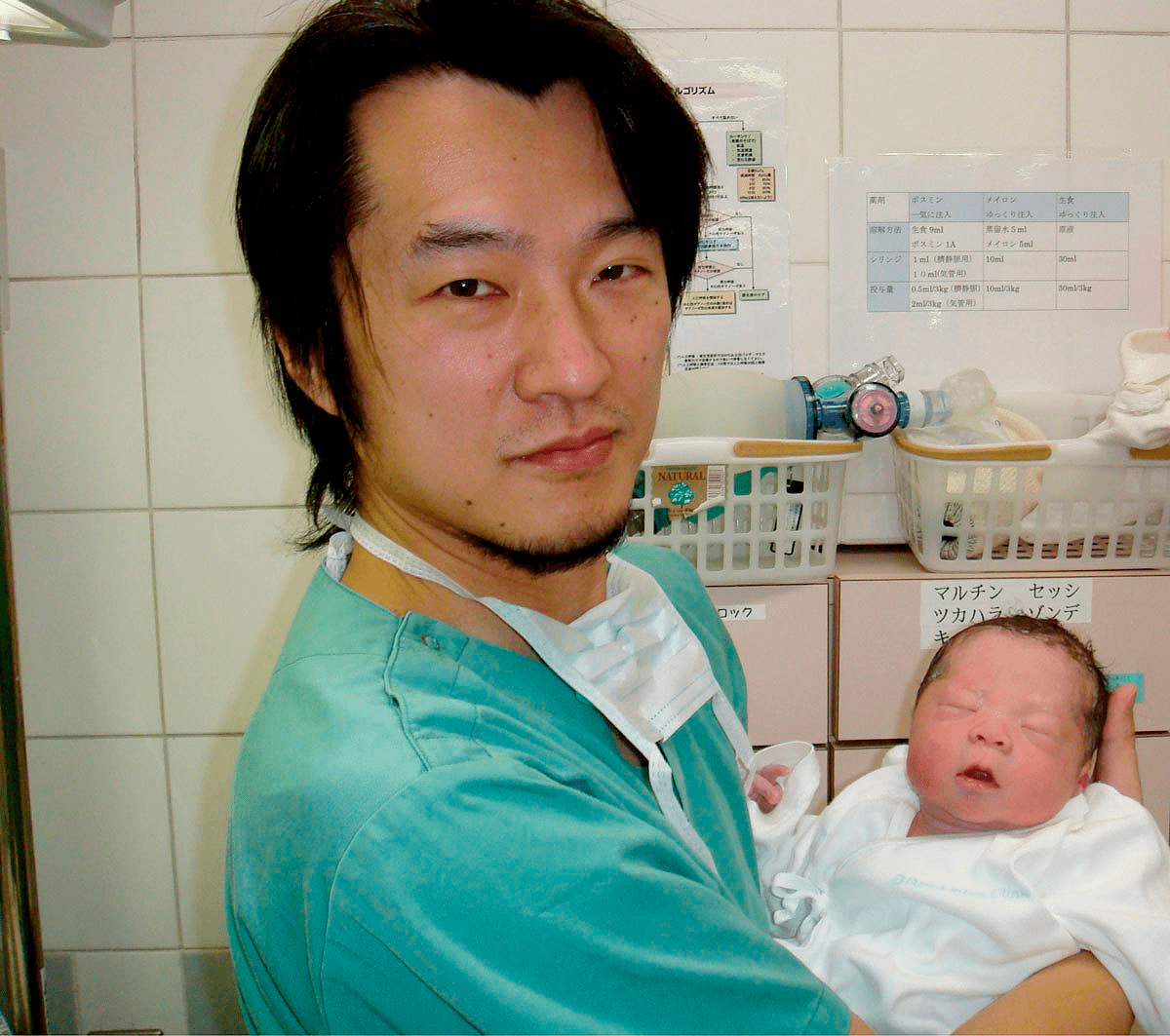
В результате зрелые яйцеклетки были получены у пяти женщин и использованы для ЭКО. Одна из пациенток в возрасте 29 лет во время курса лечения на 37 неделе беременности родила ребенка весом 3,3 кг (рис. 6). Научная группа надеется, что эффективность нового метода лечения достигнет 30%. И, более того, по их словам, этот метод может также помочь женщинам, перенесшим лучевую или химиотерапию, и пациенткам в возрасте лет с нерегулярным менструальным циклом [11].
Рисунок 6. Казухиро Кавамура (Kazuhiro Kawamura) — один из ученых, участвовавший в исследовании — держит на руках новорожденного мальчика, которого родила первоначально бесплодная женщина
Мнения и прогнозы
По мнению Марчелле Цедарса (Marcelle Cedars) — специалиста в области репродуктивной онкологии из Университета Калифорнии в Сан-Франциско — исследователи поторопились апробировать новый метод лечения бесплодия на человеке: «Ученые продемонстрировали рождение здорового потомства при проведении предварительных исследований на мышах, но не было получено доказательств роста, развития и/или плодовитости этого поколения» [12].
Авторы исследования полагают, что метод подходит бесплодным женщинам среднего возраста, а также тем, кому диагностировали первичную недостаточность яичников, вследствие которой в более чем 50% случаев беременность не наступает. Однако не все эксперты разделяют их оптимизм. Руководитель врачебной группы, изучающей оплодотворение, из Университета Южной Калифорнии Ричард Паульсон (Richard Paulson) убежден, что ключевое условие эффективности разработанного механизма лабораторной «активации» фолликула — наличие в нем здоровой яйцеклетки. Кроме того, Паульсон заостряет внимание на том, что неразумно сопоставлять результаты лечения женщины в возрасте 29 лет с результатами лечения женщины в 40 лет, поскольку гормональная стимуляция роста и развития фолликулов в разные возрастные периоды происходит с различной интенсивностью.
Рассмотренный консервативный метод стимуляции овуляции путем блокировки сигнального пути Hippo в отдельных фрагментах ткани яичников может быть полезен женщинам, больным раком или проходящим процедуры стерилизации. Но все же главное достижение ученых — это рождение ребенка у женщины, которая без их участия никогда не смогла бы стать матерью.
Фолликулогенез и современная овариальная стимуляция (обзор литературы).
| Несмотря на то, что со времени публикации последнего нашего обзора прошло только пять лет, в научной литературе, посвященной фолликулогенезу и овариальной стимуляции, накопилось достаточно материала для того, чтобы поделиться им с заинтересованным читателем [35]. |
Миграция первичных половых клеток из эндодермы желточного мешка в гонады начинается с 7—8-й нед беременности, и к 16 нед в яичниках девочки определяются ооциты. К 5-му месяцу беременности число половых клеток достигает максимума (около 7 млн), после чего происходит массивная атрезия фолликулов, и ко времени родов их остается около 1 млн. К менархе в яичниках остается от 270 до 500 000 фолликулов [36]. В яичнике женщины определяются фолликулы на различных стадиях развития [1]:
Примордиальный (I стадия) [6] — ооцит частично или полностью окружен уплощенными клетками гранулезы, размер фолликула около 30—40 мкм.
Первичный (II стадия) [6] — ооцит окружен одиночным слоем кубических клеток гранулезы.
Ранний вторичный — неполный второй слой кубических клеток гранулезы.
Вторичный (III стадия) [6] — два полных слоя клеток гранулезы, размер фолликула около 50 мкм.
Преантральный (1-й класс) [6] — ооцит увеличен в объеме и окружен более чем двумя слоями гранулезы без образования полости, размер фолликула около 100 мкм.
Антральный (2—8-й класс) [6] — ооцит увеличен в объеме и окружен несколькими слоями клеток гранулезы с образованием полости. Размер фолликула более 0,2 мм в диаметре.
Рост фолликулов от примордиальной стадии до овуляции доминантного фолликула остается наиболее важной частью исследований в репродукции человека. За жизнь у женщины в норме овулируют около 400 фолликулов, остальные подвергаются атрезии на различных стадиях. Фолликулогенез можно разделить на следующие стадии: 1) формирование пула растущих фолликулов; 2) базальный рост (рост до стадии антрального фолликула 4-го класса); 3) селекция и созревание доминантного фолликула. Зависимость первых двух этапов от гипофизарных гонадотропинов, преимущественно от ФСГ, является непрямой и скорее опосредована внутрияичниковыми факторами, и лишь последний этап напрямую регулируется гипофизом.
Точное время роста фолликулов от примордиаль ной стадии до овуляции трудно установить, что в первую очередь связано со сложностью определения начала роста и дифференцировки фолликулов, а также достаточной продолжительностью начальных этапов роста фолликула. По различным данным, гормональ но-независимый этап роста фолликулов длится от 180 до 300 сут и гормонально-зависимый до 50 сут [5].
1. Формирование пула растущих фолликулов (продолжается более 120 сут)
Особый интерес вызывает механизм выхода фолликулов из состояния покоя (рис. 1). Факторы, определяющие начало роста и дифференцировки примордиальных фолликулов, до сих пор не определены, однако ряд авторов высказывают предположение о том, что это некий внутрияичниковый гормонально-неза висимый фактор, связанный с образованием межклеточных контактов и поддерживающий фолликулы в состоянии покоя. Культивирование отделенных друг от друга фолликулов в среде ведет к их росту и дифференцировке. Эти данные позволяют предположить, что потеря межклеточных контактов может быть пусковым фактором начала дифференцировки. Данная теория получила название теории латеральной спецификации (lateral specification) [2]. Согласно данной гипотезе, в рост идут те фолликулы, которые потеряли боковой контакт с соседними фолликулами, и обычно рост фолликулов происходит по краю яичника, а также в районе недавно образовавшегося желтого тела. Эта гипотеза объясняет наблюдения, что при делеции фолликулов при старении увеличивается относительное число растущих фолликулов. Как один из кандидатов на роль этого фактора, отвечающего за потерю межклеточных контактов и начала дифференцировки, был предложен продукт экспрессии гена Notch, один из вариантов которого был выделен из яичника мыши [2]. О гормонально-независимом характере начала роста фолликулов также говорит тот факт, что он происходит в аваскулярной зоне.
Процесс выхода примордиальных фолликулов из состояния покоя происходит постоянно и зависит от возраста женщины. Так, в возрасте 24—25 лет ежедневно уходят в рост около 50 примордиальных фолликулов, в 34—35 лет — около 17 фолликулов, в 44—45 лет — только около 3 фолликулов [6]. При исчезновении последних фолликулов в яичнике женщины наступает менопауза.
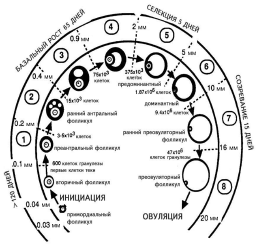 |
| Рис. 1. Стадии развития фолликулов. |
Также указаны размеры фолликулов и количество клеток гранулезы. Рисунок воспроизведен из работы A. Gougeon [16].
Большинство фолликулов подвергается атрезии на стадии малых антральных фолликулов [7]. Следует отметить, что в 37—38 лет к данному механизму атрезии прибавляется выраженная атрезия собственно примордиальных фолликулов, что значительно убыстряет процесс исчезновения фолликулов из яичника [6].
Также в ооците продуцируются морфогенетический протеин кости 15 и 6, фактор роста фибробластов 8, ТФР-b2. Роль этих факторов в фолликулогенезе еще недостаточно определена и ждет дальнейших исследований [4, 5].
2. Базальный рост (рост до стадии антрального фолликула 4-го класса)
Эта стадия, несмотря на то что продолжается около двух менструальных циклов (около 65 дней), является также малоизученной, и лишь немного известно о факторах, определяющих рост фолликулов на данной стадии. По данным гистологического исследования, в начале этой фазы преантральные фолликулы, размером 0,1—0,2 мм и содержащие около 3,5 тыс. клеток гранулезы, начинают активно расти. Происходит процесс дифференцировки гранулезы на клетки предшественники пристеночного слоя и кумулюса, постепенно образуются лакуны, которые затем объединяются и образуют антральную полость (см. рис. 1, рис. 2).
Большой интерес в современной литературе уделяется антимюллеровому гормону (antimulleran hormone, mullerian-inhibiting substance), который играет важнейшую роль в эмбриогенезе мужской особи млекопитающих и продуцируется клетками Сертоли, что вызывает регрессию органов мюллерова протока (маточных труб, матки и верхней части влагалища). Однако роль данного гормона не ограничивается эмбриогенезом. Выяснилось, что антимюллеровый гормон играет роль в фолликулогенезе и определяется в яичниках девочки с 32-й недели беременности и во взрослом состоянии продуцируется клетками гранулезы фолликулов [9]. Показано, что концентрация этого гормона с молекулярной массой около 72 кДа мало зависит от фазы цикла и, возможно, отражает число фолликулов, находящихся в базальной фазе роста. Это делает данный гормон уникальным маркером старения яичников и овариального резерва, а также позволяет говорить о его ценности в диагностике синдрома поликистозных яичников [10—12].
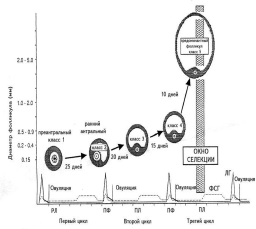 |
| Рис. 2. Динамика развития фолликулов в стадии базального роста. |
ПФ — поздняя фолликулярная фаза цикла, РЛ — ранняя лютеиновая фаза, ПЛ — поздняя лютеиновая фаза цикла. Рисунок воспроизведен из работы A. Gougeon [16].
3. Селекция и созревание доминантного фолликула
Данный этап фолликулогенеза можно разделить на следующие этапы: формирование пула малых антральных фолликулов и их рост, селекция доминантного фолликула и собственно овуляция.
Гормонально-зависимая стадия фолликулярного роста начинается в конце лютеиновой фазы цикла, когда снижение уровня эстрадиола, прогестерона и ингибинов А и В вызывает повышение уровня ФСГ. Под воздействием этого подъема фолликулы 5-го класса, размером около 2—5 мм в диаметре начинают интенсивно расти (см. рис. 1).
В последние годы сложное взаимодействие различных факторов роста и цитокинов на этапе созревания доминантного фолликула было изучено подробно.
Эпидермальный фактор роста (ЭФР) и ТФР-a играют важную роль в пролиферации клеток гранулезы антральных фолликулов, размером от 1 до 5 мм, и в то же время защищают фолликулы от воздействия на их гранулезу ФСГ. Этот механизм позволяет фолликулам достаточно долго находиться на данной стадии, например при беременности и при длительном воздействии агонистов люлиберина (при лечении эндометриоза и миомы матки), а также способствует формированию пула данных фолликулов. Снижение концентрации ЭФР и ТФР-a в фолликулах более 4—5 мм в диаметре позволяет ФСГ воздействовать на гранулезу этих фолликулов [17, 18]. В то же время концентрация ТФР-b с увеличением диаметра фолликула от 2 до 20 мм возрастает, что позволяет говорить об антагонизме между воздействием на гранулезу фолликулов ЭФР и ТФР-a, с одной стороны, и ТФР-b, с другой [16].
Крайне важной представляется роль ИПФР I и II в фолликулогенезе, селекции доминантного фолликула и атрезии фолликулов. В исследованиях последних лет выяснилось, что высокие концентрации ИПФР I и II способствуют воздействию ФСГ на клетки гранулезы. В атретических фолликулах наблюдается повышенная концентрация протеинов, связывающих инсулиноподобные факторы роста (ИПФРСП), и в первую очередь ИПФРСП-4. Однако действие этого фактора в яичниках может быть заблокировано специфиче ской протеазой, которая недавно выделена из клеток гранулезы фолликулов и желтого тела человека. Специфической протеазой к ИПФРСП-4 оказался протеин, ранее известный как ассоциированный с беременностью сывороточный белок А (pregnancy-associated plasma protein-A — PAPP-A) [5]. Тонкое взаимодействие ИПФР I и II, а также белков, связывающих эти факторы, и их протеаз является важным направлением в изучении фолликулогенеза, а также таких состояний, как синдром поликистозных яичников, инсулинорезистентность и овариальная стимуляция.
Большое значение в последние годы уделяется васкулярному эндотелиальному фактору роста. Выяснилось, что рост сосудов и васкуляризация играют важнейшую роль в росте доминантного фолликула. Исследования с помощью цветной допплерультрасо нографии показали, что только фолликулы с хорошей васкуляризацией способны продуцировать жизнеспособные ооциты в программах ЭКО [19, 20].
Роль цитокинов в фолликулогенезе до конца не изучена, однако известно, что интерлейкин-1 b является антиапоптотическим фактором, вызывая продукцию в гранулезе преовуляторных фолликулов оксида азота [21].
В последние годы роль ингибинов и активинов в регуляции менструального цикла изучена основатель но. Ингибины представляют собой димерные белки, состоящие из цепи альфа и бета. Предшественник цепи альфа (про-a-С), ранее считавшийся собственно ингибином и выявляемый в крови в высоких концентра циях, не обладает высокой активностью и в настоящее время не определяется. Цепь бета имеет два варианта: А и В. Каждый из этих вариантов может быть ковалентно соединен с цепочкой альфа и соответст венно образовать ингибины альфа-бета А (ингибин А) и альфа-бета В (ингибин В). Молекулярная масса обоих ингибинов составляет примерно 31—32 кДа. Две цепочки бета могут образовывать димеры, которые называются активинами, и соответственно существуют активины А, В и АВ. Основная роль ингибинов состоит в подавлении выделения ФСГ в передней доле гипофиза, в то время как активины способствуют выбросу ФСГ. Синтез ингибинов и активинов обнаружен в головном мозге человека, плаценте, костном мозге, гипофизе, яичках и яичниках, однако у взрослой женщины главным источником этих гормонов являются клетки гранулезы фолликулов. Долгое время оставалось загадочным то, как регулируется уровень ФСГ в начале менструального цикла женщины. Предположения о том, что это может происходить под воздействием эстрадиола, не оправдались, так как уровень синтеза этого гормона в фолликуле значителен только после достижения фолликулом диаметра 10 мм и более. В последние годы благодаря работам группы N. Groome из Оксфордского университета выяснилось, что клетки гранулезы предоминантных фолликулов (до 10 мм в диаметре) продуцируют ингибин В, и именно он регулирует продукцию ФСГ в начале и середине менструального цикла. В то же время доминантный фолликул и желтое тело продуцируют ингибин А и эстрадиол, которые в свою очередь ингибируют выделение ФСГ гипофизом (рис. 3).
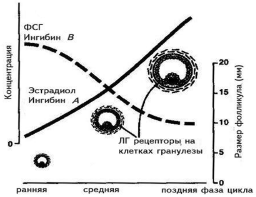 |
| Рис. 3. Изменения в концентрации основных гормонов в фолликулярной фазе цикла и механизм селекции доминантного фолликула. |
Рисунок воспроизведен из работы D. Baird [39].
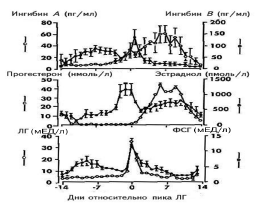 |
| Рис. 4. Концентрации ингибинов А и В, эстрадиола, прогестерона, ФСГ и ЛГ в зависимости от фаз менструального цикла. |
Данные представлены в зависимости от овуляторного пика ЛГ. Рисунок воспроизведен из работы N. Groome и соавт. [22].
Знания о взаимодействии традиционных гормонов (ФСГ, ЛГ, эстрадиол и прогестерон) и новых (ингибины А и В) значительно обогащают наши представления о регуляции менструального цикла женщины и должны использоваться в учебном процессе как врачей гинекологов, так и специалистов общей практики (рис. 4) [22].
Двухклеточная теория стероидогенеза в яичниках остается наиболее важной теоретической базой, на которой строится современная регуляция менструаль ного цикла и индукция суперовуляции. Согласно современной интерпретации этой теории, в растущих фолликулах начала менструального цикла синтез андрогенов (тестостерона и других) из холестерола происходит в клетках теки фолликулов под воздействием стимулирующего действия ЛГ. В то же время в клетках гранулезы фолликулов из тестостерона происходит синтез эстрадиола с помощью фермента ароматазы. Главным стимулятором ароматазы является ФСГ, который действует через свой аденилатциклазный рецептор. Уровень синтеза эстрадиола в фолликулах до 10 мм в диаметре остается невысоким. При достижении доминантным фолликулом более 10 мм в диаметре на клетках гранулезы яичников появляются рецепторы не только к ФСГ, но и к ЛГ. Под воздействием стимуляции ФСГ и ЛГ синтез эстрадиола значитель но увеличивается.
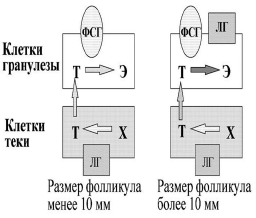 |
| Рис. 5. Двухклеточная теория синтеза эстрадиола в зависимости от размера фолликулов. |
Т — тестостерон; Х — холестерол; Э — эстрадиол.
Высокая концентрация эстрадиола в крови вызывает по принципу отрицательной обратной связи снижение выделения ФСГ гипофизом (см. рис. 3, рис. 5). Под воздействием снижающегося уровня ФСГ все фолликулы, которые не успели достигнуть 10 мм в диаметре, подвергаются атрезии. В то же время уровень синтеза эстрадиола в доминирующем фолликуле растет экспоненциально и строго коррелирует с диаметром фолликула. При достижении фолликулом овуляторного диаметра (16—23 мм) высокий уровень эстрадиола вызывает по принципу положительной обратной связи пик ЛГ и овуляцию фолликула. Данный механизм лежит в основе селекции доминантного фолликула не только человека, но, вероятно, и других моноовулярных млекопитающих [23, 24].
В конце 70-х годов прошлого века исследователя ми было отмечено, что при овариальной стимуляции препаратами кломифенцитрата и чМГ растущие фолликулы продуцируют высокий уровень эстрадиола, который в естественном цикле мог бы вызвать по принципу положительной обратной связи выброс ЛГ и преждевременную лютеинизацию фолликулов. Однако этот выброс часто не происходит до достижения фолликулами преовуляторных размеров 15—20 мм. Предположено, что фолликулы продуцируют некую субстанцию, ингибирующую выброс ЛГ. Установле но, что данное биологически активное вещество по своим свойствам и структуре отличается от ингибинов и выделяется клетками гранулезы в ответ на стимуляцию ФСГ. Лишь в середине 90-х годов XX века эта субстанция была охарактеризована и получила название фактор отмены пика гонадотропинов — ФОПК (Gonadotropin Surge — Attenuating/Inhibiting Factor, LH-RH Attenuating Factor) [13]. Найдено, что активность этого вещества в фолликулярной жидкости зависит от размеров фолликула и максимальна в фолликулах от 5 до 15 мм в диаметре, после чего резко снижается [14]. Также установлено, что присутствие ФОПК может отражать качество фолликулов, и у женщин со сниженным овариальным резервом фолликулы продуцируют низкую активность данного фактора, что может объяснять частую раннюю лютеиниза цию фолликулов у таких пациенток [15].
Появление в начале 60-х годов минувшего столетия первых препаратов, содержащих ФСГ [человеческий менопаузальный гонадотропин (чМГ) и человеческий гипофизарный гонадотропин (чГГ)], позволило проводить лечение пациенток с хронической ановуляцией. Основываясь на этих работах, J. Brown (1978) и D. Baird (1987) предложили теорию роста и селекции доминантного фолликула, получившую название теории окна [31, 38] (рис. 6). Согласно этой теории, для роста антральных фолликулов 3—5 мм в начале фолликулярной фазы цикла уровень ФСГ должен преодолеть определенное значение, так называемый порог. Уровень данного порога строго индивидуален и скорее всего зависит от овариального резерва (уровня базального ФСГ). В нормальном менструальном цикле механизм, описанный выше, снижает уровень ФСГ в середине фолликулярной фазы цикла и в овуляцию уходит только один фолликул. Однако при индукции суперовуляции длительное воздействие экзогенного ФСГ позволяет фолликулам до 10 мм в диаметре избежать атрезии и достигнуть овуляторного размера. Долгое время существовали дискуссии, что важнее для множественного роста фолликулов — однократное воздействие высокой дозы ФСГ (превышение порога) или хроническое воздействие более низкой дозы ФСГ (расширение окна). В недавней работе B. Fauser и соавт. сравнили действие однократной высокой дозы ФСГ (375 мЕД), назначенной в самом начале менструального цикла, и низких доз ФСГ (75 мЕД), назначаемых ежедневно со 2—3-го дня менструального цикла. Выяснилось, что однократное воздействие высокой дозы ФСГ не влияет на формирование одиночного доминантного фолликула и лишь вызывает более бурный рост предоминантных фолликулов. В то же время хроническое назначение низких доз ФСГ позволяет фолликулам преодолеть механизм формирования одного доминантного фолликула и вызывает образование нескольких преовуляторных фолликулов [25]. Это свидетельствует о том, что расширение окна более, чем преодоление порога, важно для индукции суперовуляции.
За последние 40 лет индукция овуляции и суперовуляции претерпела значительные изменения. Первым препаратом, успешно примененным для индукции овуляции человека, был чГГ [26]. Однако широкое применение данного препарата было ограничено сложностью технологии изготовления и возможностью передачи болезни Крейнфельда—Якоба. В 1961 г. появились сообщения об использовании чМГ (B. Lunenfeld) и кломифенцитрата (R. Greenblaat) [26]. Использование этих двух препаратов в комбинации с хорионическим гонадотропином (ХГ) стало классической схемой для индукции овуляции одного или нескольких фолликулов до конца 80-х годов XX века. Мощной стимуляцией использования данного класса препаратов стала возможность совместить индукцию суперовуляции и проведение экстракорпорального оплодотворения с последующим переносом эмбрионов в полость матки. В середине 80-х годов прошлого века появились технологии очистки мочевых препаратов и резкого снижения содержания ЛГ, таким образом, появились мочевые препараты ФСГ — метродин в 1985 г. и высокоочищенный мочевой ФСГ — метродин-ВЧ в 1993 г.
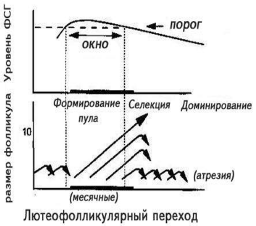 |
| Рис. 6. Теория окна/порога. |
Зависимость селекции доминантного фолликула в естествен ном цикле женщины от подъема уровня ФСГ. Рисунок воспроизведен из работы B. Fauser, A. van Heusden [40].
В конце 80-х годов XX в. было предложено и получило широкое применение в программах ЭКО использование препаратов агонистов люлиберина (а-ГнРГ). Данный класс аналогов люлиберина при начале назначения вызывает кратковременный подъем уровня гипофизарных гонадотропинов (так называемый «flare-up» эффект), но затем наступает стойкая десенсити зация гипофиза, что позволяет предотвратить преждевременный пик ЛГ. Из всех предложенных схем применения а-ЛГРГ стоит отметить так называемый длинный протокол, который включает в себя применение препаратов а-ГнРГ с середины лютеиновой фазы предшествующего стимуляции цикла до дня назначения овуляторной дозы ХГ.
Однако подлинной революцией в современной индукции суперовуляции стал синтез и применение рекомбинантных препаратов ФСГ (пурегон и фоллистим, «Органон» и гонал-Ф, «Сероно»). С первых контролируемых мультицентровых исследований выяснилось, что пурегон («Органон») является эффективным препаратом с точки зрения большего количества ооцитов, эмбрионов высокого качества и числа прогрессирующих беременностей, включая беременности после переноса размороженных эмбрионов [27]. В фолликулярной жидкости пациенток, у которых была получена беременность после применения пурегона («Органон») и ЭКО, обнаружена низкая концентрация тестостерона, что говорит о высоком качестве фолликулов и их низкой склонности к атрезии [34].
В конце 90-х годов прошлого века на рынке появились препараты антагонистов люлиберина (ант-ГнРГ), которые способны вызывать быстрое снижение выработки гипофизарных гонадотропинов и не имеют «flare-up» эффекта. Были предложены такие схемы применения ант-ЛГРГ, как ежедневные инъекции препаратов (по 0,25 мг подкожно) с 6-го дня стимуляции до дня назначения ХГ или введение однократно 3 мг препарата подкожно на 7—8-й день стимуляции. Несмотря на то, что рандомизированные исследования пока не показали преимуществ данной схемы стимуляции перед традиционным длинным протоколом, нельзя не отметить такие достоинства применения ант-ГнРГ, как более короткое время стимуляции, а также меньшее число ампул, необходимых для адекватного овариального ответа [28].
Другим важным вопросом современной индукции овуляции остается роль ЛГ. В соответствии с классической двухклеточной теорией стероидогенеза ЛГ необходим для адекватного синтеза андрогенов в клетках теки и в растущих фолликулах более 10 мм в диаметре, а также для синтеза эстрадиола в клетках гранулезы. У пациенток с выраженной гипофизарной недостаточностью назначение одного только ФСГ приводит к удовлетворительному фолликулярному росту, однако уровень эстрадиола в фолликулярной жидкости и в сыворотке крови сохраняется низким и эндометрий остается на уровне базального роста [37]. Однако при применении аналогов люлиберина в рекомендуемых стандартных дозах: агонистов люлиберина декапептила дейли («Ферринг») 0,05—0,1 мг ежедневно подкожно или препаратов антагонистов люлиберина — оргалютрана («Органон») или цетротайда («Аста-Медика»/«Сероно») в дозе 0,25 мг ежедневно подкожно уровень базального экзогенного ЛГ достаточен для адекватного синтеза эстрадиола [29, 30].
Дозировка препаратов для овуляторной дозы ХГ была разработана австралийскими учеными в конце 60-х годов прошлого века. Согласно их представлени ям, овуляция и окончательное созревание преовуляторных фолликулов после стимуляции препаратами ФСГ могут быть достигнуты дозой ХГ от 5000 до 80 000 мЕД [31]. Современные схемы используют от 5000 до 10 000 мЕД ХГ, однако к существенным недостаткам ХГ можно отнести высокую вероятность развития синдрома гиперстимуляции яичников, что связано с большой продолжительностью периода полужизни ХГ — 56 ч, тогда как время полужизни ЛГ только около 3—5 ч. Предложено применение рекомбинантного ЛГ в дозах от 15 000 до 30 000 мЕД. В недавнем рандомизированном контролируемом исследовании было показано, что данные дозы по эффективности могут быть сравнимы с дозой ХГ 5000 мЕД, однако частота гиперстимуляции меньше [32]. Другим новым методом достижения окончательной зрелости и индукции овуляции является назначение одиночной инъекции препарата а-ЛГРГ. Данное назначение вызывает выброс пика ЛГ гипофизом, по своим характеристикам сходным с естественным пиком. К преимуществам данного метода стоит отнести низкую вероятность синдрома гиперстимуляции, однако этот метод может быть применим лишь в циклах, в которых не используют препараты а-ЛГРГ, например, в схемах с ант-ЛГРГ или в схемах с применением только препаратов ФСГ и/или кломифенцитрата [33].
Ниже мы попытаемся ответить на сложные вопросы, касающееся фолликулогенеза и овариальной стимуляции, которые часто задают как коллеги, так и пациенты.
Может ли овариальная стимуляция, особенно многократная и с применением современных высокоактивных препаратов (рекомбинантного ФСГ, чМГ, а-ЛГРГ и ант-ЛГРГ) вызвать более раннюю менопаузу?
Могут ли операции на яичниках, такие, как односторонняя овариэктомия, резекция яичников, химиотерапия, облучение яичников, влиять на время наступления менопаузы?
Несомненно, могут. Стоит отметить, что если у женщины до 35 лет данные вмешательства влияют на время наступления менопаузы не столь значительно, то у женщин старшей возрастной группы данные вмешательства в большинстве случаев приводят к преждевременной менопаузе.
Может ли применение гормональных пероральных контрацептивов отсрочить менопаузу?
Скорее всего нет. Данные препараты влияют на процессы овуляции, тогда как собственно процесс роста фолликулов и их атрезии остается нетронутым.
Какие экологические факторы влияют на время наступления менопаузы?
Несмотря на то, что влияние окружающей среды на репродуктивную функцию человека является модной темой средств массовой информации, строгих научных исследований в данной области мало. В настоящее время доказано, что лишь курение снижает овариальный резерв, и длительное курение ускоряет наступление менопаузы на 2—3 года, причем если женщина все-таки отказывается от курения, показатели овариального резерва могут стабилизироваться.
Какие клинические симптомы связаны с началом процесса старения яичников женщины и как эти процессы влияют на эффективность вспомогательных репродуктивных технологий?
Возраст пациентки является одним из наиболее важных факторов, определяющих успех лечения бесплодия. Условия современной цивилизации и малая информированность пациенток и, зачастую, врачей о процессах старения репродуктивной системы женщины приводят к тому, что деторождение откладывается на долгий срок. Однако современные исследования показывают, что первые симптомы угасания репродуктивной функции появляются у женщины уже в 27—28 лет, когда статистически достоверно начинает повышаться базальный уровень ФСГ и снижается частота зачатия, рассчитанная на один менструальный цикл женщины. Интересно отметить, что собственно овуляторная функция женщины и регулярность менструального цикла не страдают до 45 лет, и такой важный диагностический признак для ановуляторного бесплодия, как наличие собственно овуляции, мало говорит о снижении репродуктивного потенциала у женщин старшей возрастной группы. Первым клиническим симптомом старения может служить сокращение продолжительно сти менструального цикла, которое происходит в конце четвертой декады жизни женщины и связано с укорочением фолликулярной фазы цикла. Стоит отметить, что только показатели овариального резерва, такие как базальный уровень ФСГ, тест с нагрузкой кломифенцитратом, наличие фолликулов при УЗИ яичников в начале цикла, могут говорить о процессах старения репродуктивной функции.
Может ли неоднократная стимуляция яичников вызывать повышенную частоту рака яичников и злокачественных заболеваний других локализаций?
Многочисленные эпидемиологические исследова ния последнего времени не показали зависимости между применением овариальной стимуляции при ЭКО и повышенной частотой рака яичников и таких заболеваний, как рак эндометрия, рак молочной железы, рак шейки матки. С другой стороны, отмечалось незначительное повышение частоты злокачественных и пограничных опухолей яичников у женщин, принимавших более 6 циклов кломифенцитрата, и поэтому не рекомендуется применять данный препарат при лечении бесплодия более 6 циклов.
1. Salha O., Abusheika N., Sharma V. Dynamics of follicular growth and in vivo oocyte maturation. Hum Reprod Update 1998; 4: 816—832.
2. Baker S., Spears N. The role of intra-ovarian interactions in the regulation of follicle dominance. Hum Reprod Update 1999; 5: 153—165.
3. Falck B. Site of production of oestrogen in rat ovary as studied in microtransplants. Acta Physiol Scand 1959; 47: 1—101.
4. Erickson G., Shimasaki S. The role of the oocyte in folliculogenesis. Trends Endocrinol Metab 2000; 11: 193—198.
5. Erickson G., Shimasaki S. The physiology of folliculogenesis: the role of novel growth factors. Fertil Steril 2001; 76: 943—949.
6. Faddy M., Gosden R. A mathematical model of follicle dynamics in the human ovary. Human Reprod 1995; 10: 770—775.
7. McGee E., Hsueh A. Initial and cyclic recruitment of ovarian follicles. Endocrin Rev 2000; 21: 200—214.
8. Perez G., Robles R., Knudson M., Flaws J., Korsmeyer S., Tilly J. Prolongation of ovarian lifespan into advanced chronological age by Bax — deficiency. Nat Genet 1999; 21: 200—203.
9. Teixeira J., Maheswaran S., Donahoe P. Mullerian inhibiting substance: an instructive developmental hormone with diagnostic and possible therapeutic applications. Endocrin Rev 2001; 22: 657—674.
10. de Wet A., Laven J., de Jong F., Themmen A., Fauser B. Antimulleran hormone serum levels: a putative marker for ovarian aging. Fertil Steril 2002; 77: 357—362.
11. Seifer D., MacLaughlin, Christian B., Feng B., Shelden R. Early follicular serum mullerian-inhibiting substance levels are associated with ovarian response during assisted reproductive technology cycles. Fertil Steril 2002; 77: 468—477.
12. Cook C., Siow Y., Brenner A., Fallat M. Relationship between serum mullerian-inhibiting substance and other reproductive hormones in untreated women with polycystic ovary syndrome and normal women. Fertil Steril 2002; 77: 141—146.
13. Fowler P., Tempelton A. The nature and function of putative gonadotopin surge — attenuating/inhibiting factor (GnSAF/IF). Endocrin Rev 1996; 17: 103—120.
14. Fowler P., Sorsa T., Harris W., Knight P., Mason H. Relationship between follicle size and gonadotropin surge attenuating factor (GnSAF) bioactivity during spontaneous cycles in women. Hum Reprod 2001; 16; 1353—1358.
15. Martinez F., Barri P., Coroleu B., Tur R., Sorsa-Leslie T., Harris W., Groome N., Knight P., Fowler P. Women with poor response to IVF have lowered circulating gonadotropin surge attenuating factor (GnSAF) bioactivity during spontaneous and stimulated cycles. Hum Reprod 2002; 17; 634—640.
16. Gougeon A. Regulation of ovarian follicular development in primates: facts and hypotheses. Endocrin Rev 1996; 17: 121—155.
17. Weestergaad L., Andersen C., Byskov A. Epidermal growth factors in small antral follicles in pregnant women. J Endocrinol 1990; 127: 363—367.
18. Mason H., Carr L., Leake R., Franks S. Production of transforming growth factor-a by normal and polycystic ovaries.
J Clin Endocrinol Metab 1995; 80: 2053—2056.
19. Zimmermann R., Xiao E., Husami N., Sauer M., Lobo R., Kitajewski J., Ferin M. Short-term administration of antivascular endothelial growth factor antibody in the late follicular phase delays follicular development in the rhesus monkey. J Clin Endocrinol Metab 2001; 86: 768—772.
20. Gregory L. Ovarian markers of implantation potential in assisted reproduction. Hum Reprod 1998; 13: Suppl 4: 117—132.
21. Chun S., Eisenhauer K., Kubo M., Hsueh A. Interleukin-1b suppresses apoptosis in rat ovarian follicles by increasing nitric oxide production. Endocrinology 1995; 136: 3120—3127.
22. Groome N., Illingworth P., O’Brien M. et al. Measurement of dimeric inhibin B throughout the human menstrual cycle. J Clin Endocrinol Metab 1996; 81: 1401—1405.
23. Ginter O., Wiltbank M., Fricke P., Gibbons J., Kot K. Selection of the dominant follicle in Cattle. Biol Repr 1996; 55: 1187—1194.
24. Levy D., Navarro J., Schattman G., Davis O., Rosenwaks Z. Exogenous LH: let’s design the future. Hum Reprod 2000; 15: 2258—2265.
25. Schipper I., Hop W., Fauser B. The FSH threshold/window concept examined by different interventions with exogenous FSH during the follicular phase of the normal menstrual cycle: duration, rather than magnitude, of FSH increase affects follicle development. J Clin Endocrinol Metab 1998; 83: 1292—1298.
26. Townsend S., Brown J., Johnstone J., Adey F., Evans J., Taft H. Induction of ovulation. J Obstet Gynec Br Com 1966; 73: 529—543.
27. Out H., Mannaerts B., Driessen S., Bennink C. Recombinant FSH (rFSH; Puregon) in assisted reproduction: more oocytes, more pregnancies. Results from five comparative studies. Hum Reprod Update 1996; 2: 162—171.
28. Huirne J., Lambalk C. Gonadotropin-releasing-hormone-receptor antagonists. Lancet 2001; 358: 1793—1803.
29. The Ganirelix Dose Finding Study Group. A double blind, randomized, dose-finding study to assess the efficacy of the Gn-RH antagonist ganirelix (Org 37462) to prevent premature LH surges in women undergoing ovarian stimulation with recombinant FSH hormone (Puregon). Hum Reprod 1998; 13: 3023—3031.
30. Janssens R., Lambalk C., Vermeiden J. et al. Dose-finding study of treptorelin acetate for prevention of a premature LH surge in IVF: a prospective, randomized, double-blind, placebo-controlled study. Hum Reprod 2000; 15: 2333—2340.
31. Brown J. Pituitary control of ovarian function — concepts derived from gonadotropin therapy. Aust N Z J Obstet Gynaec 1978; 18: 47—54.
32. The European recombinant LH study group Recombinant hLH is an effective, but saferthan, urinary hCG in inducing final follicular maturation and ovulation in IVF procedures: results of a multicenter double-blind study. J Clin Endocrinol Metab 2001; 86: 2607—2618.
33. Itskovitz-Eldor J., Kol S., Mannaerts B. Use of a single bolus of GnRH agonist triptorelin to trigger ovulation after GnRH antagonist ganirelix treatment in women undergoing ovarian stimulation for assisted reproduction, with special reference to the prevention of OHSS: preliminary report. Hum Reprod 2000; 15: 1965—1968.
34. Леонов Б.В., Кулаков В.И., Финогенова Е.Я., Козлова А.Ю., Беляева А.А., Кузмичев Л.Н. Использование препарата рекомбинантного ФСГ (фоллитропина- b) при лечении бесплодия в программах ЭКО. Акуш гин 2001; 6: 35—40.
35. Боярский К.Ю. Овариальная стимуляция и фолликулоге нез в конце 80-х: на пороге будущего. Пробл репрод 1997; 3: 4: 61—68.
36. Китаев Э.М. Элиминация половых клеток в процессе гаметогенеза и ее значение в репродукции. Акуш гин 1977; 86: 31—36.
37. Fauser B. Follicular development and oocyte maturation in hypogonadotrophic women employing recombinant FSH: the role of oestradiol. Hum Reprod Update 1997; 3: 101—108.
38. Baird D. A model for follicular selection and ovulation: lessons from superovulation. J Steroid Biochem 1987; 27: 15—23.
39. Baird D. Folliculogenesis and gonadotropins. In: Gonadotropins and fertility in the women. Eds Adashi E., Baird D. and Crosignani P. Serono Fertility Series, Roma 1999; 1—10.
40. Fauser B., van Heusden A. Manipulation of human ovarian function: physiological concepts and clinical consequences. Endocrin Rev 1997; 18: 71—106.
К.Ю. Боярский
Центр планирования семьи Пушкинского района, Санкт-Петербург
Вышло в свет «Руководство по климактерию»
(Под редакцией В.П. Сметник и И.В. Кулакова ).
Тел.: (095) 245-8620; 242-9110